리튬이온전지용 양극활물질 LiNi0.83 Co0.11Mn0.06O2의 전기화학적 특성에 미치는 Ce와 Nd 희토류 금속의 단독 혹은 이중 도핑효과
Effect of Single and Dual Doping of Rare Earth Metal Ce and Nd Elements on Electrochemical Properties of LiNi0.83 Co0.11Mn0.06O2 Cathode Lithium-ion Battery Material
Article information
Abstract
Layered LiNi0.83Co0.11Mn0.06O2 cathode materials single- and dual-doped by the rare-earth elements Ce and Nd are successfully fabricated by using a coprecipitation-assisted solid-phase method. For comparison purposes, nondoping pristine LiNi0.83Co0.11Mn0.06O2 cathode material is also prepared using the same method. The crystal structure, morphology, and electrochemical performances are characterized using X-ray diffraction (XRD), scanning electron microscopy (SEM), energy dispersive spectrometer (EDS) mapping, and electrochemical techniques. The XRD data demonstrates that all prepared samples maintain a typical α-NaFeO2-layered structure with the R-3m space group, and that the doped samples with Ce and/or Nd have lower cation mixing than that of pristine samples without doping. The results of SEM and EDS show that doped elements are uniformly distributed in all samples. The electrochemical performances of all doped samples are better than those of pristine samples without doping. In addition, the Ce/Nd dualdoped cathode material shows the best cycling performance and the least capacity loss. At a 10 C-rate, the electrodes of Ce/Nd dual-doped cathode material exhibit good capacity retention of 72.7, 58.5, and 45.2% after 100, 200, and 300 cycles, respectively, compared to those of pristine samples without doping (24.4, 11.1, and 8.0%).
1. 서 론
상업적인 리튬이온전지에 가장 많이 적용되고 있는 양 극재료는 274 mAh/g의 높은 이론용량을 가진 LiCoO2 (LCO)이다[1, 2]. 하지만 LCO는 충방전시 리튬의 함량변 화에 따른 구조변화 때문에 실제로 구현되는 가역용량 (~140 mAh/g)이 매우 낮고 또한 Co가 고가이고 독성이 있 기 때문에 새로운 양극활물질의 필요성이 인식되어 왔다 [3, 4]. 이에 지금까지 Co가 포함되지 않은 LiNiO2(LNO), LiMnO2(LMO) 그리고 LiFePO4(LFP)와 Co를 다른 원소 로 일부 대체한 층상구조의 LiNi1-x-yCoxMnyO2(NCM)와 LiNi1-x-yCoxAlyO2(NCA)가 LCO를 대체할 수 있는 후보 양 극활물질로 개발되었다. 이들 중에서 NCM은 높은 용량, 고율특성 그리고 우수한 안정성 등 전반적으로 특성이 뛰 어날 뿐만 아니라 가격이 저렴하여 소형 및 중대형 전지 에도 적용할 수 있다는 큰 장점 때문에 LCO 양극활물질 을 대체할 수 있는 가장 강력한 후보 물질로 평가받고 있 다[5-8]. 하지만 NCM은 낮은 이온전도성, 낮은 사이클 성 능과 탭 밀도(tap density)를 가지고 있으며, 특히 복잡한 제조공정이라는 문제점과 높은 용량을 얻기 위해 Ni의 비 율을 높이면 율속특성과 충방전시 용량이 감소한다는 단 점을 가지고 있다[6, 9-14]. 이러한 Ni함량 증가에 따른 전 기화학적 특성 감소의 두 가지 주요 원인은 부 반응(side reaction)과 구조 붕괴(structure degradation)이다. 부 반응 은 NCM입자 표면에 존재하는 리튬염들이 전해질과 반응 하여 NCM표면에 부도체 물질을 형성하거나 Ni4+이온이 전해질 분해를 가속화하여 두꺼운 고체 전해질 계면 (solid-state electrolyte interface; SEI)을 형성하는 반응을 말하고[15-18], 구조 붕괴는 Ni2+와 Li+의 자리교환 반응 (양이온 혼합)과 격자로부터 산소 손실에 기인한 층상구조 의 구조적 변화(혹은 붕괴)를 말한다[19-23]. 여기서 부 반 응은 전극의 전기전도성을 감소시키고 구조 붕괴는 충방 전시 Li이온의 이동을 방해하여 전기화학적 특성을 감소 시키는 역할을 하게 된다.
이전 연구자들은 상기 두 원인에 의해 감소하는 전기화 학적 특성을 개선 혹은 보완하기 위하여 두 가지 방법을 제안하였다. 하나는 NCM 표면을 다양한 물질로 코팅 (coating)하여 NCM과 전해질 사이의 부 반응을 줄이는 것 이고[24-26], 또 다른 하나는 NCM 표면 혹은 전체를 도 핑(doping)하는 것이다[27-34]. 표면 코팅은 NCM활물질 이 제조된 후에 부가적인 하소(calcination) 공정을 통하여 이루어지기 때문에 제조 비용이 증가하고 균일 코팅층을 얻기 어렵다는 단점을 가지고 있다. 이에 비해 도핑 공정 은 활물질 제조과정 중에 부가적인 공정없이 도핑물질만 을 추가하는 것이기 때문에 제조공정 측면에서 매우 큰 장점을 가지고 있고, 전기/이온 전도성 향상, 양이온 혼합 감소 그리고 결정구조 안정성 개선이라는 장점들을 동시 에 가지고 있기 때문에 표면 코팅보다는 장점이 매우 크 다고 할 수 있다. 이에 많은 연구자들은 여러 가지 양이온 (Na+[27], Mg2+[28], Mn4+[29], Ti4+[30], V4+[31], Zr4+[32], K+[33]) 혹은 음이온(F-[34]) 물질들을 NCM 양극활물질에 도핑하여 전기화학적 특성 개선을 보고하였다. 즉, 지금까 지 사용된 도핑물질은 주로 전이금속(transition metal), 알 칼리 토금속(alkaline earth metal), 할로겐 원소(halogen element)들이었으며, 희토류 금속에 대한 연구는 매우 제 한적이었다. 특히 Ni 함량이 80% 이상인 고 니켈계 NCM 양극활물질에서의 희토류 금속에 대한 도핑연구는 거의 없다.
따라서 본 연구에서는 희토류 금속 중에서 Ce와 Nd를 리튬이차전지용 고 니켈계 NCM양극활물질의 도핑물질로 선택하여 전기화학적 특성을 평가하고 그 결과를 비교하 였다. Ce와 Nd를 선택한 이유는 Nd는 리튬이차전지 소재 와 관련된 전극물질에서 비용량과 전기 전도성을 개선하 는 효과가 있는 것으로 알려져 있고 Ce는 사이클 성능과 율속 특성 개선에 효과가 있는 물질로 알려져 있기 때문 이다[35, 36]. 실험은 도핑을 하지 않은 경우와 Ce와 Nd를 각각 도핑한 경우 그리고 Ce와 Nd의 장점을 동시에 얻기 위해 두 물질을 혼합하여 도핑한 4가지 종류에 대해 실시 하였다.
2. 실험방법
NCM의 전구체인 Ni0.83Co0.11Mn0.06(OH)2는 기존에 잘 알려진 금속 황산염(NiSO4·6H2O, CoSO4·7H2O, MnSO4· H2O)을 물에 용해시키고 pH 조절 용액인 NaOH 및 착화 제로서 NH4OH를 사용하여 합성하는 공침법을 이용하였 다[10, 12, 37]. 제조된 전구체 Ni0.83Co0.11Mn0.06(OH)2 분말 과 리튬 원료인 LiOH(98%, Sigma-Aldrich) 그리고 도핑물 질이 첨가된 희토류 금속 산화물(Nd2O3; 99.99%와 CeO2; 99.99%, Sigma Aldrich)을 선택한 무게비로 정량한 다음 볼밀을 이용하여 균일하게 혼합하였다. NCM 양극활물질 시료는 총 4가지로 도핑하지 않는 것(이하 ‘LiNCM’으로 표기), Ce를 도핑한 것(이하 ‘Ce-LiNCM’으로 표기), Nd를 도핑한 것(이하 ‘Nd-LiNCM’으로 표기) 그리고 Ce와 Nd 를 동시에 도핑한 것(이하 ‘CeNd-LiNCM’으로 표기)이다. 도핑물질의 첨가 함량은 0.8%였으며, Nd와 Ce를 동시 에 첨가할 때는 각각 0.4%씩 첨가하여 총 0.8%를 첨가 하였다. 도핑물질의 첨가무게는 Nd를 예로 들면 Li (Ni0.83Co0.11Mn0.06)1-xNdxO2 화학식에 기준하여 계산하였다. 또한 리튬의 기화를 고려하여 Li/금속 비율은 1.05로 하였 다. NCM 양극활물질의 합성공정은 균일하게 혼합된 전구 체, LiOH 그리고 도핑물질을 O2분위기의 수평식 관상로 에 장입한 후 480°C에서 6시간 열처리한 다음 750°C까지 승온하여 20시간 열처리한 후 로냉하는 두 단계로 이루어 졌다. 제조된 4가지 NCM양극활물질의 결정구조와 입자 의 형태와 크기 그리고 도핑물질이 잘 분산되어 있는지를 알아보기 위해 XRD(DE/D2 PHASER, Bruker Co.), FESEM( JEOL, JSM-7610F) 그리고 EDS(FE-SEM에 부착된) 분석을 실시하였다.
합성된 4종의 NCM 양극활물질의 전기화학적 특성을 분석하기 위하여 CR2032(Ø20, T3.2 mm) 형태의 코인셀 을 사용하였다. Li 금속을 음극으로 사용하였으며, 양극제 조에는 도전재로 Super-P, 바인더로 PVdF를 사용하였고 전해질은 분리막(Celgard 2400)에 유기전해액을 함침하여 사용하였다. 전해액은 1:1 체적비를 갖는 Ethylene Carbonate (EC)/Diethyl Carbonate(DEC) 안에 1 mol의 LiPF6 리튬염 을 용해시켜 제조하였다. 셀의 조립은 아르곤 분위기의 글로브 박스 내에서 실시하였으며, 정전류 시험법 (Galvanostatic charge-discharge) 및 순환 전압-전류법 (Cyclic voltammetry, CV)을 위해 WBCS3000L(Won-A tech) 장비를 사용하였다. 이 때, Cut-off 전압은 2.8 - 4.6 V 이고, 정전류 시험법에서 전극 내 양극 활물질의 무게에 대한 0.5, 1, 5와 10 C-rate 전류밀도를 적용하였다. 순환 전압-전류법에서 주사속도는 0.2 mV/s로 설정하였다. 전지 내 저항 측정을 위한 전기화학 임피던스(Electrochemical impedance spectroscopy, EIS) 시험은 VMP3(BioLogic co.) 장비를 이용하여 10 mHz - 1 MHz의 주파수 범위로 분석 되었다.
3. 결과 및 고찰
그림 1은 본 실험에서 선택한 4가지 양극활물질(LiNCM, Nd-LiNCM, Ce-LiNCM, NdCe-LiNCM)에 대한 합성 후 결정구조를 관찰한 XRD결과이다. 4가지 양극활물질 모두 hexagonal의 α-NaFeO2 결정구조(R-3m 공간그룹)와 잘 일 치하는 회절픽으로 구성되었으며 다른 불순물에 관련된 회절픽은 관찰되지 않았다. 또한 (108)과 (110) 회절픽의 분리가 명확하게 관찰되는데 이는 잘 발달된 층상구조를 의미한다. Ce와 Nd의 단독 혹은 혼합 도핑에 따라서 XRD 회절픽은 변화가 없었는데 이는 본 연구에서의 도핑 이 LiNCM의 결정구조에 영향을 미치지 않았다는 것을 의미한다. 그림 1의 XRD결과를 이용하여 각 시료들의 격 자상수(lattice constant), 단위정(unit cell)의 부피 그리고 XRD의 (003)과 (104) 회절픽의 강도비율(intensity ratio,I(003)/I(104))을 구하여 표 1에 나타내었다. Nd와 Ce를 단독 혹은 혼합 도핑한 경우가 아무것도 도핑하지 않은 LiNCM 양극활물질에 비해 격자상수나 단위정의 부피가 전체적으로 증가하였다. 이는 Co3+/Mn4+보다 크기가 큰 Ce4+/Nd3+가 결정격자 내에 잘 도핑 되었다는 것을 의미하 고 더 나아가서는 Li이온의 이동속도를 높여 전기화학적 특성이 개선될 수 있다는 것을 의미한다[38].I(003)/I(104)와 c/3a 비율은 격자 내에 양이온 혼합의 정도를 결정하는 중 요한 인자이며,I(003)/I(104) 비가 1.2에 가까울수록 그리고 c/ 3a 비가 1.633에 가까울수록 양이온 혼합의 정도가 심한 것을 의미한다고 알려져 있다[6, 39]. 서론에서 언급한 바 와 같이 양이온의 혼합이 심해질수록 구조붕괴가 빨리 일 어나게 되고 이는 전기화학적 특성 감소로 이어지게 된다. 표 1에서 볼 수 있듯이 모든 시편에서I(003)/I(104) 비는 모 두 1.2보다 매우 높은 1.4 이상의 높은 값을 보였고 c/3a 비도 1.633보다 높은 값을 나타내었다. 이는 양이온 혼합 이 거의 없었거나 있더라도 매우 한정적으로 일어났다는 것을 의미한다. 또한 Ce와 Nd를 도핑을 하지 않은 것 보 다는 도핑을 한 것이 두 비율에서 모두 더 높은 값을 보 였고, c/3a와 I(003)/I(104) 비율은 각각 Ce-LiNCM시편과 Nd- LiNCM시편에서 가장 높은 값을 보였다. Ce와 Nd를 함께 도핑한 경우는 도핑을 하지 않은 경우에 비해서는 모두 높은 값을 보이지만 Ce와 Nd를 각각 도핑한 경우와 비교 해 보면 격자상수와 관련된 값에서는 낮은 값을 보인 반 면 I(003)/I(104) 비율은 중간 정도값(1.5970)을 보였다. 즉, 그 림 1과 표 1의 결과를 요약하면 도핑을 한 것이 하지 않 은 것에 비해 양이온 혼합을 더 많이 억제하는 효과가 있 어 전기화학적 특성이 높을 것으로 기대되나 Ce와 Nd를 각각 도핑한 것과 함께 도핑한 것의 전기화학적 특성을 미리 예측하기는 어려운 유사한 XRD 결과값을 보였다.
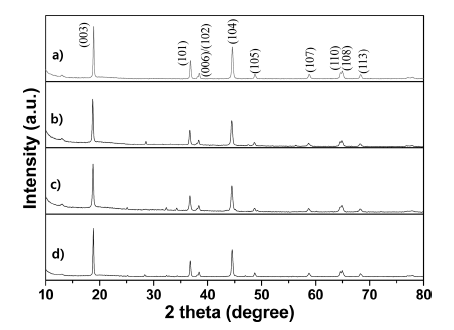
X-ray diffraction patterns of a) LiNCM, b) Ce- LiNCM, c) Nd-LiNCM and d) CeNd-LiNCM cathode materials.

Structural parameters and I(003)/I(104) of X-ray diffraction results for LiNCM, Ce-LiNCM, Nd-LiNCM and CeNd-LiNCM cathode materials
그림 2(a-c)는 NCM의 전구체인 Ni0.83Co0.11Mn0.06(OH)2 입자 그리고 그림 2(d-f)와 (g-i)는 각각 도핑은 하지 않은 LiNCM과 Ce와 Nd를 동시에 도핑한 CeNd-LiNCM 양극 활물질 입자의 형상을 관찰한 SEM결과이다. 주 입자는 전반적으로 균일한 구형의 형상을 하고 있었고 그 직경이 대략 10 um 정도였고, 주 입자를 이루고 있는 작은 입자 들은 형상이 불규칙하여 그 크기를 논하기는 어렵지만 대 략 1 um 이내의 크기였다. 그리고 NCM의 전구체(그림 2(a-c))와 NCM활물질(그림 2(d-i))의 주입자의 크기와 형 상은 유사하였으나 주 입자를 이루고 있는 작은 입자는 볏짚과 유사한 형상에서(그림 2(c)) 각진 입자의 형상으로 (그림 2(f,i)) 바뀐 것을 관찰할 수 있었다. Ce와 Nd를 각 각 도핑한 Ce-LiNCM과 Nd-LiNCM의 SEM이미지는 본 논문에 나타내지 않았지만 그림 2(d-i)에서 보여준 결과와 거의 유사하였다. 즉, 도핑 여부 혹은 도핑 재료와 상관없 이 외형적인 형상은 거의 유사하였다. 4가지 NCM 양극활 물질의 화학적 조성 및 각 원소들의 분포상태를 분석하기 위해 EDS분석을 실시하였고 대표적으로 CeNd-LiNCM활 물질의 결과를 그림 3에 나타내었다. 결과에서 볼 수 있는 것처럼 일부 도핑 물질이 모여 있는 부분이 있기는 하지 만 NCM전구체에 포함되어 있던 원소들뿐만 아니라 도핑 물질로 첨가한 원소들이 전체적으로 균일하게 잘 분포되 어 있다는 것을 확인할 수 있었다. 또한 본 논문에 나타내 지 않은 LiNCM, Ce-LiNCM 그리고 Nd-LiNCM 시료의 경우에도 첨가 혹은 도핑한 원소들이 매우 균일하게 분포 하고 있었다. 그림 1, 2 그리고 3의 결과를 통해 도핑을 하 지 않은 NCM양극활물질과 Ce와 Nd의 단독 혹은 혼합하 여 도핑한 NCM양극활물질의 전기화학적 특성을 평가 및 상호 비교할 수 있는 시료가 잘 준비되었다고 판단하였다.

EDS mapping of CeNd-LiNCM cathode materials: a) SEM image, b) Ni, c) Co, d) Mn, e) Ce, and f) Nd individually.
상기 제조된 4종의 양극활물질에 대한 전기화학적 특성 평가를 위해 수명특성, 저항특성, 고율특성 및 100 싸이클 후의 CV시험을 실시하였다. 그림 4a)는 합금분말 4종을 활물질로 각각 적용하고, NCM 무게에 대한 0.5C-rate의 전류밀도에서의 수명특성을 보여준다. 제조된 활물질을 적용한 셀의 초기용량은 각각 187.6, 190.9, 195.3과 191.2 mAh/g이었다. 그리고 100 싸이클 후 각각 81.6, 83.4, 82.2 와 95.3%의 특성용량이 유지되고 있음을 확인할 수 있었 다. 4종의 활물질을 각각 적용한 셀은 0.5 C-rate의 저 율 속에서 아주 큰 수명특성 차이가 나타나진 않았지만, CdNd-LiNCM이 가장 높은 용량유지율을, LiNCM이 가장 낮은 용량유지율을 보여주었다. 즉, Ce와 Nd의 단독 혹은 이중으로 도핑을 하면 사이클 특성이 개선된다는 것을 보 여주는 결과이다. 이러한 사이클 특성의 개선 결과는 Ce 와 Nd가 잘 도핑되어 Co와 Mn의 자리를 대체함으로써 격자와 관련된 값들(표 1 참조)을 도핑되지 않은 것에 비 해 더 크게 만들게 되고 이는 층상구조를 갖는 NCM 양 극활물질의 층간 공간을 더욱 넓게 만들어 리튬이온의 이 동을 더욱 용이하게 하기 때문으로 판단된다. 쿨롱 효율 (Coulombic efficiency, 충방전 효율)은 대표적으로 방전용 량이 가장 높은 CdNd-LiNCM에 대해 그림 4a)의 상단 부 분에 나타내었다. 초기 88.8%를 시작으로 100 싸이클까지 평균 99.15%의 높은 효율을 나타내었다. 그림 4b)는 0.5 C-rate에서 수명 특성이 가장 우수한 CeNd-LiNCM의 충 방전 곡선을 나타내었다. 본 활물질과 Li 이온의 반응구간 은 약 3.6 - 4.2 V임을 확인할 수 있었고, 방전용량에서 초 기 싸이클 후 용량이 약간 높아졌다가 점차 감소함을 확 인할 수 있었다. 즉, 어떤 특이한 분극현상 없이 안정적이 고 부드러운 충방전 거동을 나타내었다. 이러한 거동은 본 논문에 나타내지 않은 다른 3가지 종류의 NCM 양극활물 질에 대해서도 유사한 경향을 보였다.
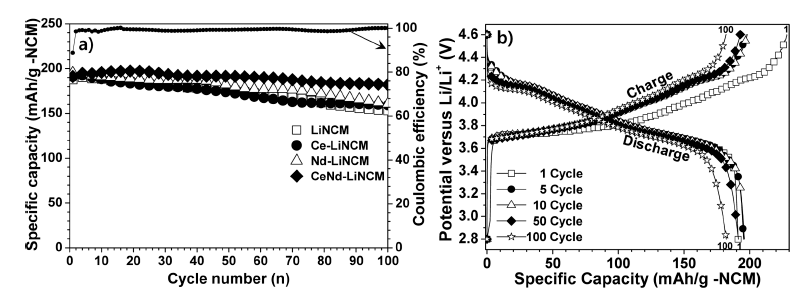
a) Cycle performance of cells using the LiNCM, Ce-LiNCM, Nd-LiNCM an CeNd-LiNCM at discharge of 0.5 C-rate and coulombic efficiency of CeNd-LiNCM cell and b) galvanostatic charge-discharge curves of CeNd-LiNCM cell.
그림 5는 도핑의 효과를 보다 잘 이해하기 위해 셀 내 의 활물질들의 싸이클 진행에 따른 저항 특성을 알아보기 위해 교류회로전기저항(EIS; electrochemical impedance spectra)분석하여 Nyquist plot을 결과로써 0.5 C-rate 전류 밀도에서 시험 전, 1, 30과 50 싸이클 후 활물질의 저항을 나타낸 것이다. 그림 5의 Nyquist plot에서 볼 수 있듯이 고주기(high frequency)에서 전극과 전해질 사이의 커패시 턴스에 해당하는 전하 전달 저항(charge transfer resistance) 을 나타내는 반원(semicircle)이 본 연구에서 준비한 4가지 NCM 전극 모두에서 나타났다. 이 전하 전달 저항은 리튬 이온의 삽입과 탈리, 전기 전도성 그리고 리튬이온의 거동 에 영향을 준다. 즉, 그 값이 낮을수록 전극의 전기화학적 특성은 개선된다. 그림 5에서 4가지 전극 모두 시험 전에 는 비교적 높은 저항을 유지하다가 1 싸이클 후 가장 낮 은 저항을 나타내었고 싸이클이 진행됨에 따라서 저항은 점점 커지는 경향이 있음을 확인하였다. 하지만 저항이 커 지는 정도는 도핑을 하지 않은 LiNCM시편에서 가장 확 연하게 나타났고, 도핑을 한 경우에는 사이클 진행에 따른 저항 증가폭이 많이 둔화되는 것을 볼 수 있다. CdNd- LiNCM 전극이 전 과정에서 가장 낮은 전하 전달 저항을 보여주었고, 시험 전, 1, 30과 50 싸이클 후 각각 101.7, 45.6, 46.4와 50.1 Ω의 결과를 확인하였다. 도핑을 함으로 써 전극과 전해질 사이의 전하 전달 저항이 개선된다는 것은 여러 가지가 복합적인 원인이 있을 수 있으나 대표 적인 한 가지는 도핑물질이 전해질의 분해를 억제하여 전 극물질과 전해질 사이의 반응에 의해 형성될 수 있는 고 체 전해질 계면(SEI; solid-state electrolyte interface)을 억 제했기 때문으로 분석할 수 있다. 즉, 그림 5는 Ce와 Nd 의 단독 혹은 혼합 도핑은 사이클 진행에 따른 전하 전달 저항의 증가를 억제하는데 매우 중요한 역할을 한다는 것 을 보여 주는 결과이다. 이러한 도핑에 따른 전하 전달 저 항의 개선은 그림 4a)에 나타낸 사이클 특성과도 잘 일치 한다.
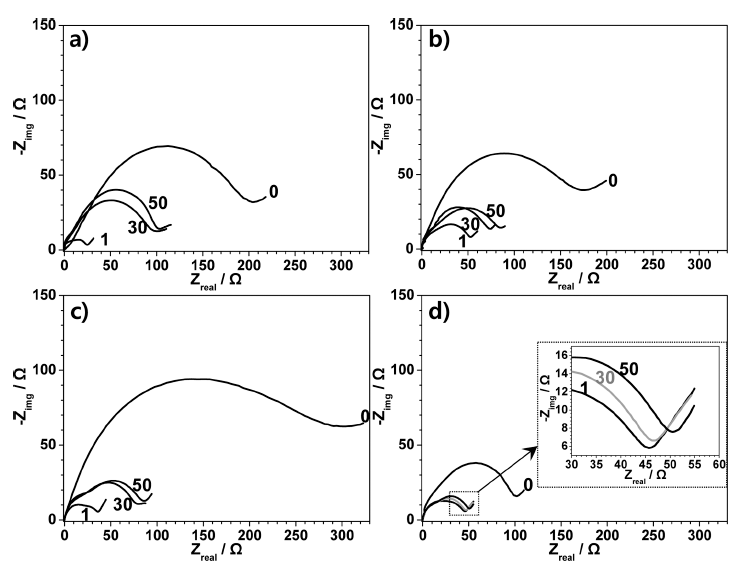
Nyquist plots from the impedance results of cells using the a) LiNCM, b) Ce-LiNCM, c) Nd-LiNCM and d) CeNd- LiNCM after 0, 1, 30 and 50 cycles.
그림 6a)는 본 연구의 활물질을 각각 적용한 셀을 5 Crate의 고율속으로 측정한 싸이클 특성이다. LiNCM, Ce- LiNCM, Nd-LiNCM 그리고 Ce/Nd-LiNCM 전극별 초기 방전용량은 166.2, 170.8, 164.3과 176.8 mAh/g, 100 싸이 클 후 방전용량은 각각 66.1, 152.2, 154.9과 143.9 mAh/g 그리고 300 싸이클 후 방전용량은 각각 29.5, 39.8, 39.4와 67.8 mAh/g으로써 100싸이클 후 용량유지율은 각각 39.8, 89.1, 94.3 그리고 81.4%이었고 300 싸이클 후 용량유지율 은 각각 17.7, 23.3, 24.0과 38.3%이었다. 또한 보다 높은 율속에서의 특성을 확인하고자 10 C-rate의 전류밀도를 인 가하여 시험하였고 그 결과는 그림 6b)에 나타내었다. 초 기 방전용량은 각각 145.7, 145.2, 148.7과 149.8 mAh/g, 100 싸이클 후 방전용량은 각각 35.5, 68.1 78.7과 108.9 mAh/g이었고 300 싸이클 후 방전용량은 각각 11.7, 64.7, 48.4와 67.7 mAh/g을 나타냄으로써 100 싸이클 후 용량유 지율은 각각 24.4, 46.9, 53.0 그리고 72.7%이었고 300 싸 이클 후 용량유지율은 각각 8.0, 44.5, 32.6과 45.2%이었다. 그림 4a)와 그림6a,b)를 함께 비교해 볼 때 도핑으로 사이 클 특성이 전체적으로 개선됨을 알 수 있었고, 특히 고율 (high C-rate)에서 도핑의 효과가 더 잘 발현된다는 것을 알 수 있었다. 또한 전반적으로 볼 때 CdNd-LiNCM 양극 활물질을 적용한 전지가 가장 초기 용량을 잘 유지하는 것을 확인할 수 있었다.
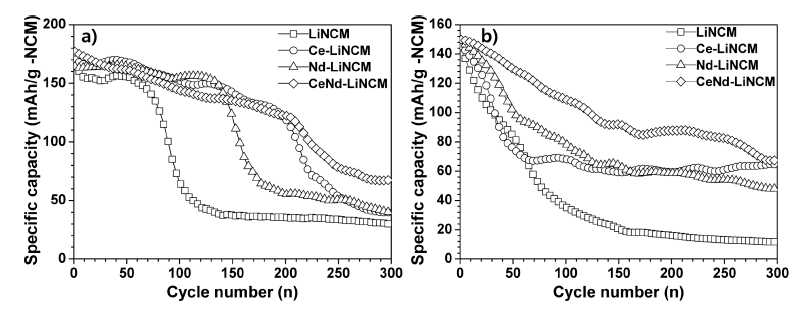
Cycle performances of cells using the LiNCM, Ce-LiNCM, Nd-LiNCM and CeNd-LiNCM at discharge of a) 5 C-rate and b) 10 C-rate
그림 7은 4종의 양극 활물질이 각각 적용된 전지의 다 양한 율속 특성을 평가한 결과이다. 적용된 율속은 순서대 로 0.1, 0.5, 1, 3, 5, 10과 0.5 C-rate로 측정하였으며, 마지 막 0.5 C-rate를 제외하고는 5 싸이클 씩 측정하였다. 각각 의 활물질이 적용된 전지는 1 C-rate까지는 비슷한 특성을 보여주다가 3 C-rate부터 점차 특성 차이가 나타났다. LiNCM의 경우 3 C-rate부터 가장 낮은 방전용량이 측정 되었고, 그 이후 5, 10과 0.5 C-rate의 결과에서도 가장 낮 은 방전용량을 보여주었다. 도핑을 하지 않은 LiNCM과 Ce와 Nd가 함께 도핑된 CeNd-LiNCM 전극에 대해 0.5와 10C에서의 방전용량을 비교해 보면 CeNd-LiNCM의 경우 0.5C 대비 10C에서의 방전용량은 50.5%이지만 LiNCM의 경우 39.7%로 낮은 유지율을 보였다. Ce와 Nd를 단독으 로 도핑한 경우도 각각 48.9%와 48.5%로 도핑하지 않은 LiNCM에 비해 높은 유지율을 보였다. 또한 10C에서 0.5C로 다시 되돌렸을 경우에도 도핑을 한 것이 도핑을 하 지 않은 전극보다 높은 방전용량을 나타내는 것을 볼 수 있었다. 이것은 도핑으로 율속특성이 개선되었다는 것을 의미하며, Ce와 Nd가 함께 도핑된 전극이 가장 좋은 율속 특성을 보였다.
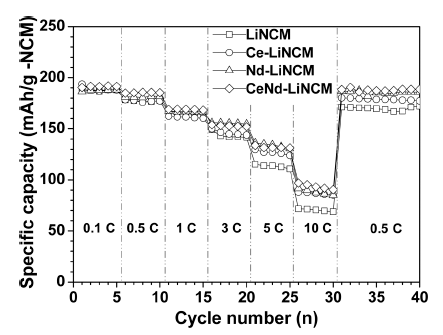
The rate capabilities of cells using the LiNCM, Ce- LiNCM, Nd-LiNCM and Ce/Nd-LiNCM at discharge of 0.5, 1, 3, 5, 10 and 0.5 C-rate in regular sequence.
그림 8은 0.5 C-rate의 전류밀도로 100 싸이클 후에 각 각의 활물질이 적용된 전지의 CV결과를 나타낸 것이다. 그래프 상단의 픽은 리튬이온이 격자에서 탈리되는 산화 반응이고 하단의 픽은 리튬이온의 삽입에 해당하는 환원 반응이다. 세부적으로는 3개의 산화(A-C)/환원(A'-C') 픽이 관찰되는데 리튬이온의 삽입과 탈리에 해당하는 주된 픽 은 산화반응에서는 3.9 V 근처의 픽(A로 표시된 픽)이고 환원반응에서는 3.6 V 근처의 픽(A'로 표시된 픽)이다. 그 림에서 볼 수 있듯이 도핑을 함으로써 산화/환응반응의 픽 이 이동하는 것을 볼 수 있다. 그림 8에서 주의 깊게 관찰 해야 하는 것은 산화/환원반응의 포텐셜(V)값 차이이다. LiNCM, Ce-LiNCM, Nd-LiNCM 그리고 Ce/Nd-LiNCM 전극의 주된 산화/환원반응의 포텐셜(V)의 차이 값(A-A') 은 각각 0.32, 0.31, 0.26 그리고 0.18 V이다. 즉, CeNd- LiNCM전극이 포텔셜 차이 값이 가장 적게 나타내었다. 이 차이 값이 적다는 것은 전극반응 동안 분극반응이 억 제되고 리튬이온의 가역성이 개선되는 것을 의미하는 것 으로 궁극적으로는 사이클 동안 용량을 잘 유지 할 수 있 다는 것을 의미한다.
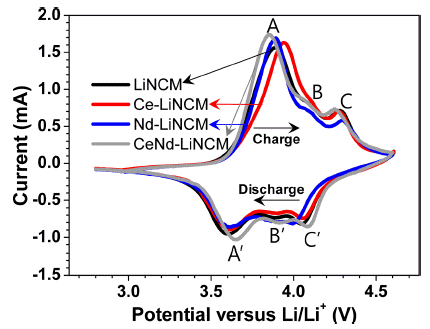
Cyclic voltammograms of cells using the LiNCM, Ce- LiNCM, Nd-LiNCM and CeNd-LiNCM applied with potential scan rate of 0.2 mV/s after 100 cycles at 0.5 C-rate.
이상의 결과를 간단히 요약하면, Ce와 Nd를 도핑하면 하지 않은 것에 비해 전기화학적 특성이 개선되며 특히 고율에서 도핑의 효과는 더 크게 나타났다. 또한, Ce와 Nd를 단독으로 도핑했을 때 보다는 함께 도핑을 했을 때 더 우수한 전기화학적 특성이 관찰되었는데 이는 그림 5 에 나타낸 임피던스의 결과에서 Ce에 의한 계면의 안전성 과 Nd에 의한 내부 전기전도성 개선의 영향으로 판단되나 정확한 원인규명을 위해서는 좀 더 연구가 필요하다.
4. 결 론
도핑없이(LiNCM) 그리고 Ce와 Nd의 단독(Ce-LiNCM, Nd-LiNCM) 그리고 이중(CeNd-LiNCM)으로 도핑된 층상 구조의 고 니켈계 NCM 양극활물질 Li(Ni0.83Co0.11Mn0.06) 을 공침법과 고상법을 이용하여 합성하였고 그 특성을 서 로 비교하였다. SEM 분석결과, 준비된 4가지 시편은 1 um 이하의 많은 작은 입자들이 모여 대략 직경 10 um 크기의 구형 입자를 이루고 있었고 이러한 양상은 도핑의 여부 그리고 도핑물질의 종류와 상관없이 유사하였다. EDS 분석결과, 도핑된 물질들은 모든 입자에서 균일하게 분포하고 있음을 알 수 있었다. XRD 분석결과, 4가지 양 극활물질 모두 hexagonal의 α-NaFeO2 결정구조(R-3m 공 간그룹)를 나타내었고 Ce와 Nd 도핑으로 단위 격자와 관 련된 값들은 조금씩 증가하였으며, 양이온 혼합 정도의 기 준이 되는 격자상수 c/3a와 회절픽의 강도 비율(I(003)/I(104)) 을 분석한 결과 도핑한 양극활물질이 하지 않은 것에 비 해 양이온 혼합의 정도가 낮게 분석되었다. 0.5, 5.0 그리 고 10 C-rate로 사이클 특성을 분석한 결과 도핑한 전극이 더욱 우수한 사이클 특성 및 안정성을 나타내었고 고율에 서 더 큰 효과를 보였다. 교류회로전기저항(EIS) 분석에서 도 도핑을 함으로써 리튬이온의 확산계수 증가를 의미하 는 전하 전달 저항이 낮게 나타났다. 결론적으로 Ce와 Nd 로 도핑된 NCM활물질이 도핑하지 않은 것에 비해 우수 한 전기화학적 특성을 보였으며, 특히 Ce와 Nd의 단독보 다는 함께 도핑한 것이 가장 우수한 결과를 보였으며, 도 핑 효과는 고율에서 더욱 개선된 결과를 보였다.
감사의 글
이 논문은 2017년도 경남과학기술대학교 대학회계 연구 비 지원에 의하여 연구되었음.

