내부 도핑 법에 의한 Cu 도핑 Cu:ZnSe 양자점의 수계 합성 및 발광 특성
Aqueous Synthesis and Luminescent Characteristics of Cu:ZnSe Quantum Dots by Internal Doping Method
Article information
Abstract
Cu-doped ZnSe quantum dots were successfully synthesized in an aqueous solution using an internal doping method. The effects of ligand type, CuSe synthesis temperature, and heating time on Cu-doped ZnSe synthesis were systematically investigated. Of MPA, GSH, TGA, and NAC used as ligands, MPA was the optimal ligand as determined by PL spectrum analysis. In addition, the emission wavelength was found to depend on the synthesis temperature of the internal doping core of CuSe. As the temperature increased, the doping of Cu2+ was enhanced, and the emission wavelength band was redshifted; accordingly, the emission peaks moved from blue to green (up to 550 nm). Thus, the synthesis of Cu:ZnSe using internal doping in aqueous solutions is a potential method for ecomanufacturing of colortuned ZnSe quantum dots for display applications.
1. 서 론
최근에 유해한 물질을 사용하는 Cd계 양자점의 대체 소 재로 친환경적인 셀렌화 아연(ZnSe)이 관심을 받고 있다. 또한, 다량의 폐수가 발생하는 유기용매를 대체하여 환경 친화적이며 합성 공정의 경제성을 향상시키기 위해 수계 합 성법이 대두되고 있다[1, 2]. ZnSe 양자점은 탈이온수를 사 용하는 수성 분위기에서도 입자가 안정적으로 합성된다는 특성이 있어 친환경 양자점 합성에 적합한 소재이다[3-5].
ZnSe는 InP, CdS 등의 다른 반도체 나노 입자들에 비해 넓은 에너지 밴드 갭(2.7 eV)을 가지고 있어 청색 발광이 가능하다. 발광 파장대는 380~410 nm 정도이며 가시광선 영역보다 근자외선 영역에 가까운 파장대이다. 따라서 가 시광선 영역의 청색 발광 ZnSe를 합성하기 위해서는 금속 이온의 도핑 등으로 발광파장의 조절이 요구된다[6-10].
Cu2+는 양자점 입자의 발광 파장대를 조절하기 위해 주 로 사용되는 금속 이온이다. Cu2+를 도핑할 경우, 양자점 의 밴드갭 사이에 새로운 에너지 준위를 생성하고 이로 인해 발광 파장대가 red-shift 하게 된다[11-14]. 양자점에 금속을 도핑하는 합성법은 대표적으로 표면도핑과 내부도 핑이 보고되고 있다. 표면도핑은 모체 양자점을 앞서 합성 하여 금속 이온을 표면에 도핑하는 방법이다. 양자점은 평 균 10 nm 이하의 입자로 표면적대 부피 비율이 커 표면이 매우 불안정하다. 따라서 표면에 금속이온이 도핑되면 공 기와의 접촉으로 도핑 물질이 산화가 되고 광소멸 현상이 빠르게 관찰된다[15, 16]. 이러한 표면도핑의 화학적 불안 정성을 개선하여 새로 고안된 합성법은 내부 도핑이다. 내 부도핑은 모체 양자점의 전구체와 불순물 즉, 금속이온을 동시에 성장시키는 합성법이다. 불순물이 모체 양자점과 함께 핵을 형성하게 되면 핵중심에 도핑이 되고 불순물이 표면이 아닌 내부에 존재하므로 화학적 안정성이 향상된 다[17-19].
내부도핑은 표면도핑에 비해 화학적 안정성이 뛰어나고 발광 특성을 향상시킬 수 있지만, 수계 ZnSe에서는 내부 도핑을 합성법으로 적용하는 다양한 연구가 진행되지 않 고 있다. 특히 리간드 종류에 따른 광학 특성에 대한 연구 가 부족한 실정이다. 수성 양자점은 유기 용매 내에서 합 성된 양자점에 비해 표면결함이 많아 안정성과 발광효율 이 낮다. 이를 개선하기 위해 리간드를 표면에 부착하게 되는데 리간드 종류에 따라 광학특성에 변화가 있다[20, 21]. 저자들은 이전 연구를 통해 ZnSe 양자점이 리간드에 따라 입자의 응집성과 발광 강도에 차이가 있음을 밝힌 바가 있다[22].
따라서 본 연구에서는 수계 분위기에서 내부도핑 합성 법을 연구하기 위하여 ZnSe에 Cu 도핑을 하였다. 리간드 의 종류가 양자점의 발광 안정성에 미치는 영향을 조사하 기 위해 다양한 리간드MPA, GSH, TGA, NAC를 사용하 였다. 리간드의 영향과 함께 전구체의 합성 온도, 가열 시 간을 변수로 하여 양자점의 발광특성을 분석하고 발광 파 장 제어에 대한 영향을 분석하였다.
2. 실험방법
2.1 시료
본 연구에서는 양자점 시료 합성에 분석등급의 시약을 사 용하였다. 사용된 고순도 시약은 zinc acetate(Zn(CH3COO)2, 99.99%), zinc nitrate hexahydrate(Zn(NO3)2·6H2O, 98%), copper nitrate trihydrate(Cu(NO3)2·3H2O, 99%), copper chloride dihydrate(CuCl2·2H2O, 99.95%), 3-mercaptopropionic acid (C3H6O2S, 99%), glutathione(C10H17N3O6S, 98%), thioglycolic acid(C2H4O2S, 99%), N-acetyl-L-cysteine(C5H9NO3S, 99%), sodium borohydride(NaBH4, 99.99%), Se powder(Se, 99.99%), sodium hydroxide(NaOH, 97%) 이다. 모든 시약은 Sigma- Aldrich에서 구매하였다.
2.2 표면도핑 Cu:ZnSe 나노 입자 합성
실험에서 사용되는 모든 용매는 탈이온수(deionized water, DIW) 이고 실험은 글로브박스 내의 N2 분위기에서 진행되었다. ZnSe 코어를 먼저 합성한 후 Cu 전구체를 주 입하였다. Zn 전구체는 DIW 50mL에 0.5 mmol zinc acetate 과 0.6 mmol glutathione(GSH) 을 용해시킨 후, NaOH를 사용하여 pH 11로 적정하였다. Se 전구체는 pH 12인 DIW 1 ml에 0.835 mmol의 NaBH4 환원제와 Se 분말 0.2 mmol를 초음파 세척기를 이용해 용해시킨 후, pH 12인 DIW 9 ml 추가로 주입하여 10mL의 Se 전구체를 합성하 였다. 교반 중인 Zn 전구체에 Se 전구체를 빠르게 주입하 였다. 가열은 90°C에서 1시간 진행하였다. Cu 전구체는 DIW 10 mL에 copper nitrate hexahydrate 0.01 mmol과 GSH 0.1 mmol를 용해시켜 pH 11로 조절하였다. 합성된 ZnSe에 Cu 전구체를 빠르게 주입하고 50°C에서 1시간 가 열 후 천천히 냉각시켰다.
2.3 내부도핑 Cu:ZnSe 나노 입자 합성
내부도핑 합성법은 총 3단계의 과정으로 진행되었다. 1 단계로Cu 전구체와 Se 전구체를 각각 합성했다. 2단계는 앞서 합성된 Cu전구체와 Se전구체를 반응시켜 CuSe를 합성하였다. 3단계는 가열 중인 CuSe에 Zn 전구체를 주 입하는 것으로 Cu:ZnSe를 합성하였다. Cu전구체 합성은 DIW 200 mL에 copper chloride dihydrate 0.012 mmol과 3-mercaptopropionic acid(MPA) 0.06 mmol 넣고 교반 후, NaOH 로 pH 11.4로 조정했다. 리간드 종류에 따른 실험 에서도 GSH, thioglycolic acid(TGA), N-acetyl-Lcysteine (NAC) 모두 MPA와 동일하게 0.06 mmol을 주입하였다. Se 전구체는 pH 11.8로 맞춘 DIW 1mL에 NaBH4 0.62 mmol과 Se 분말 0.15 mmol을 넣어 초음파 발생기로 용해 시켰다. Cu 전구체에 Se 전구체를 주입시키고 90°C까지 가열을 시켜주었다. CuSe의 가열온도에 따른 실험에서는 CuSe 합성온도를 25, 50, 70, 90°C로 변화시켰다. Zn전구 체는 DIW 3.5mL에 zinc nitrate 0.35 mmol과 MPA 0.7 mmol 넣고 교반 후, NaOH 로 pH 11. 4로 조정했다. 리간 드 종류에 따른 실험에서는 리간드를 각각 MPA, GSH, TGA, NAC로 변화시켜 0.7mmol로 동일하게 주입하였다. 90°C 인 CuSe에 Zn 전구체 1.5mL를 주입하였다. 10분 후, 2 mL의 Zn 전구체를 주입하고 1시간 동안 글로브 박스 내 에서 90°C로 열처리 후 서냉하였다.
2.4 특성 분석
합성된Cu:ZnSe 양자점 입자에 대해 PL spectroscope (FP-8500, Jasco사) 분광기를 사용하여 발광 특성을 분석 하였다.
3. 결과 및 고찰
3.1 도핑 공정 따른 Cu:ZnSe 특성
본 연구에서는 Cu2+를 ZnSe에 도핑하기 위하여 표면도 핑과 내부도핑의 두 가지 다른 공정을 적용하여 비교하였 다. 표면도핑은 그림 1(a)에서 보듯이 양자점 입자를 우선 적으로 합성한 후 금속 이온을 양자점 표면에 도핑하는 방법이다. 그림 1(b)는 표면도핑 합성법을 이용하여 같은 조건에서 3번의 재현성 실험을 한 Cu:ZnSe와 도핑하지 않 은 ZnSe 양자점의 PL 스펙트럼이다. 표면도핑 Cu:ZnSe는 GSH 를 리간드로 90°C에서 합성된 ZnSe에 구리 전구체 를 추가적으로 첨가하여 ZnSe 코어와 함께 성장시켜 합성 되었다. 이렇게 합성된 표면도핑 Cu:ZnSe의 PL스펙트럼 은 여러 파장대에서 피크가 나타났으며 발광 파장대가 넓 게 분포되었다. ZnSe의 PL 스펙트럼과 비교하면 표면도 핑 Cu:ZnSe 의 스펙트럼은 red-shift 되었으나 발광강도가 현저히 낮은 것을 볼 수 있다. 또한, 460 nm와 530 nm 부 근에서 발광 피크가 관찰되었다. 460 nm에서 나타난 발광 파장대는 벌크 크기의 ZnSe에 의한 것이다[23]. 이를 통해 Cu2+가 도핑 되지 않은 조대한 ZnSe 입자가 합성되었음을 확인하였다. 또한, 530 nm 부근에서 나타난 발광 피크의 강도에는 차이가 있었으나 Cu2+ 가 도핑이 되어 red-shift 된 입자가 존재함을 확인할 수 있었다. 표면 도핑된 양자 점의 PL 스펙트럼을 분석한 결과 발광 파장대가 board 하 게 분포하였으며, 순수ZnSe 나노 입자, ZnSe 벌크 입자와 Cu2+가 도핑된 ZnSe 입자 등 여러 형태의 입자가 공존하 는 것으로 판단되었다. 또한, ZnSe의 고유 여기 발광과 Cu2+으로 인한 발광을 제외하고 board 한 피크는 표면 트 랩에 인한 결함으로 생성된 것으로 광안정성이 낮은 것을 확인할 수 있다.
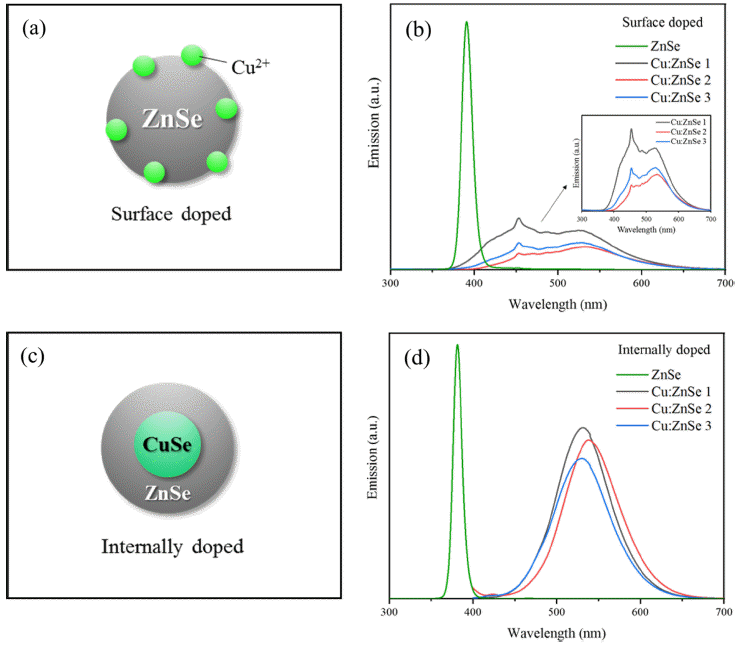
(a) Schematic of surface doping technique, (b) PL spectrum of Cu:ZnSe that was synthesized for reproducibility three times under the same conditions by surface doping method and PL spectrum of ZnSe, (c) Schematic of internally doping technique, (d) PL spectrum of Cu:ZnSe that was synthesized for reproducibility three times under the same conditions by internally doping method and PL spectrum of ZnSe.
내부도핑은 그림 1(c)와 같이 CuSe를 합성하여 핵형성 을 한 다음 Zn 전구체를 주입하여 불순물과 모체 양자점 을 동시에 성장시키는 합성법이다. 그림 1(d)는 내부도핑 법으로 합성된 같은 조건의 3번의 재현성 실험을 한 Cu:ZnSe와 ZnSe의 PL 스펙트럼이다. ZnSe의 PL 스펙트 럼과 비교하여 발광 파장대는 약 150 nm red-shift 하였다. 약 535 nm에서 하나의 발광 피크를 나타내는데 이는 Cu2+ 의 고유 여기 발광피크이다. 이는 ZnSe 에너지 밴드갭 사 이에 Cu2+의 에너지 준위가 생성되어 Cu2+의 도핑이 성공 적으로 이루어졌음을 나타낸다. 표면도핑 Cu:ZnSe에 비해 도핑이 되지 않은 ZnSe 입자가 감소하고 Cu2+가 도핑된 ZnSe 입자가 증가한 것으로 판단된다. 또한, 고유 발광 피 크만 존재하고 표면 결함에 의한 발광 피크는 감소한 것 을 통해 표면도핑 Cu:ZnSe에 비해 표면 안정성이 향상된 것을 알 수 있다[24]. 내부도핑 Cu:ZnSe는 화학적으로 안 정하며 높은 색 순도와 발광강도를 나타내므로 ZnSe 도핑 공정으로 적합한 것으로 판단된다.
3.2 리간드 종류에 따른 특성
본 연구에서는 다양한 리간드를 사용하여 Cu:ZnSe 양자 점을 합성하고 광학특성을 분석하였다. 모든 조건에서 리 간드는 동일한 몰수로 첨가하였다. 그림 2은 각각 MPA, GSH, TGA, NAC를 리간드로 사용한 Cu:ZnSe의 PL 스펙 트럼이다. 모든 조건에서 발광 파장대가 400 nm 이상에서 형성되어 발광이 red-shift 되었다. 이는 기존의 ZnSe의 발 광 파장대인 약 380 nm보다 20 nm 이상 이동하였으므로 모든 조건에서 Cu2+가 도핑 되었음을 확인하였다. GSH를 리간드로 사용한 경우 다른 리간드에 비해 짧은 파장대인 490 nm에서 발광피크가 나타났으며 스펙트럼의 양상이 뚜렷하지 않고 반치폭이 넓었다. GSH를 제외한 나머지 리간드는 발광피크가 약 500~550 nm를 나타나며 MPA를 사용한 경우 가장 발광 강도가 강하였으며 장파장으로 이 동도 우수하였다. TGA와 NAC를 사용한 경우 발광강도는 낮은 값을 보였다. 결론적으로 MPA를 리간드로 사용한 경우 발광강도가 우수했으며 좁은 반치폭과 양호한 redshift을 보여 구리 도핑 ZnSe 양자점 합성에 최적 리간드 로 판단되었다.
3.3 CuSe 전구체 가열 온도의 영향
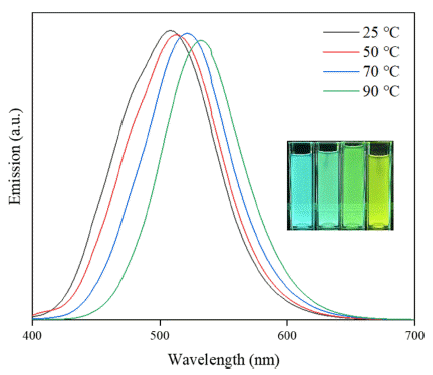
CuSe를 합성하는 과정에서의 가열온도에 따른 발광특 성을 관찰하기 위해 25°C부터 90°C까지 가열온도를 조 절하였다. 양자점 입자의 합성은 우선 각각의 가열온도 에서 CuSe 합성한 후에 Zn 전구체를 넣고 90°C에서 1시 간 가열을 하였다. 그림 3는 CuSe 합성 온도에 따른 PL 스펙트럼이다. 합성 온도가 증가할수록 red-shift되어 긴 파장대로 이동하는 것을 확인할 수 있다. 25°C부터 90°C 까지 각각의 발광피크는 506.5 nm, 513.5 nm, 521 nm, 531 nm로, 파장대 변화 폭이 온도에 따라 평균 8 nm씩 증가하였다. 높은 온도에서 CuSe입자 형성이 활성화되었 고 결과적으로 양자점 합성 시 Cu2+의 도핑도 증가하여 발광 파장대의 차이가 발생한 것으로 판단된다[25]. 한편 온도변화에 따른 발광 스펙트럼의 강도는 차이가 크지 않았다.
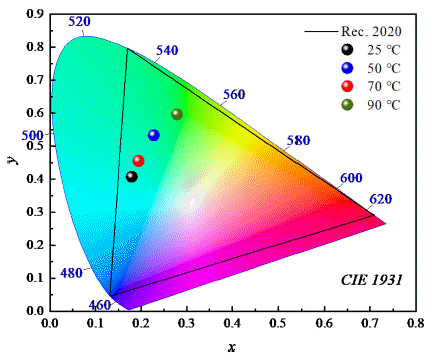
그림 3에 삽입된 발광 사진을 보면 청색에서 녹색으로 발광색이 변하는 것을 확인할 수 있다. 25°C에서 CuSe를 합성한 Cu:ZnSe는 발광 파장대가 가장 짧으므로 청색 발 광을 나타내는 것을 관찰할 수 있다. CuSe 가열 온도가 증 가할수록 발광 파장대가 red-shift 되며 그에 따라 발광색 도 점차 녹색으로 변하였다. 90°C에서 합성된 Cu:ZnSe 는 완연한 녹색을 띄고 있다. 그림 4는 온도 별로 합성된 양 자점에 대한CIE 색좌표이다. 합성 온도에 따라 색좌표가 일정하게 변하는 것을 볼 수 있다. 합성 온도가 증가할수 록 색좌표 위치가 녹색으로 점차 이동하였다. 각각의 CIE 좌표는 25°C(0.179, 0.408), 50°C(0.194, 0.456), 70°C(0.228, 0.534), 90°C(0.279, 597)로 청녹색 방출을 나타낸다. 또한, Rec. 2020 색영역에 속하는 것을 확인할 수 있다.
3.4 Cu:ZnSe 합성 시간의 영향
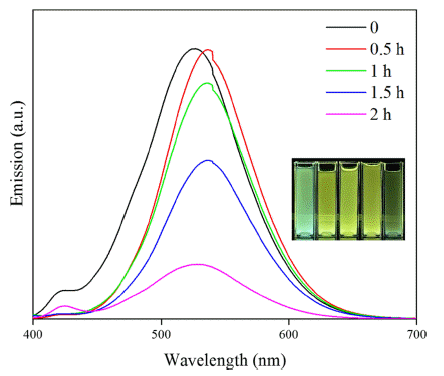
그림 5는 Cu:ZnSe 양자점 합성 시 시간 변화에 따른 발 광특성을 비교한 PL 스펙트럼이다. 합성온도는 90°C였으 며 합성을 위한 가열시간은 30분 간격으로, 가열을 하지 않았을 때부터 가열 2시간까지 분석하였다. 가열을 하지 않았을 때의 Cu:ZnSe는 두 가지의 발광 피크가 확인되었 다. 주 발광 피크는 약 526 nm였으며, 가열을 오랜 시간한 시료에 비해 red-shift가 상대적으로 가장 적었다. 또한, 약 426 nm에서의 발광 피크가 관찰되는데 이는 중심물질인 ZnSe 코어의 발광 피크로 판단된다. Cu2+와 ZnSe의 핵형 성을 위한 충분한 가열 시간이 주어지지 않아 ZnSe와 Cu:ZnSe의 발광 피크가 동시에 확인되어 Cu2+가 불완전하 게 도핑 되었음을 알 수 있다. 그림 5에 삽입된 발광 사진 에서도 알 수 있듯이 가열을 하지 않은 Cu:ZnSe는 청녹색 을 띄고 있다. 가열 30분 이상부터는 발광파장대가 유사 한 것을 볼 수 있다. 가열 시간이 증가할수록 ZnSe 코어 의 발광 피크가 약해지고 Cu:ZnSe의 발광 피크가 강해지 며 red-shift 된 것을 확인하였다. 이때의 발광 피크는 536 nm로, 가열하지 않았을 때의 피크와 비교하여 약 10 nm 정도 red-shift 되었다. 또한, 발광 사진에서 볼 수 있듯이 가열 30분 이상의 샘플은 완연한 녹색을 발광하고 있다. 하지만 가열 1시간 이상부터 급격히 발광 강도가 감소하 였다. 가열 2시간의 PL 스펙트럼에서 536 nm의 발광강도 는 가열 30분 대비 80% 감소하였다. 가열 30분 이상부터 강도가 약해졌던 ZnSe 발광 피크가 다시 생성되었다. 가 열 시간이 증가하게 되면 반응성이 증가하여 Cu2+의 도핑 또한 증가하였지만 적정 가열 시간 이상으로 합성하게 되 면 티올 리간드의 열분해로 강도가 감소하게 되며 입자 응집이 발생하게 된다. 따라서 Cu:ZnSe의 최적의 가열 시 간은 1시간으로 판단하였다.
4. 결 론
본 연구는 내부도핑법을 이용하여 Cu2+를 ZnSe에 도핑 하였고 표면도핑과 내부도핑 합성법을 비교 분석하여 다 음과 같은 결론을 얻었다.
표면도핑법으로 합성된 Cu:ZnSe는 PL 스펙트럼이 양 상이 뚜렷하지 않았으며 도핑이 불완전하게 된 ZnSe 입자의 존재를 확인하였다. 반면 내부도핑법으로 합 성된 Cu:ZnSe는 Cu2+가 도핑되어 단일 발광피크가 관찰되었고, 발광파장도 red-shift되었으며 높은 색순 도를 보였다. 따라서 ZnSe에 Cu2+를 도핑하는 공정으 로는 내부도핑이 적합한 것으로 판명되었다.
내부도핑이 적용된 Cu:ZnSe의 발광 특성은 리간드 종류에 따라 변하는 것을 확인하였다. 리간드로 MPA, GSH, TGA, NAC를 사용하여 양자점을 합성하고 발 광 특성을 분석한 결과 MPA 가 최적의 리간드 조합 임을 밝혔다. 리간드로 MPA를 사용한 경우 발광 파 장대가 약 535 nm로 충분히 red-shift 되었으며 발광 강도도 향상되었다.
내부 도핑 시 전구체의 합성온도가 발광 파장의 이동 에 영향을 미치는 것을 확인하였다. 가열온도가 증가 할수록 발광 파장대가 긴 파장대로 이동하였고, 발광 색도 청녹색에 녹색으로 변하였다. 이는 색좌표의 이 동으로 재확인하였다.
양자점 입자 합성시간도 발광특성에 영향을 미치는데, 최적 시간은 1시간 이하인 것으로 나타났다. 합성시 간이 증가할수록 도핑되지 않은 ZnSe입자의 발광 피 크는 약해지는 반면 Cu:ZnSe의 발광피크는 강해졌다. 하지만 1시간 이상의 가열은 리간드의 열분해를 촉진 시켜 발광특성을 약화시켰다. 결론적으로 수용액에서 내부 도핑을 사용한 Cu:ZnSe 합성에 대한 공정 최적 화는 색상을 조정할 수 있는 ZnSe 양자점의 친환경적 제조 방법을 제시하였으며, 향후 LED 소자 합성 공 정에 활용될 수 있을 것이다.