Articles
- Page Path
- HOME > J Powder Mater > Volume 30(4); 2023 > Article
-
Article
분말 합성법(Sol-Gel & Solid-State reaction)에 따른 Lithium Lanthanum Titanate 분말의 입자 및 결정 크기 비교 분석에 관한 연구 - 윤정재a,b, 이승환a, 백소현a, 권용범a, 송요셉c, 김범성c, 이 빈d, 곽노균b, 정다운a,*
- A Study on Particle and Crystal Size Analysis of Lithium Lanthanum Titanate Powder Depending on Synthesis Methods (Sol-Gel & Solid-State reaction)
- Jeungjai Yuna,b, Seung-Hwan Leea, So Hyun Baeka, Yongbum Kwona, Yoseb Songc, Bum Sung Kimc, Bin Leed, Rhokyun Kwakb, Da-Woon Jeonga,*
-
Journal of Korean Powder Metallurgy Institute 2023;30(4):324-331.
DOI: https://doi.org/10.4150/KPMI.2023.30.4.324
Published online: July 31, 2023
a 한국생산기술연구원 한러혁신센터
b 한양대학교 융합기계공학과
c 한국생산기술연구원 한국희소금속산업기술센터
d 경희대학교 정보전자신소재공학과
a Department of Korea-Russia Innovation Center, Korea Institute of Industrial Technology, Incheon 21655, Republic of Korea
b Department of Mechanical Convergence Engineering, Hanyang University, Seoul 04763, Republic of Korea
c Department of Korea Institute for Rare Metal, Korea Institute of Industrial Technology, Incheon 21655, Republic of Korea
d Department of Advanced Materials Engineering for Information and Electronics, Kyunghee University, Yong-in 17104, Republic of Korea
- * Corresponding Author: Da-Woon Jeong, TEL: +82-32-226-1362, FAX: +82-32-226-1374, E-mail: dwjeong@kitech.re.kr
- - 윤정재·이승환·백소현: 학생연구원, 권용범: 연구원, 송요셉·정다운: 선임연구원, 김범성: 수석연구원, 이 빈·곽노균: 교수
© The Korean Powder Metallurgy Institute. All rights reserved.
- 1,671 Views
- 19 Download
Abstract
- Lithium (Li) is a key resource driving the rapid growth of the electric vehicle industry globally, with demand and prices continually on the rise. To address the limited reserves of major lithium sources such as rock and brine, research is underway on seawater Li extraction using electrodialysis and Li-ion selective membranes. Lithium lanthanum titanate (LLTO), an oxide solid electrolyte for all-solid-state batteries, is a promising Li-ion selective membrane. An important factor in enhancing its performance is employing the powder synthesis process. In this study, the LLTO powder is prepared using two synthesis methods: sol-gel reaction (SGR) and solid-state reaction (SSR). Additionally, the powder size and uniformity are compared, which are indices related to membrane performance. X-ray diffraction and scanning electron microscopy are employed for determining characterization, with crystallite size analysis through the full width at half maximum parameter for the powders prepared using the two synthetic methods. The findings reveal that the powder SGR-synthesized powder exhibits smaller and more uniform characteristics (0.68 times smaller crystal size) than its SSR counterpart. This discovery lays the groundwork for optimizing the powder manufacturing process of LLTO membranes, making them more suitable for various applications, including manufacturing high-performance membranes or mass production of membranes.
- 전기 자동차(EV; Electric Vehicle) 분야를 필두로 하는 차세대 모빌리티 산업은 비약적인 성장을 이루고 있다. 이 로 인해 EV배터리와 같은 이차전지의 핵심 소재인 리튬 의 수요와 가격은 급증하는 추세이다[1-4]. 현재 리튬의 주요 공급원은 육지의 광석 혹은 염수이지만 향후 다양한 차세대 산업군(UAV, 드론, 친환경선박, 전자기기, 이차전지 등)에서 필요로 하는 예측 수요량에 비하면 활용 가능한 매장량은 매우 한정적이다. 이처럼 예견되는 리튬 공급 부 족 문제를 해결하고자, 최근 몇 년 사이 새로운 리튬 공급 원에 대한 조사와 더불어, 증가하는 수요를 대응하기 위한 리튬을 추출 자원화 기술에 대한 연구가 활발히 이루어지 고 있다[3-7,9,10].
- 그 중에서도 해수는 지구의 지질학적 특성으로 인한여 무한히 리튬을 함유하고 있는 리튬 공급원으로 육지의 리 튬 매장량보다 약 1,000배 많은 2,300억 톤을 함유하고 있 는 것으로 알려져 있다[5]. 그러나 해수에서 리튬을 추출 하는 기술은 매우 적은 리튬 농도(약 0.2 ppm)에 비해 그 용존량이 높은 1,2가 양이온(Na+, K+ 그리고 Mg2+ 등)의 존재로 인하여 그 기술의 난이도가 매우 높다[6-8]. 1세대 기술이라고 부를 수 있는 흡/탈착 또는 전기분해 기술에 대한 연구와 1세대 기술의 한계점을 보완한 2세대 기술인 전기투석법을 기반으로 하는 리튬 추출 기술에 관한 연구 가 진행되고 있다[5,9,10].
- 본 기술은 원수가 되는 리튬을 함유한 용액에서 리튬 이 온을 선택적으로 추출이 가능한 멤브레인을 활용하여, 전 기투석법의 원리로 직접적으로 리튬을 추출하는 시스템 (DLE; Direct Lithium Extraction)이다. 이 시스템 연속공정 이 가능하다는 점에서 1세대 기술이 지닌 효율성 측면의 한계를 극복 가능하다. 이와 더불어, 시스템에 활용 가능한 원수로는 리튬 농도가 매우 낮은 해수뿐만 아니라, 리튬 농 도가 비교적 높은 염수, 담수시설 농축 폐수, 폐배터리 블 랙파우더가 용해된 용액 등 그 활용 범위가 매우 넓으며, 리튬 추출 효율 또한 더욱 높을 것으로 기대된다[4,10].
- 전기투석법을 기반의 리튬 추출 기술에서의 핵심 소재 인 리튬이온 선택성을 갖는 멤브레인으로 전고체 전지(all solid-state battery)의 고체전해질(solid-state electrolyte)이 주목받고 있다. 나트륨 초이온 전도체(NASICON; Sodium super ionic conductor), 황화물계 고체전해질, 산화물계 고 체전해질 등이 활발히 연구 중에 있으며, 특히, 페로브스 카이트 형(perovskite-type) 구조를 갖는 Lithium Lanthanum Titanium Oxide(LLTO)가 해수 및 전기투석 공정 간의 다 변적인 용액 환경 내에서 뛰어난 안정성을 가진다. 나시콘 형(NASICON-type) 고체전해질은 이온 전도도와 리튬 금 속에 대한 불안정성이 문제가 되며, 황화물계 고체전해질 은 수분에 노출 시에 화학적 반응으로 인한 불안정성으로 사용이 제한된다. 대표적인 가넷 형(Garnet-type) 구조의 Lithium Lanthanum Zirconium Oxide(LLZO)는 이온전도 도와 리튬 금속에 대한 안정성이 우수하지만, 공기 또는 물과의 반응성 및 계면에서의 높은 저항으로 인하여 사용 이 제한된다[11,12].
- ABO3(A = Li, La; B = Ti) 페로브스카이트 구조의 LLTO (Li3xLa(2/3-x)TiO3) 고체전해질은 해수 및 용액 환경에서 응 용하기 적합한 산화물계 고체전해질이다. 그 중에서도 Li0.33La0.56TiO3(x=0.11)는 이온 전도도가 가장 높다고 알려 져 있으며, 리튬 추출의 효율을 높이기 위해서는 LLTO 멤 브레인 성능의 최적화가 중요하다[13]. 리튬 이온의 투과 성(이온 전도성) 및 선택성은 멤브레인의 성능을 판단하는 주요 인자이며, 특히 리튬 이온 투과성이 멤브레인의 효율 을 결정짓는 중요한 요소이며, 이를 향상시키기 위해 리튬 이온 전도를 저해하는 요소인 내부 입계(grain boundary) 저항을 감소하여야 하며, 동시에 멤브레인의 두께를 감소 하여야 한다[14-17]. 일반적으로 알려진 Li0.33La0.56TiO3의 내부 입자(bulk) 내의 이온전도도(σb)는 10-3 S cm-1인 반 면, 입계 저항(grain boundary resistance)으로 인해 총 이 온전도도(σt)는 10-5 S cm-1 수준이다[20]. 따라서 LLTO 내 부의 입계가 차지하는 영역을 줄이는 연구가 지금까지도 활발하게 진행되고 있다. 또한 기계적 안정성을 유지하면 서 멤브레인의 두께를 얇게 제어하기 위하여 분말 압축, Tape-casting 등의 분말 성형 공정에서 미세 분말 활용이 필수적이다[18,19]. 입자의 크기가 크면 소결 과정에서 입 자의 성장이 상대적으로 크며 같은 단위 면적에서 입계가 차지하는 영역이 줄어들기 때문에 앞서 언급한 두 가지 기술적 요소 모두 LLTO 분말의 입자 및 결정 크기와 연 관이 깊다. 하지만, 분말의 입자가 크면 분말 성형 공정 및 소결 공정을 거친 멤브레인의 두께를 얇게 제어하는 데에 어려움이 존재함으로 향후 이를 극복하기 위한 연구가 요 구된다.
- 본 연구에서는 앞서 소개한 DLE 시스템에 적용이 가능 한 LLTO 소재 합성을 위해 Sol-Gel reaction(SGR)[10,21] 및 Solid-State reaction(SSR)[18] 두 가지 공법으로 LLTO 분말을 제조하였다. LLTO 분말 합성 시에는 전통적으로 산화물과 탄산염의 분말 혼합물로부터 LLTO 화합물을 얻 는 SSR 공법이 많이 사용되었으나, 리튬 손실을 유발하는 장시간의 고온에서의 열처리가 필요하다는 단점으로 인하 여 Pechini 합성법을 기반으로 하는 SGR 공법이 대안으로 제시되었다[22]. SGR공법은 전구물질들을 습식 공정으로 혼합하여 Sol을 형성하고, 이에 열을 가해 반응을 시켜 Gel 형태의 중합체를 생성하고, 이를 하소하여 화합물 분 말을 얻는 합성 방법이다. 이 공법은 작고 균일한 반응물 을 얻기에 효과적이지만 공정이 복잡하며 대량의 분말을 제조하기에 한계가 존재한다. SSR공법은 건식공정으로, 전구물질을 분말 상태로 볼과 함께 혼합 및 분쇄하며, 최 종적으로 하소하여 화합물 분말을 얻는 합성 방법이다. 이 합성법은 공정이 간단하며, 대량의 분말을 제조하기에 적 합하지만, 입자가 비교적 크며 균일하지 않다.
- 이러한 소재 합성 공법(SGR 및 SSR)에 따라 제조한 각 LLTO 분말의 XRD, SEM 분석을 통하여 입자 및 결정 크 기의 비교하였다. 이를 바탕으로 차세대 EV 산업의 핵심 소재인 리튬을 해수에서 추출이 가능한, 고성능의 리튬이 온 선택성을 갖는 LLTO 멤브레인 제조에 적합한 분말 합 성법을 선정하고자 하였다.
1. Introduction
- 2.1 Sol-Gel Reaction 공정을 통한 분말 합성
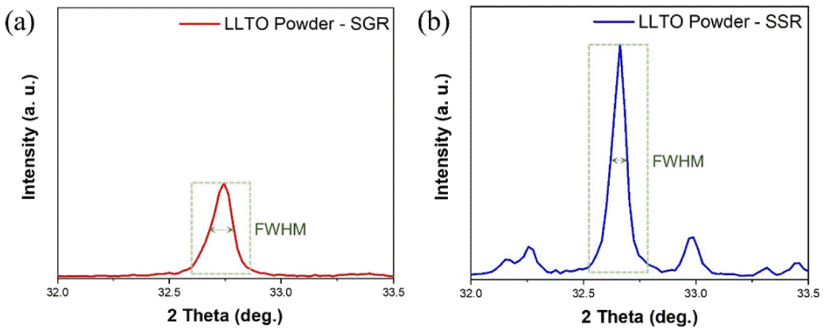
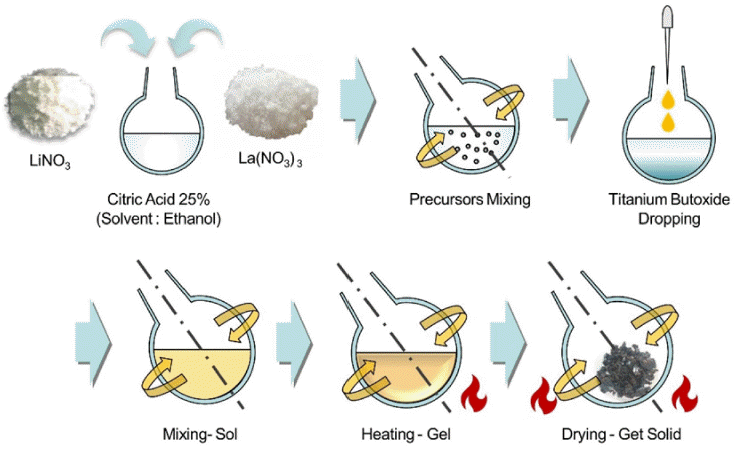
- 졸-겔 반응법으로 LLTO 분말을 합성하기 위해 Fig. 1과 같이 전구체인 LiNO3(99.99%, Sigma-Aldrich), La(NO3)3· xH2O(99.9%, Sigma-Aldrich)를 25%의 Citric Acid 용액에 혼합하였으며, 이 때, 용매로는 건조 단계에서의 원활한 증발을 위해 에탄올을 사용하였다. 혼합한 용액을 Rotary Evaporator(RV 10 digital V, IKA)를 이용하여 회전 교반하 여 완전히 용해시킨 후, Titanium(IV) butoxide(97.0%, Sigma-Aldrich)를 떨어뜨린 후 100 rpm의 회전속도에서 80°C의 오일 베스로 중탕 가열하여 균일한 용액을 얻었다. 최종 용액에서 L iNO3, La(NO3)3, titanium(IV) butoxide 및 citric acid의 몰비는 0.363 : 0.57 : 1.00 : 6.53 이다[10]. 고 온 열처리 공정에서의 리튬의 휘발로 인한 손실이 발생하 기 때문에 10 wt.%의 리튬을 추가하였다. 용액을 150°C에 서 중탕 가열하며, 100 rpm의 속도로 회전 교반하면서 건 조시켰다. 얻어진 겔 형태의 고체를 알루미나 도가니에 포 집하여 Electric Muffle Furnace(JMF14-4.5, MMK)에서 La(NO3)3·xH2O에 포함된 결정수를 제거하기 위하여 우선 적으로 600°C에서 4시간 동안 열처리한 후, 연속공정으로 1050°C에서 20시간 동안 공기 중에서 하소하여 흰색 분말 을 얻었다. 전체 열처리 공정 간 승온 속도는 2°C/min로 동일하였다. 이후 응집된 분말은 Mortar Milling 하였다.
- 2.2 Solid-State Reaction 공정을 통한 분말 합성
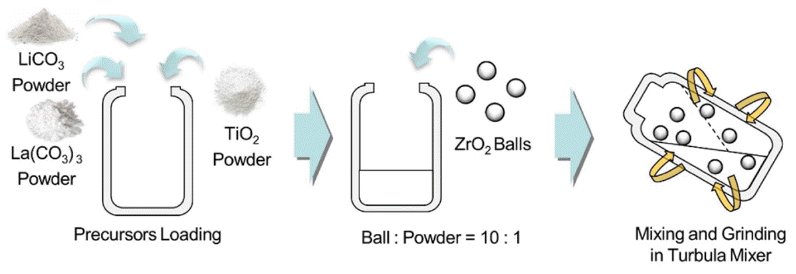
- 분말의 비교를 위하여 다른 합성법인 고체상태 반응법 으로 LLTO 분말을 합성하였다[18]. 전구체로 Li2 CO3 (99.0%, Sigma-Aldrich), La2O3(99.9%, Sigma-Aldrich), TiO2 (99.8%, Sigma-Aldrich)을 사용하였다. 각 전구체 분말들 을 화학양론적 측량에 의해 0.363 : 0.57 : 1.00의 몰비로 용 기 내에 장입한 후, 혼합 및 분쇄를 위해 직경 10mm의 지르코니아(ZrO2) 볼을 용기에 함께 장입하였다. 졸-겔 공 정에서와 마찬가지로 고온 열처리 공정에서의 리튬의 휘 발로 인한 손실이 발생하기 때문에 10 wt.%의 리튬을 추 가하였다. 이 때의 Ball Powder Weight Ratio는 10 : 1 이 었다. 이후, 분말 용기를 turbula mixer(DTB-2, DAEHWA TECH)에서 50 rpm, 6시간의 조건으로 분말을 혼합 및 분 쇄하였다. 공정이 완료된 후 용기에서 볼과 분말을 분리하 였다. 이후 알루미나 도가니를 이용하여 혼합된 전구체 분 말을 1000°C에서 12시간 동안 공기 중에서 하소하여 흰색 분말을 얻었다. 열처리 공정 간 승온 속도는 2°C/min로 동 일하였다. 응집된 분말은 Mortar Milling 하였다.
- 2.3 전구체 및 제조된 분말 특성평가
- 본 연구에서 두 합성법으로 제조한 하소 후 LLTO 분말 상의 결정구조 및 반가폭(FWHM; Full Width at Half Maximum) 분석을 통한 결정크기를 확인하기 위해 X-ray diffraction (XRD; D8 Advance, Bruker AXS)을 사용하였 다. FWHM 분석은 대상 시료의 평균 결정크기를 추측할 수 있는 분석 방법으로 XRD결과에서 가장 많은 상의 peak의 절반의 높이에서의 폭이며, 각 합성법으로 제조한 LLTO 분말의 XRD 결과를 통해 얻은 반가폭을 아래의 Scherrer’s equation에 대입하여 각 분말의 평균 결정크기 를 산출하였다[23].
Dp = average crystallite size (nm)
K = Scherrer constant (0.68-2.08), 0.94 for spherical crystallites with cubic symmetry
β = FWHM (full width at half maximum)
θ = XRD peak position (Bragg angle), one half of 2θ
λ = X-ray wavelength
- 분말의 현상은 scanning electron microscopy(SEM; JSM- 100F, JEOL)을 통하여 확인하였고, 두 합성법으로 제조한 LLTO 분말의 입자 분포의 균일성 및 입자크기를 비교하 였다.
- 추가적인 입도 분석을 위하여 Dynamic Light Scattering (DLS; Zetatrac, Microtrac)을 통하여 분산 용매(Ethanol)에 초음파로 분산시킨 각 LLTO 분말의 입자크기를 측정하여 비교하였다.
2. Experimental
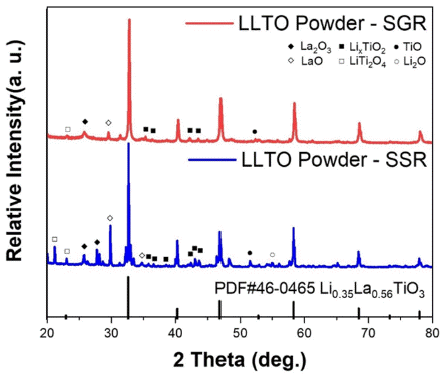
- 본 연구에서 Sol-Gel Reaction(SGR), Solid-State Reaction (SSR) 두 합성 공정을 이용하여 제조한 각 LLTO 분말의 XRD를 통한 결정구조 분석 결과를 Fig. 3에 나타내었다. 이 때, 결정구조를 비교하기 위한 기준 JCPDS Card는 Cubic 구조의 Li0.35La0.56TiO3(PDF#46-0465)와 비교를 수 행하였다. 이는 추가로 장입한 10 wt.% 리튬이 분말 하소 및 성형체 소결의 두 단계의 열처리 공정 중에서의 휘발 로 인하여 손실됨에 따라 최종적으로 Li0.33La0.57TiO3의 화 학량론적 조성이 맞추어지기 때문이다[10,18]. 또한, 최종 목표인 Perovskite LLTO 내부 격자구조의 형성은 성형체 소결 과정에서 이루어 질 것으로 예상하였다. 분석 결과 두 합성법으로 합성한 LLTO 분말의 결정 Peak 모두 Li0.35La0.56TiO3의 JCPDF Peak들의 위치와 일치함을 확인 하였다. SSR 공정으로 합성한 LLTO 분말은 SGR 공정으 로 합성한 LLTO 분말에 비하여 불순물 Peak가 다수 발견 되었다. SGR, SSR 각 XRD 결과에서 발견되는 이러한 불 순물 Peak는 반응이 완료되지 않은 전구 물질들이다. 습 식 혼합 과정인 SGR 공정은 합성 과정에서 전구체들이 고르게 혼합이 되며 반응하는 반면, SSR 공정은 합성 과 정에서 전구체 분말들의 혼합이 그 건식 공정 방식으로 인하여 SGR 공정에 비하여 충분하지 않기 때문에 비교적 단일 상을 형성하기 어려웠다. 하지만, 이러한 불순물 상 의 형성은 추후의 더욱 고온으로 진행되는 소결 공정에서 의 결정화를 통하여 완전히 제거될 것으로 예상하였다.
- Figure 4와 5는 SGR, SSR 두 합성법으로 제조한 LLTO 분말의 하소 및 mortar mill 이후의 100배 배율, 500배 배 율에서의 각 SEM image를 보여준다. 100 배율의 SEM image 비교에서 SGR로 제조한 분말은 평균적으로 수 μm ~ 20 μm의 입자들이 큰 편차없이 고르게 분포가 되어있음 을 확인할 수 있는 반면, SSR로 제조한 분말의 경우 mortar mill을 진행하였음에도 불구하고, 분말의 입자가 작 게는 수 μm 에서부터 크게는 100 μm에 가까운 응집된 입 자가 SGR 분말에 비하여 비교적 불균일하게 분포함을 확 인하였다. 500배 배율의 SEM image 에서도 SGR로 합성 한 분말에서 작은 미세 입자들이 많음을 확인할 수 있었 지만 그 차이는 미미하였다. SEM image 관찰을 통한 입 도 분석은 LLTO 분말이 단일 입자가 아닌, 다수의 입자 들이 응집한 형태이기 때문에 분말 단일 입자의 평균적인 크기 측정하는 데에 있어 한계가 존재한다.
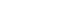
- LLTO 분말의 평균 결정크기를 측정하기 위하여, XRD 데이터를 이용하여 FWHM 값을 얻었다. FWHM는 가장 높은 강도를 보이는 peak 상의 절반의 높이에서의 peak 폭의 크기이며, Scherrer’s equation에 의해 결정크기와 반 비례 관계를 갖는다. Fig. 6은 두 공정으로 합성한 각 LLTO 분말의 XRD 데이터에서 약 32.8도에 위치한 (110) 상 peak의 FWHM을 보여준다. Table 1은 Scherrer’s equation 에 각 FWHM을 대입하여 산출한 평균 결정크기의 값과 그 차이에 관한 결과를 보여준다. SGR 및 SSR로 합성한 LLTO 분말의 평균 결정 크기는 각각 80.18 nm, 117.39 nm로, SGR로 합성한 분말이 SSR로 합성한 분말 에 비하 여 평균 결정 크기가 약 0.68배 작음을 확인하였다. 이 결 과를 통하여, Solid-State Reaction 공정으로 합성한 분말에 비해 Sol-Gel Reaction 공정으로 합성한 분말의 입자가 더 작고, 균일한 입자 분포를 가지며, 평균 결정 크기 또한 작 음을 확인하였다. 하지만 Scherrer’s equation은 일반적으 로 완벽한 구형의 결정을 가정하여 계산한다. 또한, LLTO 분말은 다결정구조의 입자이므로 결정립의 크기는 1차 입 자의 크기보다 작으므로 추가적인 입도 분석이 필요하다.
- Table 2는 SGR, SSR공정으로 합성한 LLTO 분말의 DLS 입도 분석 결과이다. 초음파를 이용하여 분산 용매에 충분히 분산시킨 LLTO 분말은 건식 분석에 비하여 응집 에 의한 불분명한 입도 해석에서 비교적 자유롭다. 이 때, SGR 공정으로 합성한 분말의 평균 입자 크기는 3.23 μm 이며, 이는 5.92 μm인 SSR로 합성한 분말의 입자 크기보다 약 0.55배로 작음을 확인하였다. 이는 Scherrer’s equation을 통하여 계산된 결정크기보다 각각 약 40, 50배 정도의 크 며, 이러한 차이는 LLTO 분말의 입자는 다결정구조로 입 자 내에 다수의 결정립이 존재하기 때문이다. 또한, 열처 리 공정 간 입자들의 일부 소결로 인한 결합이 진행되었기 때문에 입도 분석을 위해 현탁액을 분산하는 과정에서 단 일 입자로 분산되지 않았을 것으로 추정할 수 있다[25-30]. 이러한 결과는 SEM, FWHM 등으로 비교한 각 공정으로 제조한 LLTO 분말의 입자 크기 비교 결과와 유사하며, 다 양한 분석들을 통하여 SGR로 제조한 분말이 더 작은 입 도와 결정크기를 가짐을 최종적으로 확인할 수 있었다.
- 이러한 1차 결정크기 및 2차 입자 크기의 차이는 분말 의 성형, 소결 공정에 영향을 미치며, 최종적으로 LLTO 멤브레인의 성능에도 영향을 미칠 것으로 추정된다. 분말 성형 공정에서 더 얇은 성형체를 제조하기 위하여, 입자 크기가 작은 분말을 사용하는 것이 유리하다. 특히, 멤브 레인의 두께는 이온의 투과 효율에 큰 영향을 미치는 요 인이며 가압성형 뿐만 아니라, green film 형태로 제조할 시에도 입자 크기는 중요한 인자가 된다. 소결 공정에서도 입자 또는 결정 크기가 작을수록 높은 밀도를 갖는 소결 체를 얻기 유리하다. 하지만 입자 크기가 작아질수록 단위 부피 당 입자(Grain) 개수는 이에 반비례하여 증가하게 될 것이며 소결 전에는 SGR로 합성한 LLTO 분말로 이루어 진 그린 펠릿의 입계 비율이 약 1.88배 정도로 많을 것이 다. 또한, 소결 공정을 통하여 입자가 성장하게 된다면 이 러한 차이는 더욱 증가할 것으로 추정된다[24,25]. 소결 체 내의 입자의 평균 크기가 감소함에 따라 입계가 차지 하는 비율이 증가하여 입계저항이 증가하는 사례는 선행 연구들을 통하여 검증되었다[17,31,32]. 이러한 입계 저 항의 증가는 최종적으로 DLE 시스템에서의 리튬 추출 효 율 감소에도 영향을 미칠 것으로 추정된다[10].
3. Results and Discussion
Comparison of particle shapes image of LLTO powder magnified 100 times. (a) sol-gel reaction, (b) solid-state reaction.

Comparison of particle shapes image of LLTO powder magnified 500 times. (a) sol-gel reaction, (b) solid-state reaction.

FWHM analysis of LLTO powder with enlarged (110) peak of XRD. (a) sol-gel reaction, (b) solid state reaction.
Crystal size and ratio calculated for each FWHM in Scherrer's equation
| LLTO Powder - SGR | LLTO Powder - SSR | Ratio (SGR/SSR) | |
|---|---|---|---|
|
|
|||
| Average Crystal Size (nm) | 80.18 | 117.38 | 0.68 |
Particle size and ratio measured by DLS
| LLTO Powder - SGR | LLTO Powder - SSR | Ratio (SGR/SSR) | |
|---|---|---|---|
|
|
|||
| Average Particle Size (μm) | 3.23 | 5.92 | 0.55 |
- 해수에서 리튬을 추출하는 기술은 미래 리튬 공급 및 가 격 문제를 해결하는데 적극 기여할 수 있는 차세대 전략 자원 확보 기술이다. 특히 고체전해질 소재의 멤브레인을 활용한 전기투석 공법을 기반으로 하는 2세대 리튬 추출 기술은 흡/탈착, 전기 분해 등과 같은 1세대 기술에 비해 높은 안정성과 효율을 갖는 우수한 기술로 활발히 연구가 진행 중에 있다. 이 시스템에서의 핵심 소재로 활용되는 LLTO 멤브레인의 성능을 향상 시키기 위하여 총 이온전 도도(σt)를 저해하는 요소 중 하나인 입계 저항을 줄여야 하며, 기계적 안정성을 유지한 채로 얇은 형태의 멤브레인 을 제조할 필요성이 있다. 이를 결정하는 중요한 요소 중 하나는 멤브레인의 모체가 되는 LLTO 분말 입자 및 결정 의 크기이다.
- 본 연구를 통하여 LLTO 분말을 합성하는 데에 널리 이 용되는 두 가지 합성법인 Sol-Gel reaction, Solid-State reaction으로 LLTO 분말을 합성 및 제조하였다. 이후, 두 종류의 분말을 XRD, SEM, FWHM 그리고 DLS 입도 측 정을 통하여 분석하였으며, 그 결과로 SGR로 제조한 분 말은 평균적으로 20 μm 미만의 작고 균일한 입자 분포를 가짐을 확인하였다. 반면 SSR로 제조한 분말은 응집된 최 대 100 μm 미만의 입자들이 불균일하게 분포함을 확인하 였다. FWHM을 이용하여 산출한 결정 크기 비교를 통하 여 SGR로 합성한 분말은 약 80.18 nm, SSR로 합성한 분 말은 약 117.38 nm의 평균 결정 크기를 가지며, SGR로 합 성한 분말이 약 0.68배 작았다. 분산 용매에 분산시킨 분 말의 DLS 입도 크기 측정을 통하여 SGR, SSR 공정으로 합성한 각 분말은 약 3.23 μm, 5.92 μm 의 입자크기를 가 지며 SGR로 합성한 분말이 약 0.55배 작았다.
- 따라서 본 연구 결과를 통하여 LLTO 멤브레인 제조 적 합한 분말 합성법에 대한 수치적 지표를 얻을 수 있었다. SGR로 합성한 미세 LLTO 분말의 경우 Tape Casting 공 법을 활용한 얇은 멤브레인 제조에 유리하며, 이는 멤브레 인의 두께와 이온전도도 간의 반비례 관계가 성립하므로 인하여, 실제 DLE 시스템에 적용 시 리튬 이온 투과도에 상승에 중요한 영향을 미칠 것으로 추정된다. Zhen Li et al.은 50 μm 두께의 매우 얇은 멤브레인 제작에 성공하여 해수의 리튬 농도보다 약 43,000배 높은 농도를 가진 리 튬 농축수 제조를 보고하였다[10]. SSR로 합성한 LLTO 분말은 멤브레인의 소결 공정에서 Grain이 성장함에 따라 비교적 적은 Grain boundary 영역을 형성하는 데에 유리 하여, 이는 결과적으로 LLTO의 총 이온전도도를 감소시 키는 입계 저항의 감소를 기대할 수 있다. 실제 입계 전도 도는 앞선 연구들 통하여 소결 후 입자 사이즈가 1 μm에 서 5 μm로 증가할 경우 약 3.25배 정도 증가함을 알 수 있 다[33]. 실제 DLE 시스템에서는 두께가 얇고, 내부 Grain 의 크기는 큰 멤브레인을 적용할수록 시스템의 효율이 증 가할 것으로 예측된다. 추가적으로, 향후 본 연구 결과를 활용하여 두 합성법으로 제조한 분말의 혼합 비율을 조정 함에 따라 멤브레인 대량 생산, 고성능의 멤브레인 제조 등과 같이 각 용도에 적합한 분말 제조 공정의 최적화가 가능할 것으로 기대한다.
4. Conclusion
-
Acknowledgements
- 본 논문은 한국생산기술연구원 기관주요사업 “4원계 페 로브스카이트 구조의 희토류 멤브레인 신조성 및 합성법 개발을 통한 리튬이온 추출 연계기술 선행연구(KITECH JE-23-0008)”의 지원으로 수행한 연구입니다. 또한, 이 성 과는 정부(과학기술정보통신부)의 재원으로 한국연구재단 의 지원을 받아 수행된 연구입니다(No. ES-22-0015).
Acknowledgement
- 1. P. K. Choubey, M. S. Kim, R. R. Srivastava, J. C. Lee and J. Y. Lee: Miner. Eng., 89 (2016) 119. .Article
- 2. Y. M. Lin, K. C. Klavetter, P. R. Abel, N. C. Davy, J. L. Snider, A. Heller and C. Buddie Mullins: Chem. Commun., 48 (2012) 7268. .ArticlePubMed
- 3. Y. Huang, X. Wu, L. Nie, S. Chen, Z. Sun, Y. He and W. Liu: Solid State Ion., 345 (2020) 115171. .Article
- 4. K. Sasaki, R. Hiraka, H. Takahashi and K. S. Mura: Fusion Eng. Des., 170 (2021) 112500. .Article
- 5. S. Yang, F. Zhang, H. Ding, P. He and H. Zhou: Joule, 2 (2018) 1648. .Article
- 6. A. Siekierka, B. Tomaszewska and M. Bryjak: Desalination, 436 (2018) 8. .Article
- 7. J. F. Song, L. D. Nghiem, X. M. Li and T. He: Water Res. Technol., 3 (2017) 593. .Article
- 8. P. K. Choubey, K. S. Chung, M. S. Kim, J. C. Lee and R. R. Srivastava: Miner. Eng., 110 (2017) 104. .Article
- 9. C. Liu, Y. Li, D. Lin, P. C. Hsu, B. Liu, G. Yan, T. Wu, Y. Cui and S. Chu: Joule, 4 (2020) 1459. .Article
- 10. Z. Li, C. Li, X. Liu, L. Cao, P. Li, R. Wei, X. Li, D. Guo, K.-W. Huang and Z. Lai: Energy Environ. Sci., 14 (2021) 3152. .Article
- 11. Y. Heng, W. Wang, Q. Li, X. Li, M. Dai, C. Yu, Z. Xue, J. Xia, G. Zhou and D. Jiang: J. Electroceram., 47 (2021) 23. .Article
- 12. J. K im, J. O h, J . Y. Kim, Y. G. L ee a nd K . M. K im: JKES, 22 (2019) 87. .
- 13. H. Kawai and J. Kuwano: J. Electrochem. Soc., 141 (1994) L78. .Article
- 14. X. Gao, C. A. J. Fisher, T. Kimura, Y. H. Ikuhara, A. Kuwabara, H. Moriwake, H. Oki, T. Tojigamori, K. Kohama and Y. Ikuhara: J. Mater. Chem. A, 2 (2014) 843. .Article
- 15. Y. Inaguma, C. Liquan, M. Itoh, T. Nakamura, T. Uchida, H. Ikuta and M. Wakihara: Solid State Commun., 86 (1993) 689. .Article
- 16. L. Xu, L. Zhang Y. Hu and L. Luo: Nano Energy, 92 (2022) 106758. .Article
- 17. P. Braun, C. Uhlmann, A. Weber, H. Stormer, D. Gerthsen and E. Ivers-Tiffee: J. of Electroceram., 38 (2017) 157. .Article
- 18. Y. I. Kim, S. C. Park, K. H. Shin, I. Y. Kim, K. A. Lee, S. K. Jung and B. Lee: J. Powder Mater., 30 (2023) 22. .Article
- 19. Z. Jiang, S. Wang, X. Chen, W. Yang, X. Yao, X. Hu, Q. Han and H. Wang: Adv. Mater., 32 (2020) 1906221. .ArticlePubMed
- 20. S. Xia, X. Wu, Z. Zhang, Y. Cui and W. Liu: Chem., 5 (2019) 753. .Article
- 21. Z. Z heng, H. F ang, F . Y ang, Z .-K. L iu a nd Y. Wang: J. Electrochem. Soc., 161 (2014) A473. .Article
- 22. M. Vijayakumar, Y. Inaguma, W. Mashiko, M. P. C. Lopez and C. Bohnke: Chem. Mater., 16 (2004) 2719. .Article
- 23. A. Monshi, M. R. Foroughi and M. R. Monshi: WJNSE., 2 (2012) 154. .Article
- 24. A. R. Symington, M. Molinari, J. A. Dawson, J. M. Statham, J. Purton, P. Canepa and S. C. Parker: J. Mater. Chem. A, 9 (2021) 6487. .Article
- 25. T. Polczyk, W. Zając, M. Ziąbka and K. Świerczek: J. Mater. Sci., 56 (2021) 2435. .Article
- 26. H. Y. Jeong, J. H. Lee and K. F. Hayes: Geochim. Cosmochim. Acta, 72 (2008) 493. .ArticlePubMedPMC
- 27. M. Baumung, F. Schonewald, T. Erichsen, C. A. Volkert and M. Risch: Sustainable Energy Fuels, 3 (2019) 2218. .Article
- 28. H. T. Le, D. T. Ngo, Y. J. Kim, C. N. Park and C. J. Park: Electrochim. Acta, 248 (2017) 232. .Article
- 29. T. Luo, J. J. Kuo, K. J. Griffith, K. Imasato, O. Cojocaru‐ Miredin, M. Wuttig and G. J. Snyder: Adv. Funct. Mater., 31 (2021) 2100258. .Article
- 30. H. Geng, J. Lan, A. Mei, Y. Lin and C. W. Nan: Electrochi. Acta, 56 (2011) 3406. .Article
- 31. R. Li, K. Liao, W. Zhou, X. Li, D. Meng, R. Cai and Z. Shao: J. Membr. Sci., 582 (2019) 194. .Article
- 32. R. Inada, K. Kimura, K. Kusakabe, T. Tojo and Y. Sakurai: Solid State Ionics, 261 (2014) 95. .Article
- 33. C. W. Ban and G. M. Choi: Solid State Ionics, 140 (2001) 285..Article
Figure & Data
References
Citations

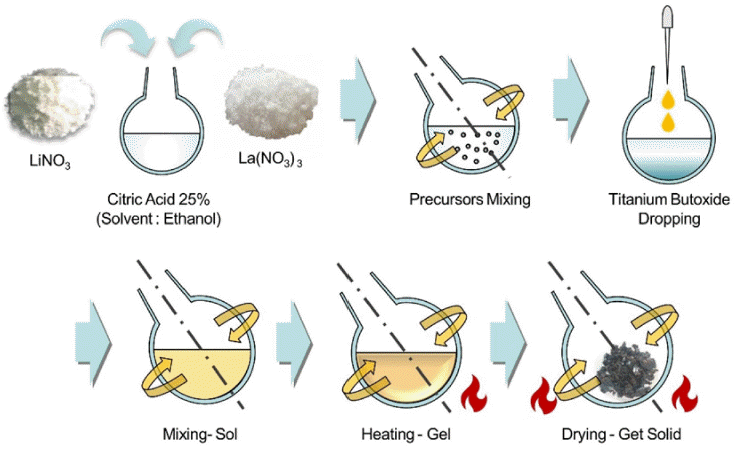



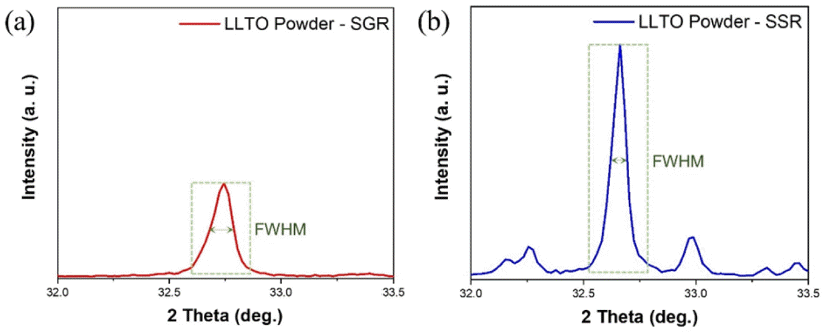
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
| LLTO Powder - SGR | LLTO Powder - SSR | Ratio (SGR/SSR) | |
|---|---|---|---|
|
|
|||
| Average Crystal Size (nm) | 80.18 | 117.38 | 0.68 |
| LLTO Powder - SGR | LLTO Powder - SSR | Ratio (SGR/SSR) | |
|---|---|---|---|
|
|
|||
| Average Particle Size (μm) | 3.23 | 5.92 | 0.55 |
Table 1
Table 2
TOP
 KPMI
KPMI

 Cite this Article
Cite this Article