Articles
- Page Path
- HOME > J Powder Mater > Volume 29(3); 2022 > Article
-
Review Paper
코발트의 제련과 리사이클링 - 손호 상*
- Extractive Metallurgy and Recycling of Cobalt
- Ho-Sang Sohn*
-
Journal of Korean Powder Metallurgy Institute 2022;29(3):252-261.
DOI: https://doi.org/10.4150/KPMI.2022.29.3.252
Published online: May 31, 2022
경북대학교 신소재공학부
School of Materials Science and Engineering, Kyungpook National University, Daegu 41566, Republic of Korea
- * Corresponding Author: Ho-Sang Sohn, TEL: +82-53-950-5560, FAX: +82-53-950-6559, E-mail: sohn@knu.ac.kr
- - 손호상: 교수
• Received: April 25, 2022 • Revised: May 30, 2022 • Accepted: May 30, 2022
© The Korean Powder Metallurgy Institute. All rights reserved.
- 1,649 Views
- 19 Download
- 2 Crossref
Abstract
- Cobalt is a vital metal in the modern society because of its applications in lithium-ion batteries, super alloys, hard metals, and catalysts. Further, cobalt is a representative rare metal and is the 30th most abundant element in the Earth’s crust. This study reviews the current status of cobalt extraction and recycling processes, along with the trends in its production amount and use. Although cobalt occurs in a wide range of minerals, such as oxides and sulfides of copper and nickel ores, the amounts of cobalt in the minerals are too low to be extracted economically. The Democratic Republic of Congo (DRC) leads cobalt mining, and accounts for 68.9 % of the global cobalt reserves (142,000 tons in 2020). Cobalt is mainly extracted from copper–cobalt and nickel–cobalt concentrates and is occasionally extracted directly from the ore itself by hydro-, pyro-, and electro-metallurgical processes. These smelting methods are essential for developing new recycling processes to extract cobalt from secondary resources. Cobalt is mainly recycled from lithium-ion batteries, spent catalysts, and cobalt alloys. The recycling methods for cobalt also depend on the type of secondary cobalt resource. Major recycling methods from secondary resources are applied in pyro- and hydrometallurgical processes.
- 코발트(cobalt, Co)는 화합물로서 B.C. 3000년경부터 유 리의 발색제로 이용되는 등 유리나 도자기의 청색 안료로 사용되어 왔다. 그러나 금속 Co는 1735년 스웨덴의 화학 자인 Georg Brandt가 광산에서 채굴한 광석으로부터 추출 한 Co 성분의 안료를 정제하여 밝은 회색의 금속을 분리 하면서 알려지게 되었으며, 1780년 Bergman에 의해 금속 원소로 확인되었다[1,2]. 코발트(cobalt)라는 명칭은 ‘도깨 비’의 독일어인 ‘kobold’에서 유래된 것으로 알려져 있다. 은(Ag) 광석과 비슷한 Co 광석(As 함유)을 제련하는 과정 에서 유독한 비소 화합물이 생성되면서 은 대신 산화코발 트 분말이 생성되었기 때문이다[3].
- Table 1에는 Co의 물리화학적 성질을 Ni, Cu와 함께 비 교하여 나타내었다. Co의 지각 중 원소 존재도는 30위(25 ppm)로 Ni의 23위(84 ppm), Cu의 26위(60 ppm)[4]와 비슷 하며, 서로 이웃한 원소이지만, Co와 Ni은 융점이 각각 1,495°C, 1,453°C로 구리의 1,085°C 보다 높은 고융점 금 속이다. 따라서 Co는 제트엔진이나 가스터빈용의 내열강 이나 슈퍼알로이(superalloy), 고속도강 등의 특수강 등에 사용되고 있다. 특히 Co는 공구나 금형 등에 사용되는 초 경합금에서 탄화텅스텐(WC)의 바인더 금속으로 사용되고 있다[5]. 또 Co의 강자성을 이용하여 영구자석이나 자기 테이프 등의 자성재료로도 사용되고 있으며, 촉매, Ni-Cd 건전지의 전극 재료, 전자재료, 안료, 유리 첨가제 등으로 사용되고 있다. 그리고 Co는 Ni과 함께 Li 이온 배터리 (LiBs, lithium ion battries)의 대표적인 양극 재료이다[6].
- 이와 같이 Co는 현대 사회에 필수적인 금속원소이지만, 지역적 편재가 심한 금속이다. 특히 LiBs 의 필수 양극 재 료인 Co는 전기자동차의 보급이 활성화되면서 수요량의 증가에 따라 향후 공급 부족 사태가 예상되는 핵심 금속 이다. 따라서 지구환경 보호는 물론 Co의 안정적인 수급 을 위해서도 필히 리사이클링 되어야 하는 재료이다. 한편 Co는 광물학적 특성상 Ni, Cu와 동일한 광물에서 산출되 므로 광석 종류에 따라 여러 가지 제련법으로 금속 Co를 추출하고 있다. 특히 Co 2차 자원에서 Co를 비롯한 유가 금속을 추출하는 리사이클링에서도 유사한 공정으로 처리 하고 있다. 따라서 본 논문에서는 Co의 새로운 리사이클 링 기술을 개발하기 위한 기초 조사로 Co의 제련 기술과 리사이클링 기술에 대해 고찰하였다.
1. 서 론
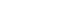
- Fig. 1에는 1900년부터 Co의 전 세계 생산량을 변화를 나타내었다[7]. Co는 1930년대부터 본격적으로 사용되기 시작하였으며, 1950년대에 들어서 생산량이 꾸준히 증가 하기 시작하였다. 2000년대에는 중국의 철강특수는 물론 휴대용 기기의 전원으로 사용되는 LiBs 양극재의 주원료 로 사용되면서 Co 생산량이 비약적으로 증가하였다.
- Fig. 2에는 2020년 기준의 국가별 Co 매장량과 광산 생 산량을 나타내었다[8]. Co 자원의 전 세계 매장량은 700 만 톤 이상인 것으로 추정되고 있지만, 콩고공화국(Democratic Republic of the Congo, DRC)이 전체 매장량의 약 46%, 뒤이어 호주에 약 18%가 매장되어 있다. 그리고 나 머지는 브라질, 러시아, 뉴칼레도니아 등의 일부 한정된 국 가에만 매장되어 있다. 특히 DRC의 광산 생산량이 전 세 계 생산량의 약 69%를 차지할 정도로 편재가 심한 금속이 다. 또 Co의 대부분은 Cu와 Ni 정광의 부산물로 생산되고 있으므로 Co 생산량은 Cu와 Ni 생산량에 따라 좌우된다.
- Fig. 3에는 2021년 기준 Co의 주요 용도를 나타내었다 [9]. 전 세계 Co 생산량의 약 52%는 LiBs의 양극재 원료 로 사용되고 있으며, 약 17%는 슈퍼알로이에, 약 14%는 촉매 등 화학제품에 사용되고 있다.다. 그 외에도 Co는 내 열강이나 고속도강 등의 특수강, 초경공구강 등의 합금원 소 및 자성재료 등의 용도로 사용되고 있다. 특히 1990년 대 중반까지 2차 전지용의 Co 수요는 전체 Co 수요량의 약 1%에 불과했으나, 2021년에는 70,000톤 이상의 Co가 필요하게 되었다. 따라서 Co는 LiBs 등에서의 리사이클링 이 중요하며, 그 외에도 Co 합금, 초경공구, 폐촉매 등에 서 리사이클링하고 있다.
2. 코발트의 생산량과 용도
- 3.1 코발트 자원과 제련 개요
- Table 2에는 Co 함유 광물과 조성, 산지 등을 나타내었 다[10]. 특히 아프리카 잠비아에서 DRC에 걸쳐있는 구리 광산 지역인 Copper Belt의 Cu 광석 중 Co 함유량이 높 은 것을 알 수 있다. 이 지역의 추정 매장량은 약 7억 400 만 톤에 이르며, Co의 주요 공급원으로 전 세계 Co 생산 량의 약 60%를 차지한다. 나머지 약 40%는 Ni 제련 부산 물로 회수된다. Ni 황화광 중의 Co 품위는 매우 낮으나 부 유선광 등으로 10%까지 Co를 농축할 수 있어서 Ni 제련 에서도 경제성있게 Co를 회수하고 있다.
- Fig. 4에는 Co 광석 종류에 따른 제련법과 중간 생성물 및 Co 농도, 응용분야를 종합하여 나타내었다[11]. 대부분 의 Co는 Cu-Co광과 Ni-Co광에서 Cu, Ni 제련의 부산물 로부터 만들고 있다. 따라서 Co 제련은 Cu나 Ni 제련공정 에 기초한 것이다. Co 비화광은 모로코에서만 소량 생산 되고 있다.
- 3.2 구리 광석 중 코발트 회수
- Fig. 5에는 Copper Belt에서 산출되는 구리 광석으로부 터 Co를 회수하는 공정도를 나타내었다[12]. Cu 산화광 (heterogenite)은 전처리한 후 곧바로 황산으로 침출하여 Cu와 Co를 용출시킨다. 다만 산화광을 황산으로 침출할 때, Co3+는 용액 중에서 불안정하므로 Co2+로 환원시켜야 한다. 따라서 SO2(g, 10%) 가스를 버블링하면서 다음식과 같이 침출한다.
- Cu광석(malachite) 중의 Cu도 다음식과 같이 용해된다.
- 이어서 침출액을 여과하여 잔사를 제거하고 여액 중의 Co2+와 Cu2+는 용매추출로 분리하며, Cu는 전해채취하여 전기동으로 회수한다. Co는 Cu를 전해채취한 후의 전해 액이나 Co 수용액에 중화제로 MgO를 첨가하여 pH를 7.8~8.5 수준으로 중화시켜 Co 수산화물인 Co(OH)2로 석 출시켜 회수한다. Co(OH)2는 황산용액에 쉽게 용해되므로 재침출하고 전해채취하여 금속 Co를 얻는다.
- Fig. 6에는 Cu-Co 황화광으로부터 고순도 Co를 회수하 는 공정도[13]를 재구성하여 나타내었다. 부유선광에 의해 품위를 높인 정광(Cu 45%, Co 1~3%)을 유동 배소로에서 황산화 배소하여 산화광과 함께 탈동 전해미액으로 침출 한다. 침출액을 고액분리한 후, 여액을 용매추출하여 Cu 를 제거하고, 추출 후액(raffinate) 중의 불순물(Al, Cu, Fe, Mn, Zn 등)은 중화, 용매추출 등으로 제거한다. 불순물이 제거된 용액에 CaO를 첨가하여 pH를 8.8까지 높이면 Co(OH)2가 침전된다. Co(OH)2 침전물을 Co 전해미액으로 리펄프하여 불용성 양극을 이용한 전해채취로 Co를 음극 상에 석출시키며, 얻어진 Co의 순도는 99.7% 정도이다. 용매추출에서 분리한 Cu 용액에서 Cu를 전해채취하여 전 기동을 생산하며, 전해미액은 침출공정으로 되돌린다. 황 화광을 산화배소나 황산화 배소한 후 황산으로 침출하여 산화광과 동일하게 Co 수산화물을 얻기도 한다. 또 황화 광을 자용로(flash furnace)[14]에서 건식처리하여 조동 (blister Cu)으로 만들고, 전해정제하여 전기동을 회수한다. 이 과정에서 Co는 자용로 슬래그에 분배되므로, 이 슬래 그를 전기로에서 환원하여 Cu-Fe-Co 합금으로 제조하여 회수하기도 한다.
- 3.3 전 광석 침출법(Whole Ore Leaching, WOL)
- DRC의 KCC(Kamoto Copper Company, DRC) Luile 제 련소의 WOL법은 산화구리 광석 중의 Cu를 공기+황산으 로 산화 침출시키고, 이어서 환원제를 첨가하여 Co를 2가 로 환원하여 침전 잔사를 재용해하는 환원 황산 침출법이 다. 정광에서의 Co 추출률은 85%까지 향상되었지만, WOL법에서는 환원제, 황산, 전력 등의 소비량이 증대하 는 것으로 알려져 있다[10]. WOL법에서는 Cu와 Co의 침 출과 동시에 Fe도 2가로 환원되어 침출액 중에서 황산이 재생되며, 반응식은 다음과 같다.
- Fig. 7에는 Co, Cu, Ni, Fe의 Eh-pH도를 나타내었다[10]. Cu의 추출율을 높이기 위한 공기산화에서 산화-환원전위 가 1.8 V 이상이 되면 그림에서와 같이 Co는 3가로 되어 수산화물로 침전된다. 일반적으로 Co3+는 황산에 잘 용해 되지 않으며, Co3+로 용출되어도 산화환원 전위가 높으면 Co3+는 Co(OH)3로 침전된다. 따라서 침출액 중에 Co2+로 존재하기 위해서는 전위를 낮추어야 한다. Co를 2가로 환 원하기 위해 환원제로 SO2, SMBS(sodium metabisulfite), Cu 분말, Fe 분말 등을 첨가하면 Co3+, Fe3+가 환원됨과 동 시에 황산이 재생된다. 다만 이 과정에서 Cu가 용액 중에 Cu2+ 상태로 존재하도록 Cu/Cu2+의 평형전위인 0.35 V 이 하가 되지 않도록 0.5 V 정도를 유지하여야 한다.
- 3.4 니켈 광석 중 코발트 회수
- Fig. 8에는 Ni 광석으로부터 Co를 회수하는 공정도를 나타내었다[12]. Ni 광석에는 산화광인 라테라이트광과 황 화광이 있으며, 처리방법도 매우 다양하다. 일반적으로 Ni 황화광의 건식제련에서는 Ni 매트(matte)를, 습식제련에서 는 복합 황화물을 경유하여 Co를 회수한다. Ni 산화광은 습식제련으로 Co를 회수한다. Co 비화광도 배소, 산침출, 용매추출, 전해채취 등 유사한 공정으로 처리하여 Co를 회수한다.
- Ni 황화광은 정광 중 Fe, Ni의 산소, 유황과의 친화력 차 이를 이용하여 황화물인 매트로 농축하여 처리한다. 매트 는 PS 전로에서 산화정련하여 Co를 비롯한 Ni, Cu, 귀금 속 등이 농축된 정제 매트를 만들어 Ni 회수공정으로 보 내어 처리한다.
- Ni 산화광은 주로 페로니켈 원료로 사용하지만, Co를 회수하기 위해서는 습식으로 처리하고 있다. 특히 고온 고 압 침출법(HPAL, high pressure acid leach)에서는 Co와 Ni을 200°C 이상 및 3MPa 이상의 고온, 고압에서 침출시 키며, 동시에 불순물인 Fe, Al의 산화물은 침전된다. Co와 Ni의 침출반응은 다음과 같다[6].
- 침출액을 용매추출하여 Co와 Ni 용액으로 분리하여 H2(g)로 환원하면 각각의 분말이 얻어진다.
- 한편 Co+Ni 수용액 중의 Ni을 가압수소로 우선 환원한 후의 여액을 H2S(g)로 처리하면 Co 및 Ni을 각각 20% 함 유하는 황화물 혼합 케이크가 얻어진다. Co+Ni 함유 혼합 케이크를 공기와 암모니아로 침출한 여액에 별도로 암모 니아를 첨가하여 Co와 Ni의 복합 헥사민염(hexamine salt) 을 침전시킨다. 침전물을 수침출하여 Ni을 제거한 여액을 가압수소 환원으로 순도 99.8%의 금속 Co 분말을 회수할 수 있으며, Sherritt Gordon법이라 한다. Co의 수소환원 반 응은 아래와 같으며, 금속상의 Co는 Co seed에 석출된다[6].
- Ni의 전해정제 부산물에서도 Co를 회수한다. 우선 Ni 황화광이나 산화광에서 얻은 고품위 Ni 매트를 산화배소 하고 Cu를 제거한 전해 미액으로 Cu를 침출하여 제거한 잔사를 얻는다. 이 잔사를 전기로에서 용융환원하면 Cu와 Co가 함유된 조 Ni(Ni 76%)이 얻어진다. 조 Ni을 전해정 제하여 고순도 Ni을 얻는 과정에서 발생하는 전해미액의 정액공정에서 부산물로 나오는 탈철 케이크에 환원제인 SO2 가스를 취입하여 Co를 2가로 환원하면서 묽은황산으 로 침출하면 Ni, Co 및 Cu가 우선적으로 용해한다. 침출액 중의 Cu를 Ni분말로 치환침전하여 제거한 후, Co는 Cl2 가스와 Na2CO3로 pH를 약 2.2로 맞추어 Co(OH)3로 선택 침전시키면 Co 50%, Ni 1%의 수산화물 케이크를 얻을 수 있다. 이것을 하소·환원하여 얻어지는 Co를 양극으로 하 고, 음극으로는 스테인리스판을 사용하여 전해정제하면 99.6%의 전기 Co가 만들어진다.
- 3.5 코발트 침출액의 정제
- Co 침출액 중에는 Cu, Fe, Mn, Al, Mg, Ca, U, Zn, Ni 등이 함유되어 있다. 이러한 불순물은 침전분리나 용매추 출에 의해 제거한다. Fig. 9에는 침전분리에 의해 용액을 정제하는 공정도를 나타내었다[10]. 다단계에 걸쳐서 정제 한 Co 용액을 중화할때, 1단계에서는 석고 생성을 방지하기 위해 MgO를 사용하며, 약 40%Co의 석출물이 생성된다.
- 한편 용매추출에서는 1회만으로는 높은 효율로 분리할 수 없으므로 침전분리 정제나 이온 교환법과 조합하여 Co 용액을 정제한다. 또 Ni 제련의 부산물인 Ni과 Co의 혼합 황화물을 원료로 하여 침출한 후, 용매추출법으로 양자를 분리하는 프로세스도 실용화되어 있다.
3. 코발트 제련
Fig. 4

Most important current cobalt primary production routes, intermediate products, cobalt content and applications [11].

- LiBs나 NiMH(nickel metal hydride) 배터리, 석유화학 촉매 등에도 Co가 사용되고 있으므로 이러한 것의 리사이 클링에 대해 많은 연구가 이루어지고 있다. 특히 Co 생산 량의 약 52%가 배터리에 사용되고 있으므로 필히 리사이 클링되어야 한다. 또 Co가 함유된 Co-Ni, Co-Ni-Re 등의 특수강이 있으며, Co 함유량이 높은 것은 잘 리사이클링 되고 있으나, 함유량이 낮은 것은 탄소강 스크랩과 구분하 기 곤란하여 정확한 리사이클링 현황을 파악하기 곤란한 실정이다. 그외에도 촉매재료로 사용된 Co도 Ni, Mo, V 등과 함께 리사이클링하여 회수하고 있다.
- 4.1 Li 이온 배터리의 리사이클링
- Fig. 10에는 LiBs의 일반적인 리사이클링 공정도를 종합하 여 나타내었다. LiBs는 LCO(LiCoO2), NCM(LiNiCoMnO2), NCA(LiNiCoAlO2) 등 양극재 중에 Co를 함유한 것들이 많으며, 순환경제를 위해서는 Ni, Co 등의 유가금속은 필 히 회수되어야 한다. 사용 후 LiBs의 리사이클링은 물리 적인 처리와 화학적인 처리로 구분할 수 있다. 물리적인 처리에는 배터리의 해체와 구성물의 분리이며, 화학적인 처리에는 습식처리의 침출, 석출, 정제 및 건식처리 등을 의미한다.
- 주요 리사이클링 대상에는 전해질(electrolyte), anode, cathode 등과 플라스틱 및 금속성 케이스류 등이 있으나, 일반적으로 양극재 중의 유가금속을 회수하고자 많은 연 구들이 수행되고 있다. LiBs의 리사이클링에서는 전처리 공정에서 방전시키고, 재활용률을 높이기 위해 해체하여 물리적으로 분류하는 공정을 거친다[16]. 따라서 이러한 전처리 공정의 효율을 높여서 비용을 절감하는 것이 필요 하다. 해체와 방전 비용을 절감할 수 있는 효율적인 방법 으로 350~500°C 정도에서 열처리하는 방법이 유력하게 제시되고 있다. 열처리하면 전해질은 증발시키고, 유기물 은 열분해시킬 수 있다[17,18]. 다른 방법으로는 액체질 소를 이용한 냉각에 의해 안정화시키는 방법도 실용화되 어 있다.
- 물리적으로 분류하여 회수한 양극재는 다시 파분쇄와 분류 공정을 거쳐서 Al 박판과 활성물질로 분리하고, 양 극 활성물질은 파분쇄 등의 기계적 처리를 거쳐 분류한 후에 습식, 건식+습식, 건식 등의 공정을 거친다. 한편 해 체, 분류 등의 공정을 생략하고 곧바로 건식으로 처리하기 도 한다[19].
- 습식처리에서는 양극재를 산침출 등으로 용해하여 용매 추출 등의 정제방법으로 Li, Co, Ni, Mn 등을 분리한다. 건식법에서는 전처리 여부와 관계없이 고온의 노에서 환 원시켜 Co 등의 유가금속을 합금상으로 회수하며, 필요에 따라 합금상을 다시 산침출-용매추출 등의 방법으로 Co를 분리하여 회수하고 있다.
- 4.2 폐촉매의 리사이클링
- 귀금속 함유량이 많은 촉매는 Umicore 등의 2차 정련 회사에서 처리하지만, Ni과 Co가 많은 Ni-Co 촉매는 Sudbury(Xstrata)와 Kokkola(OMG) 등의 Ni 제련소에서 처리하는 경우가 많다. Fig. 11에는 폐촉매를 습식으로 처 리하는 공정을 분류하여 나타내었다[20]. 수소화 탈황 (hydrodesulfurization, HDS) 폐촉매의 습식 처리에는 다양 한 방법들이 알려져 있다. 우선 촉매 전체를 용해하는 방 법과 유가금속만 선택적으로 용해하는 방법이 있다. 그리 고 촉매 전체를 용해하는 방법에는 배소-침출법과 직접 침 출법이 있다. 유가금속만 선택적으로 용해하는 방법에도 배소-침출법과 직접 침출법으로 구분할 수 있다. 침출 용 매로는 묽은 황산+과산화수소, 진한 황산, 진한 염산 등을 사용하고 있다. 직접 침출에서는 고압침출, 고온 침출 등 이 알려져 있다.
- 건식법에는 직접법과 열처리 후 정련하는 두 가지 방법 이 알려져 있으며, Fig. 12에는 배소 후 정련하는 공정을 나타내었다[20]. 직접법은 전기로에서 폐촉매를 용융환원 하는 것으로 코크스를 환원제로 사용한다. 그리고 플럭스 로 생석회나 석회석을 첨가하며, 유가금속을 포집하기 위 해 철 스크랩 등을 첨가하기도 한다. 폐촉매 중의 Co는 환 원되어 Ni 등과 함께 포집 금속(collector metal)의 합금상 으로 회수된다. 합금상은 습식으로 처리하여 금속별로 분 리하고 있다.
- 4.3 합금 스크랩의 리사이클링
- Co가 함유된 합금 스크랩에는 주조 공정이나 기계 가공 공정, 그리고 제품의 수명이 다하여 발생한 것(노폐 스크 랩) 등이 있다. 이러한 합금 스크랩은 Ni-Co 제련소나 2차 자원 전문 제련소에서 처리하고 있다. 특히 자가 발생 합 금 스크랩 중에서 조성이 관리되고 별도의 유해물질이 함 유되지 않은 것은 별도의 처리 없이 재용해하여 곧바로 사용할 수 있다. 그러나 기계 가공 중에 발생한 터닝 (turning) 스크랩 등은 비표면적이 커서 진공용해나 아크로 용해 및 유도 용해과정에서 약 20%까지 산화 손실이 발 생한다. 그리고 이러한 스크랩은 압축하여 소모형 전극으 로 만들기가 곤란하여 비소모형 수냉 전극식 ESR(electro slag remelting)법으로 용해하기도 하였다[21].
- 한편 Fig. 13에는 Xstrata 제련소의 황화광 처리 공정에 서 여러 가지 형태의 Co 2차 자원을 처리하는 공정도를 나타내었다[22]. Co 2차 자원에는 Co-Ni 합금은 물론 폐 촉매, Li이온 배터리 등도 함께 처리하여 Co, Ni 등을 회 수하고 있다.
- 재용해할 수 없는 탄화물 스크랩 등은 Fig. 14와 같이 복 잡한 과정을 거쳐서 리사이클링하고 있다. 탄화물 스크랩 을 Zn와 함께 용융하면 Co는 용융 Zn 중으로 용해되어 들 어가며, 진공증류하여 Zn를 제거하면 Co는 스펀지상으로 남아 쉽게 파분쇄할 수 있다. 파분쇄한 것을 체질하여 Co 분말과 W, Ta 등의 탄화물을 분리하여 회수한다[5,23].
- 한편 Co 합금 스크랩을 습식으로 처리하기도 하며[24], Fig. 15에 Ni-Co와 Ni-Co-Re 합금의 간단한 습식처리 공 정도를 나타내었다[23]. 다만 습식처리는 Ni과 Co를 분리, 회수하거나 제련소에서 손실된 유가금속(Ta, W, Re 등)을 회수하기 위한 소규모 작업으로 이루어진다. 특히 합금 성 분의 종류가 많으면 처리 공정은 더욱더 복잡해진다. 일부 에서는 Co 합금 스크랩을 전기화학적으로 용해하여 유가 금속을 회수하기도 한다[25].
4. 코발트의 리사이클링
Fig. 11

Metallurgical processes for spent HDS catalysts by bulk leaching (a) and selective leaching (b) [20].

Fig. 15

Recovery of cobalt and valuable by-products (Ni, Ta, W, Re) using hydrometallurgical techniques [23].

- Co는 연간 생산량이 14만 톤에 미치지 못하는 희소금속 이지만, Ni과 함께 Li이온 배터리의 양극재, 슈퍼알로이, 석유화학용 촉매, 초경합금의 바인더 금속 등으로 사용되 는 등 현대 산업의 필수 금속 원소가 되었다. 이러한 Co 는 Cu-Co, Ni-Co의 황화광, 산화광 등으로 산출되고 있다. 따라서 Co의 금속이나 화합물은 Cu나 Ni 제련의 부산물 로 생산되지만, 광석 종류에 따라 습식제련법, 건식제련법 및 복합 제련법 등 다양한 방법으로 만들어진다. Cu 제련 공정에서 산화광은 습식처리, 황화광은 건식정련 후 슬래 그를 습식처리하여 Co를 회수한다. Ni 황화광의 건식제련 에서는 Ni 매트를, 습식제련에서는 복합 황화물을 경유하 여 침출, 용매추출, 수소환원 등의 방법으로 Co를 회수하 고 있다. Co의 2차 자원에는 폐Li 이온 배터리의 양극재, 사용 후 석유화학 촉매, Co계 합금 등이 있다. 따라서 Co 의 리사이클링도 2차 자원의 종류에 따라 습식, 건식 및 건식+습식 등 다양한 방법을 적용하고 있다. 폐Li 이온 배 터리의 습식 리사이클링에서는 배터리 해체, 방전, 파분쇄 및 분리 등의 전처리를 거처 회수한 양극재를 침출, 용매 추출 등의 복잡한 공정으로 Co를 회수하고 있다. 건식법 에서는 용융환원으로 합금을 만들지만, 순수한 Co를 얻기 위해서는 습식정제법을 적용하고 있다. 폐촉매나 Co 합금 에서의 Co 추출 및 회수도 유사한 방법을 적용하고 있다. 향후 Co 자원 확보를 위해 다양한 지상자원에서 Co를 보 다 효율적으로 회수할 수 있는 기술 개발이 필요할 것이다.
5. 종 합
- 1. D. Lindsay and W. Kerr: Nature Chemistry, 3 (2021) 494..ArticlePubMed
- 2. M. E. Weeks: J. Chem. Educ., 9 (1932) 22..Article
- 3. O. Pourret and M. P. Faucon: Cobalt, Encyclopedia of Geochemistry, W. White (Ed.), Springer International Publishing, Switzerland, (2016) 1..
- 4. H.-S. Sohn: Recycling of Common Metals, KNU Press, Daegu, Korea, (2020) 17..
- 5. H.-S. Sohn: J. Powder Mater., 28 (2021) 342..
- 6. H.-S. Sohn: Resource Recycling, 30 (2021) 3..Article
- 7. USGS, https://www.usgs.gov/centers/nmic/cobalt-statistics-and-information..
- 8. K. B. Shedd: Cobalt, U.S. Geological Survey, Mineral Commodity Summaries 2021, USGS, Reston, Virginia (2021) 50..
- 9. https://www.cruxinvestor.com/articles/the-ultimate-guideto-the-cobalt-market-2021-2030f. (2021.12.30.).
- 10. M. Akahori: Kinzoku-shigen repoto (JOGMEC), 49 (2019) 1..
- 11. T. Schmidt, M. Buchert and L. Schebek: Resour. Conserv. Recycl., 112 (2016) 107..Article
- 12. Q. Dehaine, L. T. Tijsseling, H. J. Glass, T. Tormanen and A. R. Butcher: Miner. Eng., 160 (2021) 106656..Article
- 13. Frank K. Crundwell, M. Moats, V. Ramachandran, T. Tobinson and W. G. Davenport: Extractive Metallurgy of Nickel, Cobalt and Platinum-Group Metals, Elsevier, UK (2011) 386..
- 14. H.-S. Sohn: Recycling of Common Metals, KNU Press, Daegu, Korea, (2020) 188..
- 15. T. Usmani, C. Santos, N. Dempers, A. M. Ameen, and C. O'Brien: KCC 2017 NI 43-101 Technical Report, (2017) 82..
- 16. R. Laucournet, G. Garin, E. Senechal and B. Yazicioglu,: Li-ion Batterires Recycling, ELIBAMA, (2014) 1..
- 17. T. Georgi-Maschler, B. Friedrich, R. Weyhe, H. Heegn, and M. Rutz: J. Power Sources, 207 (2012) 173..Article
- 18. S. H. Joo, S. M. Shin, D. J. Shin and J. P. Wang: J. Eng. Manuf., 229 (2015) 212..Article
- 19. B. Friedrich, M. Vest, H. Wang, and R. Weyhe: Processing of Li-based Electric Vehicle Batteries for Maximized Recycling Efficiency, Porc. 16th ICBR, Venice, Italy (2011) 1..
- 20. L. Zeng and C. Y. Cheng: Hydrometallurgy, 98 (2009) 1..Article
- 21. V. V. S. Prasad, A. S. Rao, U. Prakash, V. R. Rao, P. K. Rao and K. M. Gupt: ISIJ Inter., 36 (1996) 1459..Article
- 22. C. M. Díaz, C. Levac, P. J. Mackey, S. W. Marcuson, R. Schonewille and N. J. Themelis: The Canadian Metallurgical & Materials Landscape 1960 to 2011, P. Mackey and N. S. J. Kapusta (Ed.), MET SOC, Canada (2011) 342..
- 23. C. J. Ferron: Ni-Co 2013, T. Battle, M. Moats, V. Cocalia, H. Oosterhof, S. Alam, A. Allanore, R. Jones, N. Stubina, C. Anderson and S. Wang(Ed.), Springer, Texas (2013) 53..
- 24. R. R. Srivastava, M.S Kim, J. C Lee, M. K. Jha, and B. S Kim: J Mater. Sci., 49 (2014) 4671..Article
- 25. H. A. Petersen, T. H. T. Myren, S. J. O’Sullivan and O. R. Luca: Mater. Adv., 2 (2021) 1113..Article
Figure & Data
References
Citations
Citations to this article as recorded by 

- Reduction Behavior of Black Mass Recovered from NCM-based Spent Lithium-ion Batteries by CO Gas
Sang-Yeop Lee, Jae-Ho Hwang, So-Yeong Lee, Ho-Sang Sohn
Korean Journal of Metals and Materials.2025; 63(10): 820. CrossRef - Recovering cobalt from cobalt oxide ore using suspension roasting and magnetic separation technique
Xinlei Wei, Yongsheng Sun, Yanjun Li, Peng Gao
Journal of Materials Research and Technology.2023; 27: 3005. CrossRef
 ePub Link
ePub Link-
 Cite this Article
Cite this Article
- Cite this Article
-
- Close
- Download Citation
- Close
- Figure
- Related articles
Extractive Metallurgy and Recycling of Cobalt














Fig. 1
Change of world mine and refinery productions of cobalt (Source; USGS) [7].
Fig. 2
World cobalt reserves and mine production based on cobalt content (Source: USGS) [8].
Fig. 3
The breakdown of cobalt usage in different applications around the world [9].
Fig. 4
Most important current cobalt primary production routes, intermediate products, cobalt content and applications [11].
Fig. 5
Cobalt extraction process from Cu-Co deposit [12].
Fig. 6
Production of high-purity cobalt from cobalt–copper sulfide concentrate [13].
Fig. 7
E-pH diagram of Co, Cu, Ni, and Fe [10].
Fig. 8
Cobalt extraction process from Ni-Co deposit [12].
Fig. 9
Purification of cobalt solution by precipitation [10].
Fig. 10
General flow sheet in recycling of LIBs.
Fig. 11
Metallurgical processes for spent HDS catalysts by bulk leaching (a) and selective leaching (b) [20].
Fig. 12
Smelting routes for spent catalysts [20].
Fig. 13
Simplified flowsheet of Xstrata Nickel’s Sudbury Smelter [22].
Fig. 14
Simplified process to recycle cemented carbides [23].
Fig. 15
Recovery of cobalt and valuable by-products (Ni, Ta, W, Re) using hydrometallurgical techniques [23].
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Fig. 7
Fig. 8
Fig. 9
Fig. 10
Fig. 11
Fig. 12
Fig. 13
Fig. 14
Fig. 15
Extractive Metallurgy and Recycling of Cobalt
Table 1
Comparison of physico-chemical properties of Co, Ni, and Cu
Table 2
Major cobalt minerals and cobalt contents [10]
Table 1
Table 2
TOP
 KPMI
KPMI