Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 27(6); 2020 > Article
-
Article
미세 기공의 한정된 공간에 의한 게스트 분자의 광학 특성 변화 고찰 - 박수현, 김주영*
- Photophysical Properties of Guest Molecules Confined in Nanopores
- Suhyeon Park, Juyeong Kim*
-
Journal of Korean Powder Metallurgy Institute 2020;27(6):477-483.
DOI: https://doi.org/10.4150/KPMI.2020.27.6.477
Published online: November 30, 2020
경상대학교 화학과
Department of Chemistry and Research Institute of Natural Sciences, Gyeongsang National University, Jinju 52828, Republic of Korea
- *Corresponding Author: Juyeong Kim, TEL: +82-55-772-1497, FAX: +82-55-772-1489 , E-mail: chris@gnu.ac.kr
- - 박수현: 학생, 김주영: 교수
• Received: December 4, 2020 • Revised: December 16, 2020 • Accepted: December 16, 2020
© The Korean Powder Metallurgy Institute. All rights reserved.
- 715 Views
- 1 Download
Abstract
- Metal-organic frameworks (MOFs) are of significant interest because of their high porosity, which facilitates their utilization in gas storage and catalysis. To enhance their current properties in these applications, it is necessary to elucidate the interactions between molecules in a confined environment that differ from those in bulk conditions. Herein, we study the confined molecular interaction by investigating the solvent-dependent photophysical properties of two different-sized molecules inside MOF-5. Ruthenium tris-bipyridine (Rubpy) and coumarin 153 (C153) are encapsulated in MOF-5. Rubpy with MOF-5 (Rubpy@MOF) is prepared by building MOF-5 around it, resulting in limited space for solvent molecules in the pores. The smaller C153 is encapsulated in the preformed MOF-5 (C153@MOF) by simply soaking the MOF in a concentrated C153 solution. C153@MOF permits more space for solvent molecules in the pore. Their characteristic absorption and emission spectra are examined to elucidate the confined molecular interactions. Rubpy@MOF and C153@MOF exhibit different spectral shifts compared to the guest molecules under bulk conditions. This discrepancy is attributed to the different micro-environments inside the pores, derived from confined host-guest interactions in the interplay of solvent molecules.
- 제올라이트부터 금속-유기 골격체(MOF)에 이르는 다공 성 분말은 다방면에서 응용 가능성이 높아 활발한 연구가 진행되고 있다. 특히, MOF는 규칙적인 미세 기공으로 이 루어진 유·무기 복합소재로서 다른 다공성 분말에 비하여 비표면적이 높고 열적 안정성이 우수하여 많은 주목을 받 고 있다[1]. MOF의 규칙적인 다공성 구조는 삼차원적으 로 유기 리간드와 금속 클러스터가 결합하여 만들어진다. 유기 리간드는 그 종류가 무수하여 이를 활용하면 구조적 다양성에 제한이 있는 다른 다공성 분말과 비교하여 다양 한 크기, 극성 및 강도의 미세 기공으로 구성된 MOF 제 조가 가능하다[2-5]. 이와 같은 손쉬운 구조 변환 가능성 을 활용해 다공성 분말의 핵심 응용 분야인 수소, 이산화 탄소, 메탄과 같은 기체 저장 및 액상 오염물 분리에 최적 화된 구조의 MOF 개발이 활발히 진행되고 있다[6-8]. MOF를 화학 반응 촉매로 활용한 연구도 활발하게 보고되 고 있으며, 기존 촉매에 비해 우수한 반응 효율을 나타내 고 있다[9, 10]. 예를 들어, 포피린 리간드로 형성한 MOF 인 ZnPOF는 포피린 단일 분자를 균일 촉매로 사용할 때 와 비교하여 높은 효율로 아세틸이미다졸을 피리딘메탄올 로 변환할 수 있음이 보고된 바 있다[11].
- 언급한 바와 같이 광범위한 응용 분야에 활용될 수 있 는 다양한 구조의 MOF가 개발되었고 현재도 새로운 구 조의 MOF를 합성하기 위한 많은 시도가 진행 중이다. 하 지만, 개발한 MOF가 지닌 미세 기공의 고유한 물리·화학 적 특성에 대한 심도있는 관찰은 충분한 연구가 필요한 실정이다. 벌크 용매 환경과 상이한 미세 기공 내부에서 MOF를 구성하는 유기 리간드 및 금속 클러스터와 게스트 분자 간 수소 결합, 파이-파이 상호 인력, 반데르발스 인 력에 기인한 호스트-게스트 상호 작용에 대한 이해가 요 구된다. 본 연구는 분자 수준에서 MOF와 게스트 분자 사 이의 상호 작용을 관찰하여 미세 기공의 역할을 파악하는 데 주목하였다. 이를 통하여 미세 기공 내부의 분자 간 상 호 작용 원리를 정립할 수 있으며, 향후 이 원리를 기반으 로 해당 응용 분야에 최적화된 MOF를 합리적으로 설계 하고 발굴할 수 있을 것이다.
- MOF의 미세 기공 안에서 균일하게 분산된 분자의 동역 학은 대부분 분자 역학 시뮬레이션을 통하여 연구되었고, 이를 바탕으로 한정된 공간에서 게스트 분자 거동 메카니 즘을 파악하였다[12]. 예를 들어, 입방체 기공 구조의 전형 적인 MOF 중 하나인 MOF-5를 활용하여 미세 기공 내부 에서 벤젠 분자의 확산에 대해 연구된 바 있다[13]. 시뮬 레이션을 통하여 벤젠 분자가 벌크 용매 환경과 비교하여 느리게 확산됨을 확인하였고, 테레프탈산과 산화 아연 클 러스터로 구성된 MOF-5의 골격에서 대부분의 벤젠 분자 는 산화 아연 클러스터에 인접하고 있음을 확인하였다. 이 는 MOF-5 골격체의 유연성에 기인한 격자의 동역학 때문 으로 추측되었다. 다른 예로, MOF-5의 미세 기공 안에서 다양한 길이의 알케인 분자 확산 현상이 연구된 바 있으 며, 알케인 분자 확산 속도는 벌크 용매 환경과 유사하지 만 제올라이트의 기공과 비교해 빠른 것이 입증되었다 [14]. 일련의 보고들을 통하여 MOF의 미세 기공 안에서 골격체-게스트 분자 및 게스트 분자-게스트 분자 상호 작 용에 대한 심층적인 이해가 가능하였다. 하지만, 실제 MOF가 활용되는 화학 반응 및 오염물 분리 환경에서 미 세 기공 내부에 존재하는 게스트 분자는 2 가지 이상일 가 능성이 높으며 이에 적합한 모델 시스템 구축 및 복합적 인 분자 간 상호 작용 이해가 필요하다.
- 본 연구에서는 크기가 다른 게스트 분자인 루테늄 트리 스바이피리딘(Rubpy)과 쿠마린 153(C153)을 각각 MOF-5 의 미세 기공 내부에 캡슐화하였고, 극성이 다른 용매 분 자 하에서 게스트 분자들의 광학적 특성 변화를 관찰하고 분자 수준에서 상호 작용을 해석하였다. MOF-5는 15 Å 직경의 미세 기공을 지니고 있어 Rubpy 및 C153 분자를 기공 내부에 캡슐화하기 적합하고, 다양한 용매 분자에 대 하여 골격체의 구조적 안정성이 높다[15-17]. 채택한 게스 트 분자들은 용매 분자의 극성에 민감하게 변화하는 용매 의존적 광학적 성질을 가지고 있다. 특히, Rubpy 분자에 서 루테늄 금속과 바이피리딘 리간드 간의 전하 이동 (MLCT) 흡수띠는 용매 극성에 의존적이고, 들뜬 에너지 상태의 이완 현상이 용매 극성에 의해 크게 영향을 받을 수 있다[18]. C153 분자는 다양한 극성의 용매에 높은 용 해도를 가지며, Rubpy 분자처럼 용매 의존적 흡수 및 방 출 스펙트럼의 변화를 보인다[19]. 이를 통하여 용매 극성 에 따른 Stokes shift 에너지를 도출하여 용매 분자의 재구 성 및 진동 완화에 소모되는 에너지 변화를 파악하며, MOF의 유무에 따른 변화를 통하여 제한된 공간에서의 게 스트 분자 거동을 이해할 수 있다. 본 연구에서는 벌크 용 매 환경에서 Rubpy와 C153 분자의 용매 의존 발색 현상 을 바탕으로, MOF-5의 미세 기공 내부에서 용매 분자 존 재 하에 Rubpy와 C153 분자의 광학적 특성 변화에 대해 관찰하고 분석하였다. 이를 통하여 한정된 공간에서 게스 트 분자-용매 분자-골격체 간의 다각적 상호 작용에 대한 이해를 도모할 수 있었다.
1. 서 론
- 2.1 원료 및 분석
- 실험에 사용한 질산아연 6수화물(98% 순도, Strem Chemicals), 테레프탈산(98+% 순도, Alfa Aesar), 쿠마린 153(99% 순도, Aldrich), 염화루테늄 수화물(97% 순도, Oakwood Products, Inc.), 2,2'-바이피리딘(bpy, 99% 순도, Aldrich), 헥사플루오로인산암모늄(99+% 순도, Alfa Aesar) 은 추가의 정제 없이 사용하였다. 흡수 및 방출 스펙트럼 측정에 사용한 아세토나이트릴(MeCN), 다이클로로메테인 (DCM), 디메틸포름아마이드(DMF)는 잔류 수분 제거 후 사용하였다. 획득한 시료는 다음과 같이 분석하였다. 엑스 선 회절 분석(XRD)은 Bruker-AXS D8 Advance Diffractometer, 비표면적은 ASAP 2020 Automated Surface Area and Porosimetry System, 주사전자현미경(SEM)은 FEI Quanta 200 Environmental Scanning Electron Microscope, 고체 시료 흡수 스펙트럼은 Perkin-Elmer Lambda 950 UV-Vis-NIR Spectrophotometer, 액체 시료 흡수 스펙트럼 은 Agilent 8453 Spectrometer, 방출 스펙트럼은 Spex 212 Fluorolog Fluorometer, 형광 이미지는 LSM-5 Pascal Laser Confocal Microscope를 사용하였다.
- 2.2 Rubpy@MOF 분말 제조
- 먼저, Ru(bpy)2Cl2 분자를 Ru(DMSO)4Cl2(DMSO=다이 메틸설폭사이드)로부터 합성하였다[20]. 그 후 아르곤 분 위기에서 0.6 g의 Ru(bpy)2Cl2와 0.194 g의 bpy를 30 mL의 에탄올에 투입하였다. 가열교반기 온도를 85°C로 설정한 뒤 교반하면서 12시간 반응을 진행하였다. 반응 후 용액 을 상온으로 식히고 소량의 헥사플루오로인산암모늄 수용 액을 주입하여 생성물을 침전시켰다. 침전된 붉은 분말은 여과를 통하여 수득한 후 100 mL의 증류수와 50 mL의 에 틸에테르로 세척하였다. 진공 건조 후 최종 분말(Rubpy) 을 회수하였다. 다음으로 아르곤 분위기에서 2.52 g의 질 산아연 6수화물과 0.477 g의 테레프탈산을 50 mL의 DMF 에 용해하였다[21]. 그 후 0.14 g의 Rubpy를 투입하고 가 열교반기 온도를 120°C로 설정한 뒤 교반하면서 16시간 반응을 진행하였다. 상온으로 식힌 후, 연한 오렌지색의 침전된 분말을 남기며 용매를 조심스럽게 제거하였다. 20 mL의 DMF를 주입하고 5분 방치한 후 용매만 제거하였다. 9회 반복하여 용액 내 잔여 전구체를 제거하였다. 연한 오 렌지색의 침전된 분말에 20mL의 클로로포름을 주입하고 5분 방치한 후 용매만 제거하였다. 6회 반복하여 기공에 잔류한 DMF를 제거하였다. 진공에서 클로로포름을 건조 하여 최종 분말(Rubpy@MOF)을 회수하였다.
- 2.3 C153@MOF 분말 제조
- MOF-5 분말은 위에서 언급한 방법과 동일하게 준비하 였다. 아르곤 분위기에서 2.52 g의 질산아연 6수화물과 0.477 g의 테레프탈산을 50mL의 DMF에 용해하였다. 가 열교반기 온도를 120°C로 설정한 뒤 교반하면서 16시간 반응을 진행하였다. 상온으로 식힌 후, 흰색의 침전된 분 말을 남기며 용매를 조심스럽게 제거하였다. 20 mL의 DMF를 주입하고 5분 방치 후 용매만 제거하는 과정을 9 회 반복한 후, 흰색의 침전된 분말에 20 mL의 클로로포름 을 주입하고 5분 방치한 후 용매만 제거하는 과정을 6 회 반복하였다. 진공에서 건조하여 MOF-5 분말을 회수하였 다. 다음으로 20mL의 메탄올에 0.0062 g의 C153를 용해 하여 농축된 C153 용액을 준비하였다. 0.05 g의 MOF-5 분말에 2 mL의 준비한 C153 용액을 투입하고 1일 방치하 였다. 분말(C153@MOF)만 남기며 용매를 제거하였다. 잔 류한 분말에 2mL의 클로로포름을 주입하고 5분 방치한 후 용매만 제거하였다. 5회 반복하여 C153@MOF의 기공 밖에 잔류한 C153 분자를 제거하였다. 스펙트럼 측정 시 클로로포름을 해당 용매로 교환한 후 분석을 진행하였다.
2. 실 험
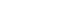
- 두 가지 다른 제조법을 적용하여 Rubpy와 C153 분자를 각각 MOF-5 내부에 캡슐화하였다(Fig. 1). Rubpy 분자는 직경이 12 Å이기에, MOF-5의 기공 크기는 15Å로 충분 하지만 기공 입구가 7 .5Å임에 따라 분자 확산을 통하여 내부에 적재될 수 없었다. 이를 극복하기 위하여 MOF-5 분말 제조 과정에 Rubpy 분자를 첨가하여 골격체 내부에 삽입하는 방식을 채택해 Rubpy@MOF를 획득하였다. 한 편, C153 분자는 직경이 4Å이기에 제조한 MOF-5 분말 을 고농도의 C153 용액에 넣고 방치하는 과정을 통하여 기공 내부로 C153 분자 확산을 유도해 C153@MOF를 획 득하였다. 이러한 게스트 분자 크기 차이를 기반으로 Rubpy@MOF에 비하여 상대적으로 많은 수의 용매 분자가 C153@MOF의 기공 안에 존재할 것을 예측할 수 있었다.
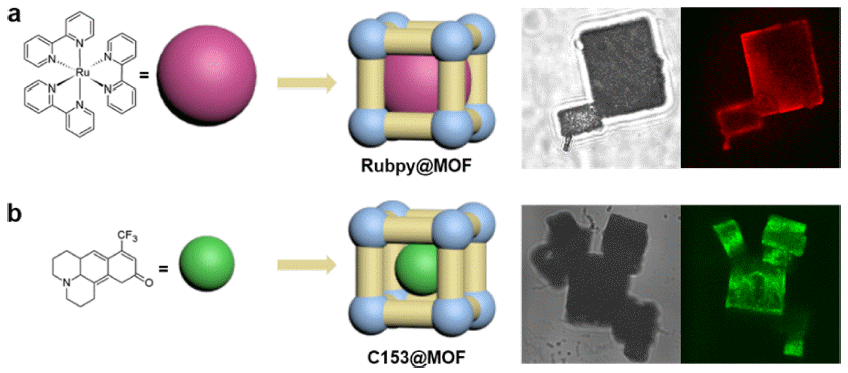
- 제조한 Rubpy@MOF와 C153@MOF 분말의 다공성 구 조는 XRD와 비표면적 측정을 통하여 확인하였다(Fig. 2). 게스트 분자의 캡슐화 방식이 다름에도 불구하고 Rubpy@MOF와 C153@MOF 분말에서 MOF-5의 결정 구 조는 그대로 유지되고 있음을 알 수 있었다. 각 분말에서 주요 피크(6.7 도, 9.8 도, 13.9 도)의 상대적 강도가 다른 것은 측정 시 분말의 배향이 다름에서 기인한 것으로 추 측된다. 비표면적은 게스트 분자가 없는 MOF-5는 693 m2/g, Rubpy@MOF는 7 87m2/g으로 유사하게 측정되었다. 이를 통하여 게스트 분자의 캡슐화 과정은 MOF-5의 결정 구조 및 다공성에 큰 영향을 미치지 않음을 판단할 수 있 었다.
- SEM 분석을 통하여 MOF-5와 Rubpy@MOF의 분말 형 태를 확인하였다(Fig. 3). 정육면체의 입자가 서로 결합되 어 있는 형태를 가지며, MOF-5 입자의 크기는 17.1 ± 4.8 μm로 측정되었다. Rubpy@MOF의 입자 크기는 26.8 ± 7.9 μm로 측정되어, MOF-5보다 상대적으로 큰 입자가 형성 되었다. 분말 제조 과정에 투입한 Rubpy 분자가 MOF-5 입자 형성 및 성장 시 작은 입자들을 연결하는 매개체로 역할 하였음을 추측할 수 있었다.
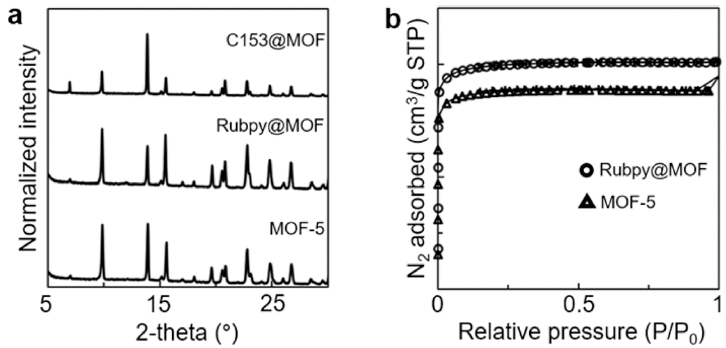
- Rubpy@MOF 분말을 극성이 다른 3 가지 용매 MeCN, DCM, DMF와 각각 혼합한 후 자외선-가시광 흡수 스펙트 럼을 확인하여 캡슐화 유무에 따른 변화를 확인하였다 (Fig. 4a-d). Rubpy 분자는 특유의 MLCT 흡수띠를 22000 cm-1에서 발현하며 연관된 낮은 강도의 흡수띠를 20500 cm-1에서 보여준다. 용매별 측정한 Rubpy@MOF의 흡수 스펙트럼에서 MLCT 흡수띠는 벌크 용매 환경과 비교하 여 낮은 에너지로 이동하였다. 이는 골격체로 인한 Rubpy 분자의 안정화 효과에 의하여 MLCT 흡수띠의 에너지가 낮아진 것으로 유추할 수 있다. Rubpy 분자 크기는 MOF- 5 기공 부피와 유사하여 Rubpy의 바이피리딘 리간드는 골 격체에 근접하게 되고 이는 들뜬 에너지 준위의 안정화로 귀속될 수 있다. 또한 흡수 스펙트럼의 형태가 1개의 단일 한 봉우리로 변화함을 통하여 진동-전자 전이에 상응하는 광학 특성은 감소한 것으로 파악되었다.
- C153@MOF 분말의 자외선-가시광 흡수 스펙트럼도 3 가지 용매 하에서 측정하였다(Fig. 4e-h). 모든 용매에서 C153@MOF의 최대흡수파장은 벌크 용매 환경과 비교하 여 낮은 에너지로 이동하였다. 이를 통하여 Rubpy@MOF 처럼 C153 분자의 들뜬 에너지 준위가 골격체에 의하여 안정화되었음을 예측할 수 있다. 또한 골격체와 C153 분 자의 상호 작용은 흡수 스펙트럼의 진동-전자 전이 신호 를 통하여 유추할 수 있다. C153의 진동-전자 전이 신호 는 DCM과 DMF 용매 하에서 발현되었으며 캡슐화되지 않은 C153의 스펙트럼 형태와 비교하여 비대칭적으로 관 찰되었다. 이러한 변화는 MOF-5의 기공 내부에 C153 분 자가 불균일하게 분포되어 있음을 시사한다. 문헌에 의하 면 벤젠 분자는 MOF-5의 기공에서 산화 아연 클러스터에 근접하여 위치하는 것이 확인된 바 있다[13]. 이와 유사하 게 DCM과 DMF 조건은 방향족 고리 구조를 포함한 C153 분자를 산화 아연 클러스터에 밀집하게 유도하는 것 으로 추정할 수 있다.
- Rubpy@MOF 분말의 방출 스펙트럼은 455 nm의 여기 파장을 사용하여 확인하였다(Fig. 5a-d). MOF-5에 의한 캡 슐화 후에도 Rubpy 분자의 방출 스펙트럼 형태는 유사하 게 유지되었다. 하지만, 모든 용매 조건에서 Rubpy@MOF 의 최대방출파장은 높은 에너지로 청색 이동하였음을 확 인하였다. Rubpy@MOF의 기공 대부분은 Rubpy 분자가 차지하고 있을 것으로 예상되며, 이는 벌크 용매 환경과 비교하여 Rubpy 분자 주위에 상대적으로 적은 양의 용매 분자가 존재하게 됨을 의미한다. 따라서 방출 파장의 청색 이동 현상은 여기 후 용매 분자의 재구성에 소모되는 에 너지 감소로 해석될 수 있다. 반면에 C153@MOF의 방출 스펙트럼은 400 nm의 여기 파장을 사용하였으며 모든 용 매 조건 하에서 낮은 에너지로 적색 이동하였다(Fig. 5eh). 이를 통하여 C153 분자는 MOF-5 기공 내부에 적재됨 에 따라 평형 들뜬 상태가 안정화될 수 있음을 추정할 수 있다. 일반적으로 형광 분자의 진동 에너지 완화 및 용매 분자 재구성에 의해 최대방출에너지의 감소가 발생한다. 캡슐화된 C153 분자는 골격체에 의하여 전자에 해당하는 에너지가 더 많이 소모되었을 것으로 추정된다.
- 용매 극성에 따른 Rubpy@MOF와 C153@MOF의 최대 흡수파장과 최대방출파장의 변화를 종합하였다(Fig. 6). Rubpy@MOF는 용매 극성이 증가할수록 흡수 에너지가 증가하는 것을 확인할 수 있었다. 하지만, 캡슐화 전 상태 에서 Rubpy의 흡수 에너지는 용매 극성 증가에도 불구하 고 감소하였다. 이는 골격체에 의한 용매 분자 거동의 변 화를 시사한다. 방출 에너지 변화는 용매 극성과 인과 관 계를 파악하기 어려우며 캡슐화 후에는 전체적으로 소폭 증가하는 것을 확인하였다. C153@MOF는 용매 극성이 증가할수록 흡수 에너지가 감소하는 것을 확인하였고, 이 는 캡슐화 전 상태의 C153 분자의 거동과 유사하다. 따라 서 용매 극성도에 의한 영향은 캡슐화 후에도 C153 분자 에 적용되고 있음을 파악할 수 있다. 방출 에너지 또한 캡 슐화 후 감소하는 경향을 확인할 수 있었다. 용매 극성에 따른 Stokes shift 그래프를 통하여 캡슐화 후 Rubpy는 적 색 이동 현상, C153는 청색 이동 현상을 확인할 수 있었 다. Rubpy@MOF의 적색 이동 현상은 감소한 흡수 에너 지와 증가한 방출 에너지에 기인한다. C153@MOF는 캡 슐화 이전과 비교하여 MeCN과 DCM 용매 하에서 높은 에너지를 가지는 것을 확인할 수 있었고, 이는 골격체에 의한 추가 에너지 손실로 유추할 수 있다. MOF-5 구조의 유연성으로 인하여 골격체 격자 구조 완화에 에너지 손실 이 발생하였을 가능성이 있으며, 이는 C153의 최대방출에 너지 감소로 연관될 수 있다.
3. 결과 및 토의
Fig. 1
Schematics of the encapsulation processes of (a) Rubpy and (b) C153 in MOF-5. Each guest molecule encapsulation is confirmed by the corresponding transmitted and fluorescence images on the right (excitation: 455 nm for Rubpy@MOF, 400 nm for C153@MOF).

Fig. 2
(a) XRD patterns of C153@MOF, Rubpy@MOF and MOF-5. (b) N2 isotherms of Rubpy@MOF (circle) and MOF-5 (triangle).

Fig. 4
(a-d) UV-visible absorption spectra of Rubpy (solid line) and Rubpy@MOF (dotted line) in different solvents ((a): no solvent, (b): MeCN, (c): DCM and (d): DMF). (e-h) UV-visible absorption spectra of C153 (solid line) and C153@MOF (dotted line) in different solvents ((e): no solvent, (f): MeCN, (g): DCM and (h): DMF).

Fig. 5
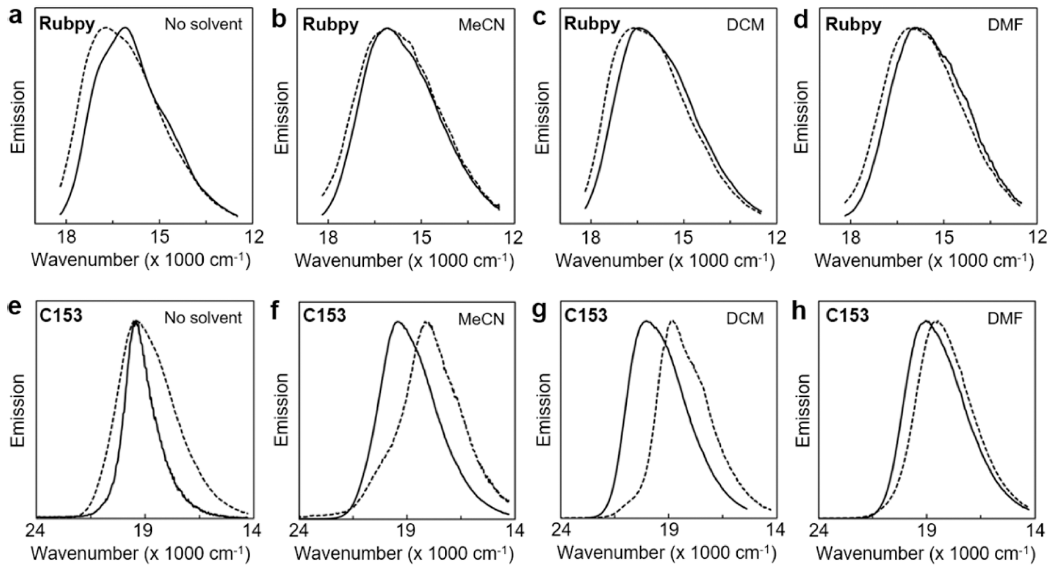
(a-d) Emission spectra of Rubpy (solid line) and Rubpy@MOF (dotted line) in different solvents ((a): no solvent, (b): MeCN, (c): DCM and (d): DMF). (e-h) Emission spectra of C153 (solid line) and C153@MOF (dotted line) in different solvents ((e): no solvent, (f): MeCN, (g): DCM and (h): DMF).

Fig. 6
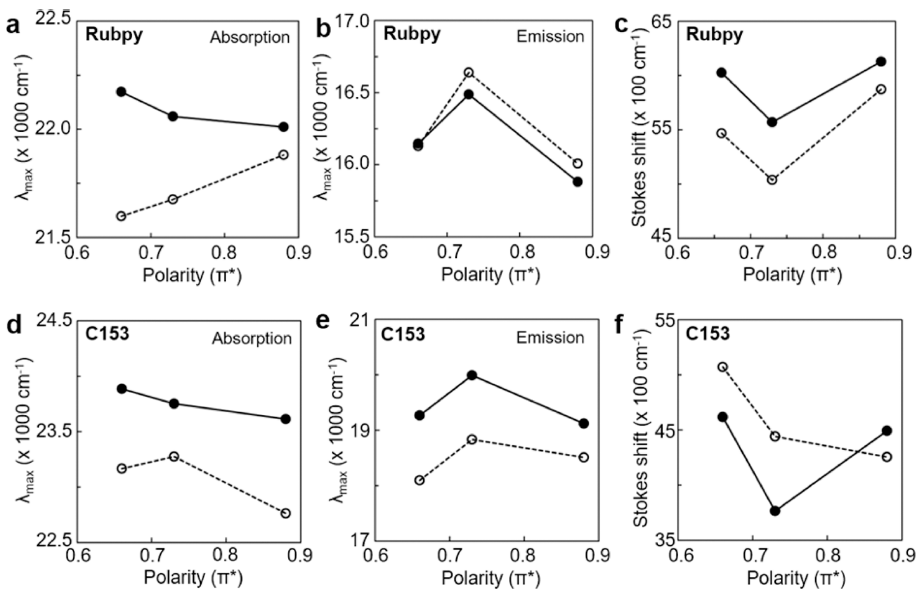
(a) Plot of absorption maxima as a function of solvent polarity with Rubpy (filled circle) and Rubpy@MOF (unfilled circle). (b) Plot of emission maxima as a function of solvent polarity with Rubpy (filled circle) and Rubpy@MOF (unfilled circle). (c) Plot of Stokes shifts as a function of solvent polarity with Rubpy (filled circle) and Rubpy@MOF (unfilled circle). (d) Plot of absorption maxima as a function of solvent polarity with C153 (filled circle) and C153@MOF (unfilled circle). (e) Plot of emission maxima as a function of solvent polarity with C153 (filled circle) and C153@MOF (unfilled circle). (f) Plot of Stokes shifts as a function of solvent polarity with C153 (filled circle) and C153@MOF (unfilled circle).

- 본 연구에서는 크기가 다른 게스트 분자인 Rubpy와 C153를 MOF-5 분말에 캡슐화해 광학적 특성 변화를 분 석하였으며, 이를 통하여 한정된 공간에서 복합적으로 발 생하는 호스트-게스트 분자적 상호 작용을 이해할 수 있 었다. 용매 분자 존재 시 캡슐화 전과 비교하여 골격체와 상호 작용에 의한 게스트 분자의 흡수 및 방출 스펙트럼 의 변화가 확인되었다. MOF-5의 기공과 유사한 크기의 Rubpy 분자는 캡슐화 후 Stokes shift 에너지가 감소하였 다. 이는 MOF-5 기공의 대부분을 차지하는 Rubpy 분자에 의해 상대적으로 적은 양의 용매 분자와의 상호 작용이 발생하였음을 추정할 수 있다. 이는 용매 분자 재구성에 소모되는 에너지 감소하였음을 의미한다. 작은 게스트 분 자인 C153의 흡수 및 방출 에너지는 캡슐화 후 전체적으 로 감소하는 것을 확인하였고, Stokes shift 에너지는 증가 하였다. 이는 골격체 격자의 완화에 소모된 에너지가 원인 으로 추정될 수 있다. 본 연구를 통하여 게스트 분자의 상 대적 크기에 따라 게스트 분자-용매 분자 및 게스트 분자- 골격체 간 복합적 상호작용에 있어, 작은 게스트 분자의 경우 전자가 우세하고 큰 게스트 분자의 경우 후자가 우 세함을 파악할 수 있었다. 그리고 골격체의 구조적 유연성 도 게스트 분자의 캡슐화를 통하여 제어될 수 있음을 확 인하였다. 본 연구 결과는 MOF의 촉매 반응, 액상 오염물 분리 및 약물 전달 기능 개선에 기여할 것으로 기대된다.
4. 결 론
-
Acknowledgements
- 이 성과는 2020년도 정부(과학기술정보통신부)의 재원 으로 한국연구재단의 지원을 받아 수행된 연구임(No. 2020R1C1C1007568)
감사의 글
- 1. M. Eddaoudi, D. B. Moler, H. Li, B. Chen, T. M. Reineke, M. O’Keeffe and O. M. Yaghi: Acc. Chem. Res., 34 (2001) 319. .ArticlePubMed
- 2. M. Eddaoudi, J. Kim, N. Rosi, D. Vodak, J. Wachter, M. O’Keeffe and O. M. Yaghi: Science, 295 (2002) 469. .ArticlePubMed
- 3. O. M. Yaghi, M. O’Keeffe, N. W. Ockwig, H. K. Chae, M. Eddaoudi and J. Kim: Nature, 423 (2003) 705. .ArticlePubMed
- 4. J. L. C. Rowsell and O. M. Yaghi: Microporous Mesoporous Mater., 73 (2004) 3. .Article
- 5. D. Hexiang, S. Gunder, K. E. Cordova, C. Valente, H. Furukawa, M. Hmadeh, F. Gándara, A. C. Whalley, Z. Liu, S. Asahina, H. Kazumori, M. O'Keeffe, O. Terasaki, J. F. Stoddart and O. M. Yaghi: Science, 336 (2012) 1018. .ArticlePubMed
- 6. K. Sumida, D. L. Rogow, J. A. Mason, T. M. McDonald, E. D. Bloch, Z. R. Herm, T. H. Bae and J. R. Long: Chem. Rev., 112 (2012) 724. .ArticlePubMed
- 7. M. P. Suh, H. J. Park, T. K. Prasad and D. W. Lim: Chem. Rev., 112 (2012) 782. .ArticlePubMed
- 8. J. R. Li, J. Sculley and H. C. Zhou: Chem. Rev., 112 (2012) 869. .ArticlePubMed
- 9. A. U. Czaja, N. Trukhan and U. Müller: Chem. Soc. Rev., 38 (2009) 1284. .ArticlePubMed
- 10. J. Lee, O. K. Farha, J. Roberts, K. A. Scheidt, S. T. Nguyen and J. T. Hupp: Chem. Soc. Rev., 38 (2009) 1450. .ArticlePubMed
- 11. A. M. Shultz, O. K. Farha, J. T. Hupp and S. T. Nguyen: J. Am. Chem. Soc., 131 (2009) 4204. .ArticlePubMed
- 12. S. Amirjalayer and R. Schmid: Microporous Mesoporous Mater., 125 (2009) 90. .Article
- 13. S. Amirjalayer, M. Tafipolsky and R. Schmid: Angew. Chem. Int. Ed., 46 (2007) 463. .ArticlePubMed
- 14. D. C. Ford, D. Dubbeldam, R. Q. Snurr, V. Künzel, M. Wehring, F. Stallmach, J. Kärger and U. Müller: J. Phys. Chem. Lett., 3 (2012) 930. .ArticlePubMed
- 15. F. Stallmach, S. Gröger, V. Künzel, J. Kärger, O. M. Yaghi, M. Hesse and U. Müller: Angew. Chem. Int. Ed., 45 (2006) 2123. .ArticlePubMed
- 16. S. Han, Y. Wei, C. Valente, I. Lagzi, J. J. Gassensmith, A. Coskun, J. F. Stoddart and B. A. Grzybowski: J. Am. Chem. Soc., 132 (2010) 16358. .ArticlePubMed
- 17. A. S. Münch, J. Seidel, A. Obst, E. Weber and F. O. R. L. Mertens: Chem. Eur. J., 17 (2011) 10958. .ArticlePubMed
- 18. E. M. Kober, B. P. Sullivan and T. J. Meyer: Inorg. Chem., 23 (1984) 2098. .Article
- 19. M. L. Horng, J. A. Gardecki, A. Papazyan and M. Maroncelli: J. Phys. Chem., 99 (1995) 17311. .Article
- 20. J. Kim, H. P. Yennawar and B. J. Lear: Dalton Trans., 42 (2013) 15656. .ArticlePubMed
- 21. J. Kim, M. R. Dolgos and B. J. Lear: Cryst. Growth Des., 15 (2015) 4781. .Article
Figure & Data
References
Citations
Citations to this article as recorded by 

Photophysical Properties of Guest Molecules Confined in Nanopores
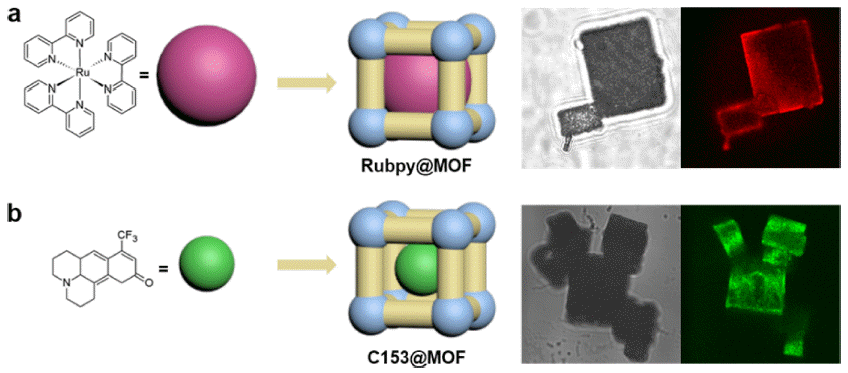


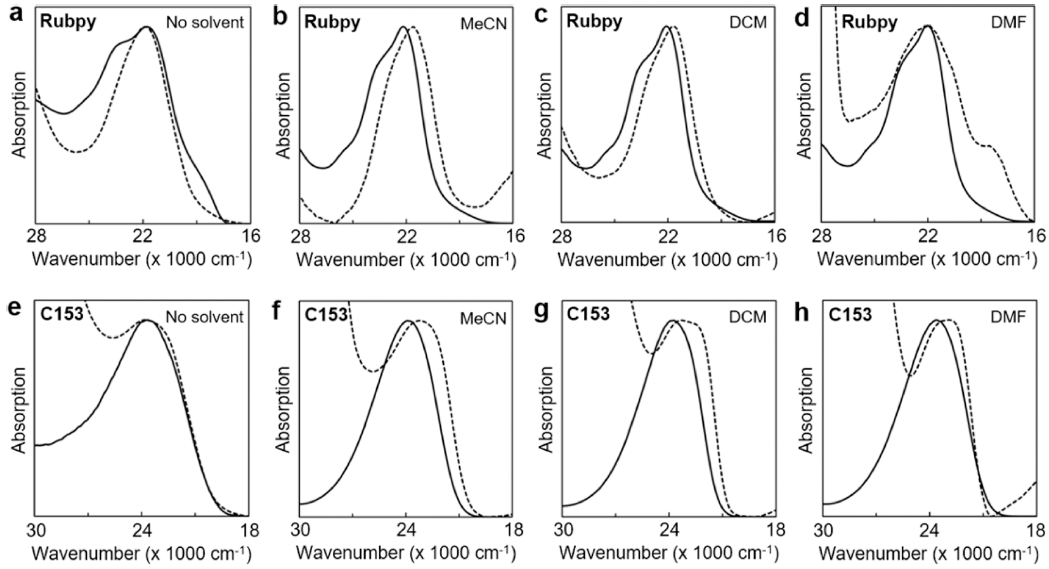
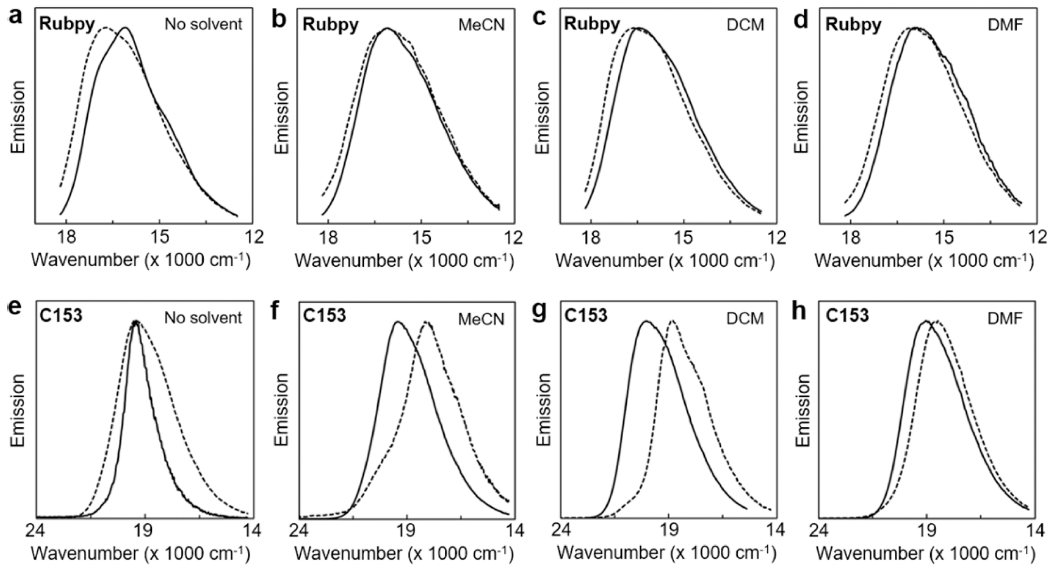
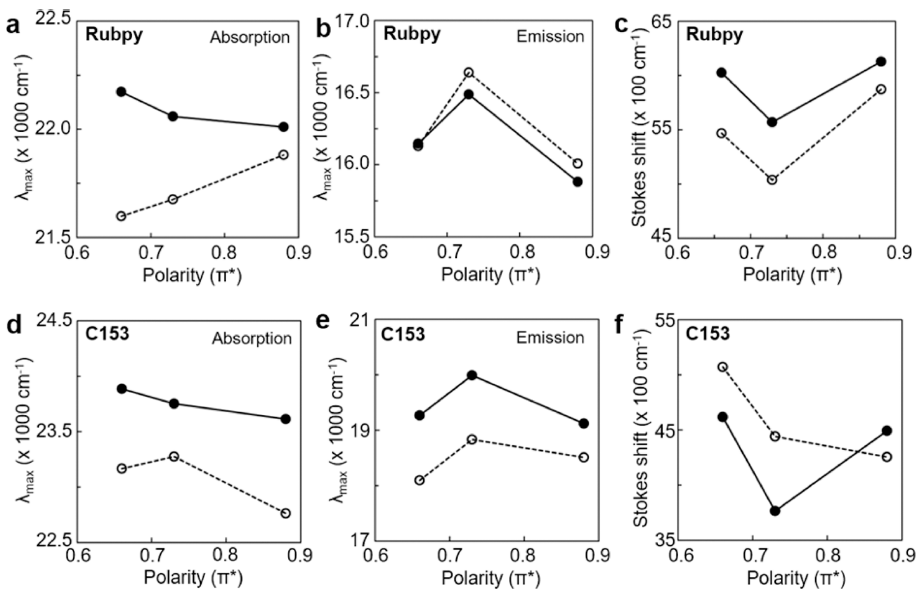
Fig. 1
Schematics of the encapsulation processes of (a) Rubpy and (b) C153 in MOF-5. Each guest molecule encapsulation is confirmed by the corresponding transmitted and fluorescence images on the right (excitation: 455 nm for Rubpy@MOF, 400 nm for C153@MOF).
Fig. 2
(a) XRD patterns of C153@MOF, Rubpy@MOF and MOF-5. (b) N2 isotherms of Rubpy@MOF (circle) and MOF-5 (triangle).
Fig. 3
(a, b) SEM images of MOF-5. (c, d) SEM images of Rubpy@MOF. Scale bars: 50 μm.
Fig. 4
(a-d) UV-visible absorption spectra of Rubpy (solid line) and Rubpy@MOF (dotted line) in different solvents ((a): no solvent, (b): MeCN, (c): DCM and (d): DMF). (e-h) UV-visible absorption spectra of C153 (solid line) and C153@MOF (dotted line) in different solvents ((e): no solvent, (f): MeCN, (g): DCM and (h): DMF).
Fig. 5
(a-d) Emission spectra of Rubpy (solid line) and Rubpy@MOF (dotted line) in different solvents ((a): no solvent, (b): MeCN, (c): DCM and (d): DMF). (e-h) Emission spectra of C153 (solid line) and C153@MOF (dotted line) in different solvents ((e): no solvent, (f): MeCN, (g): DCM and (h): DMF).
Fig. 6
(a) Plot of absorption maxima as a function of solvent polarity with Rubpy (filled circle) and Rubpy@MOF (unfilled circle). (b) Plot of emission maxima as a function of solvent polarity with Rubpy (filled circle) and Rubpy@MOF (unfilled circle). (c) Plot of Stokes shifts as a function of solvent polarity with Rubpy (filled circle) and Rubpy@MOF (unfilled circle). (d) Plot of absorption maxima as a function of solvent polarity with C153 (filled circle) and C153@MOF (unfilled circle). (e) Plot of emission maxima as a function of solvent polarity with C153 (filled circle) and C153@MOF (unfilled circle). (f) Plot of Stokes shifts as a function of solvent polarity with C153 (filled circle) and C153@MOF (unfilled circle).
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Photophysical Properties of Guest Molecules Confined in Nanopores
TOP
 KPMI
KPMI


 Cite this Article
Cite this Article