Articles
- Page Path
- HOME > J Powder Mater > Volume 30(1); 2023 > Article
-
Review Paper
열 원자층 식각법을 이용한 박막 재료 식각 연구 - 조현희, 이서현, 윤은서, 서지은, 이진우, 한동훈, 남서아, 한정환*
- Thermal Atomic Layer Etching of the Thin Films: A Review
- Hyeonhui Jo, Seo Hyun Lee, Eun Seo Youn, Ji Eun Seo, Jin Woo Lee, Dong Hoon Han, Seo Ah Nam, Jeong Hwan Han*
-
Journal of Korean Powder Metallurgy Institute 2023;30(1):53-64.
DOI: https://doi.org/10.4150/KPMI.2023.30.1.53
Published online: January 31, 2023
서울과학기술대학교 신소재공학과
Department of Materials Science and Engineering, Seoul National University of Science and Technology, Seoul 01811, Republic of Korea
- * Corresponding Author: Jeong Hwan Han, TEL: +82-2-970-6636, FAX: +82-2-973-6657, E-mail: jhan@seoultech.ac.kr
- - 조현희·이서현·윤은서·서지은·이진우·한동훈·남서아: 학생, 한정환: 교수
• Received: February 8, 2023 • Revised: February 17, 2023 • Accepted: February 17, 2023
© The Korean Powder Metallurgy Institute. All rights reserved.
- 6,331 Views
- 255 Download
- 2 Crossref
Abstract
- Atomic layer etching (ALE) is a promising technique with atomic-level thickness controllability and high selectivity based on self-limiting surface reactions. ALE is performed by sequential exposure of the film surface to reactants, which results in surface modification and release of volatile species. Among the various ALE methods, thermal ALE involves a thermally activated reaction by employing gas species to release the modified surface without using energetic species, such as accelerated ions and neutral beams. In this study, the basic principle and surface reaction mechanisms of thermal ALE?processes, including “fluorination-ligand exchange reaction”, “conversion-etch reaction”, “conversion-fluorination reaction”, “oxidation-fluorination reaction”, “oxidation-ligand exchange reaction”, and “oxidation-conversion-fluorination reaction” are described. In addition, the reported thermal ALE processes for the removal of various oxides, metals, and nitrides are presented.
- 반도체 소자의 미세화에 따른 소자 집적도는 계속해서 증가하고 있으며, 반도체 산업에서의 기술 노드(technology node)는 7 nm에 이어 5 nm 소자가 양산되고 있다. 또한, 더 높은 집적도를 위해 나노 단위를 넘어 원자 수준 의 증착 및 식각 공정 등의 연구가 활발하게 이루어지고 있다. 특히 반도체 소자 미세화에 따라 단채널 효과(short channel effect)에 의한 누설 전류 발생 및 소자 집적도의 한계를 극복하기 위해 기존의 평면 구조에서 벗어난 3차 원 구조의 소자가 적용되었다. 이러한 3차원 구조의 소자 는 높은 종횡비(high aspect ratio)를 가지므로, 3차원 구조 에서의 증착 및 식각 공정 시 높은 균일도와 원자 단위 공 정의 정확성이 요구된다[1, 2].
- 특히 현재 주로 사용되는 반응성 이온 식각법(reactive ion etching, RIE)의 경우 모든 식각이 공정시간 동안 연 속적이며 높은 공정 속도로 진행되므로 생산성이 높다는 장점이 있지만, 표면의 거칠기가 일정하지 않고, 비등방 성 식각이므로 단차 피복성(step coverage)이 낮아 높은 종횡비의 구조에서 균일도를 만족하기 어렵다는 문제점 이 있다[3].
- 이와 달리 최근 주목 받고 있는 원자층 식각법(atomic layer etching, ALE)은 자기제한적 반응(self-limiting reaction) 을 통해 박막을 순차적으로 제거하는 식각 공정법으 로, 높은 종횡비를 만족할 수 있으며 노출된 모든 표면을 같은 양으로 식각하여 박막 균일도 및 정밀한 두께 제어 가 가능한 식각 방법이다. 또한, RIE에서 나타나는 화학종 의 동시다발적인 흐름으로 인한 복잡성을 해결할 수 있으 며, 모서리 잔여물(corner residue)를 최소화하는 강점을 가 지고 있다. 또한 열 원자층 식각법(thermal ALE)의 경우 plasma ALE와 비교하여 3차원 구조에서 요구되는 등방성 식각(isotropic etching)을 원자 단위 정확도를 갖고 식각 할 수 있는 장점이 있기 때문에 복잡한 구조의 3차원 반 도체 공정에 적합한 공정 기술이라 할 수 있다[4]. 본 연 구에서는 큰 관심을 받는 차세대 식각 기술인 ALE에 대 한 전반적인 원리 및 thermal ALE를 이용한 다양한 산화 막, 금속막, 질화막의 공정에 대하여 논하고자 한다.
1. 서 론
- 2.1. ALE의 원리
- ALE는 표면 흡착 및 표면 제거의 개별적인 반응의 반 복을 통해 물질을 제거하는 식각법이며, 보통은 4단계의 반응으로 나뉜다: (A) 표면 흡착(surface absorption), (B) 초과 반응물 퍼지(purge), (C) 표면 제거(surface desorption), (D) 휘발성의 반응 생성물 퍼지(purge)[5]. 이 네 가 지 반응을 한 사이클로 하여, ALD(atomic layer deposition) 반응과 유사하게 사이클 반복을 통하여 원자층 단위로 물질을 식각하는 방법이다. 표면 흡착 반응(A)은 전구체 (precursor)가 식각 될 표면에 자기 제한적으로 흡착되어 표 면의 반응성을 높여준다. 표면 제거 반응(C)은 표면과 반응 성이 높은 반응물(reactant) 주입을 통해 표면에 화학적으로 흡착된 층을 휘발성의 부산물로 바꾸며 물질을 제거한다.
- ALE에서 A와 C 두 반응의 반복은 한 단계의 반응으로 휘발성 화합물을 만들 수 없는 물질에 필요하다. 예를 들 어 대부분의 금속이 A반응을 위한 물질(O2, O3, HF 등)과 반응할 수 있지만, 실질적인 식각에 적용되기에는 A반응 을 통해 형성되는 산화물 및 할로겐화물의 녹는점이 너무 높으므로 리간드 교환을 통해 휘발성의 부산물(byproduct) 을 형성하는 C반응이 필요하다. ALE에서의 표면 흡착 반 응(A)과 표면 제거 반응(C)으로 분리되는 불연속적 반쪽 반응(half-reaction)은 RIE에서의 연속적 반응을 통해 혼합 층이 두껍게 형성되는 것과 더불어 이어지는 플라즈마 식 각에서 끝없는 반응을 피함으로써 자기 제한적 식각 반응 을 가능하게 한다.
- 보통 ALE는 플라즈마를 사용하는 plasma ALE와 열에 너지를 사용하는 thermal ALE로 구분된다. Plasma ALE는 표면 제거 단계에서 플라즈마 충격이 식각에 사용되며 표 면 흡착 단계에서는 플라즈마 보조 흡착이 일어나 저온에 서 ALE가 가능하다. 벌크 물질이 아닌 개질된 층의 제거 를 위해 이온 에너지를 조정하지만, 두 물질의 스퍼터링 문턱 전압이 너무 근접해서 완벽한 자기 제한적 거동이 불가능하다. 따라서 고에너지의 플라즈마에 의해 소자의 손상을 가져올 수 있으므로 높은 플라즈마 에너지에 의한 데미지를 최소화 하기 위해서는 열에너지를 이용한 thermal ALE가 선호되고 있다.
- Thermal ALE를 시작하기 위해서는 상온의 26 meV보다 더 높은 활성화 에너지가 필요하기 때문에, 높은 온도로 챔버를 가열하는것이 필요하다. Thermal ALE의 경우 열 에너지만 관여하기 때문에, 적절한 반응 전구체를 선택할 경우 높은 식각 선택도를 가질 수 있다. 따라서 고종횡비 구조물 내부의 도달하기 어려운 장소에서도 표면, 모서리, 가장자리의 침식 및 잔여물 없이 특정 재료를 제거할 수 있다.
- Thermal ALE는 중성 기체와 열 에너지를 이용하여 하 부의 박막 및 소자에 데미지를 최소화할 수 있는 식각법 이다. Thermal ALE는 크게 표면에서 기상 반응물의 물리 적, 화학적 흡착단계와 표면에서의 반응 생성물 탈착단계 로 나뉜다. 먼저, 기체 분자는 표면에 물리적으로 흡착된 후, 활성화 에너지를 극복하여 화학적으로 흡착된다. 그러 나 고온에서 물리적으로 흡착된 분자는 흡착 속도와 같은 속도로 탈착되어 화학적으로 흡착하는 단계로 넘어가지 않아, 온도가 증가할수록 초기 흡착 계수 또는 화학적으로 흡착하는 속도가 감소하는 현상이 흔하게 관찰된다. 이러 한 거동은 전구체가 매개된 흡착 모델(precursor-mediated adsorption model)과 일치한다. 따라서 식각시키는 화학종 이 화학적으로 흡착하는 속도를 Fig. 1에 나타난 바와 같 이 온도 증가에 따라 감소 곡선처럼 나타낼 수 있다.
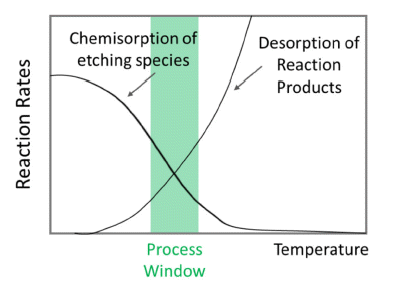
- Thermal ALE가 발생하기 위해서는 전구체 화학종의 흡 착 곡선과 반응 생성물의 탈착 곡선이 같은 온도 범위에 서 비슷한 반응 속도를 가져야 한다. 따라서 식각 공정 온 도 범위(process temperature window)는 기체 분자의 흡착 과 반응 생성물의 탈착 속도 그래프가 겹쳐지는 구간으로 정의한다. 그러나, 많은 물질이 앞서 언급한 전구체 매개 화학 흡착이 충분한 속도로 진행될 수 없을 정도의 높은 온도에서 화학반응과 탈착에 관여한다. 이는 Fig. 2a에서 확인되며, 화학 흡착 및 반응물의 탈착에 의한 식각이 가 능하기 위해서는 저온과 고온 사이를 왕복해야 한다. 하지 만 이렇게 단시간 내에 웨이퍼를 가열 냉각시키기는 것은 현실적으로 불가능하다. 따라서 일정한 표면 온도에서 thermal ALE를 진행하기 위해, C단계(개질된 표면의 표면 제거반응)를 도입하여 반응 생성물이 반응물2의 흡착이 가능한 더 낮은 온도에서 탈착되도록 한다. 이는 Fig. 2b 에서 확인할 수 있다. 즉, 표면 제거를 위해 공급한 반응물 2가 공정 온도 범위에서 흡착, 반응함으로써 개질 단계의 가스 흡착과 최종 반응물의 탈착이 가능한 것이다[5, 6].
- 2.2. ALE 반응의 메커니즘
- 일반적으로 알려진 thermal ALE의 메커니즘은 연속적 인 불소화-리간드 교환 반응(fluorination-ligand exchange reaction)에 기반한다. 하지만 모든 물질이 불소화-리간드 교환 반응을 통해 ALE가 가능한 것은 아니므로, “전환 식 각(conversion-etch)”, “전환-불소화 반응(conversion-fluorination)”, “산화-불소화 반응(oxidation-fluorination)”, “산화- 리간드 교환 반응(oxidation-ligand exchange reaction)”, “산화-전환-불소화 반응(oxidation-conversion-fluorination)” 등 기존 메커니즘에 기반한 새로운 방법이 개발되고 있다.
- 불소화-리간드 교환 반응의 예시로, HF/trimethylaluminum( TMA) 또는 HF/Sn(acac)2를 사용하는 Al2O3 ALE 가 있다[7-9]. 상기 반응의 경우 먼저 HF 가스가 Al2O3 박 막 표면과 반응하여 AlF3 층을 형성한다. 다음으로 퍼지 가스를 주입하여 잔류 HF와 H2O, CH4 또는 SnF(acac)와 같은 기상 반응 생성물을 제거한다. 이후 불화물이 형성된 박막 표면에 TMA나 Sn(acac)2와 같은 반응물2를 주입하 여 리간드 교환을 통해 AlF3 표면층을 안정하고, 휘발성을 가진 반응 생성물로 바꿔주어 식각이 가능하게 한다. 마지 막으로, 퍼지를 통해 남은 반응물2인 TMA 또는 Sn(acac)2 와 AlF(CH3)2, Al(acac)3, SnF(acac)와 같은 휘발성의 잔류 식각 생성물을 제거한다.
- 전환 식각은 불소화-리간드 교환 반응으로 식각되지 않 는 금속 산화물 표면을 다른 금속 산화물로 바꾸어 ALE 반응를 진행하는 방식이다. 예를 들어, SiO2와 Si3N4는 Si- F 결합이 매우 강해 Si을 포함하는 휘발물질을 생성하는 리간드 교환 반응이 일어나지 않기 때문에 전환 식각법이 필요하다. 이 방법의 핵심은 TMA 반응물에 노출시켜 SiO2를 Al2O3로 바꾸는 것이다. 이후 공정은 불소화-리간 드 교환 반응을 이용한 Al2O3 식각과 유사하다. 해당 메커 니즘은 SnO2, ln2O3, Si3N4, ZrO2 ALE에도 적용할 수 있 다[10, 11].
- 해당 전환 메커니즘은 표면의 불소화로 휘발성 불화 물 질을 생성하여 자발적인 식각을 하는 금속 산화물을 생성 한다. 이는 산화 텅스텐과 산화 몰리브덴에 적용할 수 있 으며, WO3의 경우에선 WO3 표면은 BCl3의 노출에 의해 B2O3로 전환되고, 전환된 B2O3는 HF에 의해 자발적으로 식각된다. B2O3가 제거되면서 드러나는 WO3는 HF에 의 해 식각되지 않으므로 자발적으로 식각을 멈추는 역할을 한다. 또한, W을 산화시킨 후 전환-불소화 반응을 통해 ALE를 진행할 수도 있다[12].
- 산화-불소화 반응은 휘발성이 높지 않은 반응 생성물이 형성되는 경우 높은 휘발성의 식각 생성물을 형성하기 위 해 산화를 통해 표면 개질을 한 후 불소화 반응을 하는 과 정을 말한다. 따라서 산화된 표면은 이후 불소화 과정을 통해 높은 휘발성의 반응 생성물을 형성하여 식각 반응이 이루어진다[13]. O3/HF를 사용한 TiN ALE를 예로 들자면, 가장 휘발성이 높은 Ti 화합물은 TiF4로 +4가의 산화가를 갖는 반면, +3가의 TiF3 화합물은 낮은 휘발성을 가져 식 각 반응이 일어나지 않음을 알 수 있다. O3는 Ti의 산화가 가 +3인 TiN를 +4인 TiO2로 산화시키고, 반응성이 높은 TiO2 표면층은 HF에 의해 자발적으로 식각된다[14]. 이러 한 산화 반응을 통해 불소화-리간드 교환 반응만으로는 식 각하기 어려운 물질을 제거할 수 있다.
- 이 메커니즘은 주로 Si 물질을 재료로 사용하는 ALE와 관련이 있다. Si을 높은 온도에서 O2 또는 O3와 반응시켜 산화시킨 후 TMA 노출로 산화된 표면을 Al2O3로 전환시 키는 방법이다[15]. 전환 식각과 마찬가지로 전환된 Al2O3 은 불소화-리간드 교환 반응을 통해 제거된다.
- 이 방식은 불소화-리간드 교환 반응과 유사한 메커니즘 을 갖는다. 휘발성이 낮아 식각이 힘든 물질 중 하나인 Cu 금속을 예로 들면, Cu를 O3를 이용하여 산화시킨 후 Hfac 반응물을 이용하여 휘발성을 갖는 반응 생성물을 만들어 제거한다[16].
2. ALE의 원리 및 반응 메커니즘
Fig. 2
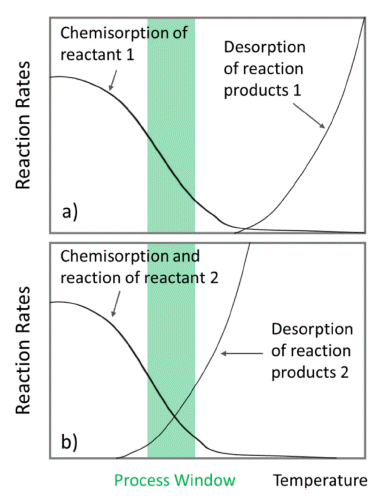
Schematic illustration of the temperature process window for thermal isotropic ALE at constant temperature. Panel (a) shows the chemisorption of a reactant 1 without initiating etching representing a modification step in thermal ALE. In panel (b), this modified surface is exposed to a reactant 2, which results in a surface layer that desorbs at the given wafer temperature resulting in etching of the modified layer [6].

2.2.1. 불소화-리간드 교환 반응(fluorination-ligand exchange reaction)
2.2.2. 전환 식각(conversion-etch)
2.2.3. 전환-불소화 반응(conversion-fluorination)
2.2.4. 산화-불소화 반응(oxidation-fluorination)
2.2.5. 산화-전환-불소화 반응(oxidation-conversion-fluorination)
2.2.6. 산화-리간드 교환(oxidation-ligand exchange reaction)
- 3.1. 산화물 thermal ALE
- 대부분 Al2O3의 ALE는 불소화 반응과 리간드 교환 반 응의 두 단계로 진행된다. Al2O3 ALE의 첫 연구는 HF와 Sn(acac)2를 각각 반응물(reactant)과 금속 전구체(metal precursor) 로 하여 진행되었으며, HF와 Sn(acac)2의 개별적인 반응의 반복을 통해 원자 단위의 식각이 가능하다고 보고 되었다[7]. 먼저 HF 노출 시 Al2O3의 표면에 AlF3가 형성 되고, 표면이 모두 불소화되면 반응이 자발적으로 멈춘다. 그 후 Sn(acac)2에 표면을 노출시키면 리간드 교환 반응으 로 AlF3이 Al(acac)3, SnF(acac)와 같은 휘발성 화합물을 형성하며 제거된다.
- 또 다른 금속 전구체로 TMA를 이용한 Al2O3의 ALE를 진행한 연구가 보고된다[8, 9]. HF/Sn(acac)2 반응물을 이 용한 ALE와 유사하게, TMA의 CH3과 표면에 형성된 불화 물과의 리간드 교환 반응을 통해 휘발성의 AlF(CH3)2 부산 물을 형성하여 Al2O3의 식각이 일어나는 메커니즘이다.
- Fig. 3 (a)에서 볼 수 있다시피, 250°C에서 325°C 내 식 각 온도 범위에서 선형적인 질량 감소 변화를 관찰 할 수 있다. 250°C에서 0.14 Å/cycle, 325°C에서 0.75 Å/cycle의 식각 속도를 나타내며 HF/Sn(acac)2를 이용한 ALE와 유 사하게 온도에 비례하여 식각 속도가 증가함을 관찰할 수 있다.
- 마지막으로 DMAC(AlCl(CH3)2)와 HF 반응물을 통해서 도 Al2O3의 ALE가 가능하다고 알려져 있으며, HF의 불소 화 반응을 통해 형성된 AlF3와 DMAC 내 CH3, Cl 리간드 의 반응을 통해 휘발성의 AlF(CH3)2, AlFCl(CH3)와 같은 화합물을 형성하며 Al2O3의 ALE가 진행된다[8, 17].
- Fig. 3 (b)에서 관찰할 수 있듯이, 다른 반응물과 마찬가 지로 특정 온도 범위 내 선형적인 식각 거동을 보이며, 225°C와 300°C에서 0.10 Å/cycle, 0.69 Å/cycle의 식각 속 도를 나타낸다. 또한, DMAC의 경우는 200°C 이하의 온 도에서 Al2O3의 식각 반응 대신 AlF3의 증착 반응이 일어 나 오히려 질량이 증가함을 확인할 수 있다.
- 앞서 언급한 대로 Sn(acac)2, TMA, DMAC 세 가지 전구 체 모두 불소화-리간드 교환 반응이라는 메커니즘을 통해 Al2O3의 ALE를 진행하지만, 물질마다 식각이 발생하는 온 도에 차이가 있음을 알 수 있다. 이는 전구체마다 리간드 교환 반응의 활성화 에너지 차이에 의해 나타나는 현상으 로, Fig. 4에서 Sn(acac)2는 ≥150°C의 온도에서 Al2O3를 식 각 할 수 있는 반면, DMAC는 더 높은 온도인 ≥225°C, TMA는 ≥250°C에서 Al2O3를 식각한다는 것을 관찰할 수 있다[8]. 이러한 식각 임계 온도 차이는 선택적 Thermal ALE의 또 다른 방법으로 활용될 수 있음을 암시한다.
- Al2O3 ALE와 마찬가지로, HfO2의 ALE도 주로 불소화- 리간드 교환 반응의 반복을 통해 이루어진다고 보고된다. 또한, 반응물과 금속 전구체도 유사하게 HF와 Sn(acac)2, HF와 DMAC를 이용하여 아래와 같은 반응 메커니즘에 의해 식각 과정이 진행된다[18].
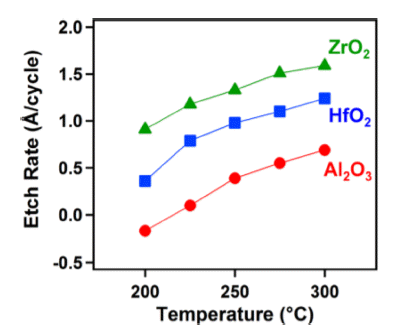
- HF와 DMAC를 이용한 HfO2 ALE의 식각 속도는 Fig. 5에 나타난 바와 같이 250°C의 온도에서 ALE cycle(time) 에 비례하여 선형적인 식각 거동을 나타냄을 관찰할 수 있다[8, 17]. 추가적으로 Fig. 6을 통해 Al2O3 ALE와 마찬 가지로 온도에 비례하여 식각 속도가 증가한다는 것을 알 수 있다. HF/DMAC를 이용한 HfO2 ALE의 경우 200°C, 250°C, 300°C에서 각각 0.36 Å/cycle, 0.98 Å/cycle, 1.24 Å/cycle의 식각 속도를 나타냄을 알 수 있다.
- ZrO2의 ALE 반응도 Al2O3와 HfO2 ALE와 동일하게 불 소화-리간드 교환 반응을 통해 진행된다고 알려져 있다. ZrO2의 식각은 대표적으로 HF의 불소화 반응과 DMAC의 리간드 교환 반응을 통해 이루어진다[8, 17].
- ZrO2 ALE는 HfO2와 유사하게 cycle 수에 따라 선형적 인 질량 감소 변화를 나타내며, 이를 통해 HF와 DMAC의 공급 시 자기 제한적 표면 반응을 통한 ALE가 진행된다 는 것을 확인할 수 있다. 또한, 200°C에서 0.91 Å/cycle, 250°C에서 1.33 Å/cycle, 300°C에서 1.59 Å/cycle로, 온도 에 따라 식각 속도가 빨라지는 것을 확인할 수 있다.
- HfO2과 ZrO2의 ALE는 Al2O3의 ALE와 동일한 메커니 즘을 통해 진행되지만, Al2O3 ALE와는 다르게 Fig. 7 (b) 와 (c)에서 볼 수 있듯이 HF의 불소화 반응 후 TMA 전 구체 공급에 따른 리간드 교환 반응이 일어나지 않는 것 을 확인할 수 있다. 추가적으로, Fig. 7 (a)에서 HF/TMA 를 노출시키는 것보다 HF/DMAC를 노출시킬 때 Al2O3의 질량 변화가 확연하게 나타나는 것을 확인할 수 있다. 이 는 TMA는 리간드 교환 반응에 참여할 수 있는 리간드가 CH3 리간드 하나이지만, DMAC는 CH3뿐만 아니라 반응 성이 높은 Cl 리간드를 가지고 있어 Al2O3의 더 빠른 식 각을 가능하게 할 것이라 예상할 수 있다. 또한, Hf(CH3)4, Zr(CH3)4 화합물은 Hf-C와 Zr-C 결합이 고온에서 불안정 하여 TMA 노출 시 CH3 리간드 교환 반응이 진행되지 않 지만, DMAC의 노출 시 Cl 리간드에 의해 HfCl4, ZrCl4는 휘발성의 안정한 화합물을 형성하게 되어 Fig. 7(b)-(c)와 같은 결과를 나타낸 것이라 예상할 수 있다.
- SiO2는 앞서 언급하였더 Al2O3, HfO2, ZrO2의 ALE 반 응 메커니즘과는 다르게 HF 반응물 노출 시 표면의 불소 화 반응이 아니라, 휘발성의 불화물을 발생시키기 때문에 앞선 방식을 이용하여 ALE가 진행되지 않는다. 그러므로 SiO2의 표면을 개질하여 불소화-리간드 교환 반응에 의한 ALE 식각 물질로 변경시킨 후, 변경된 물질의 ALE 반응 을 발생시키는 전환 식각(conversion-etch)을 이용한 SiO2 의 ALE가 보고된다[10].
- Fig. 8 (a)의 모식도와 같이 SiO2 표면에 TMA를 노출시 켜 표면의 일부를 Al2O3로 변경시킨 후, 개질된 Al2O3는 앞서 다뤘던 불소화-리간드 교환 반응을 단계적으로 발생 시켜 SiO2의 ALE 반응을 진행한다.
- 또한 SiO2의 ALE는 Fig. 8 (b)에서 볼 수 있다시피, 반 응물의 공정 압력이 달라짐에 따라 0.07 Å/cycle에서 0.27 Å/cycle로 압력에 비례하여 식각 속도가 증가함을 관찰할 수 있다.
- SiO2의 ALE와 유사하게, 산화물 반도체인 ZnO의 ALE 도 TMA 전구체의 노출을 통해 ZnO 표면에 Al2O3를 형 성한 후, Al2O3의 HF의 불소화 반응과 TMA의 리간드 교 환 반응의 반복을 통해 이뤄지게 된다[19].
- Fig. 9를 보면, 205°C에서 0.01 Å/cycle, 295°C에서 2.19 Å/cycle의 식각 속도를 나타내며 온도에 비례하여 식각 속 도가 증가함을 알 수 있다. 또한, 235°C에서 295°C 범위에 서는 식각 속도의 증가가 더디게 나타나는데, 이는 ZnO의 전환 반응보다 Al2O3가 불소화되는 반응이 온도에 의존적 이지 않아, 한 사이클 후 ZnO 표면에 남아있는 Al2O3층이 다음 사이클에서 ZnO의 전환 반응을 제한하게 되어 ALE 반응이 포화 되는 것이라 예상할 수 있다.
- 3.2. 금속의 thermal ALE
- 다양한 금속 재료에 대하여 ALE가 적용될 수 있는데, 반도체 소자에서 많이 적용되는 대표적인 배선 소재 중 하나인 W의 ALE 반응 메커니즘으로는 산화-전환-불소화 반응(oxidation-conversion-fluorination)과 산화-리간드 교 환(oxidation-ligand exchange) 두 가지 방법이 있다. 산화- 전환-불소화반응 방법의 경우 우선 O2, O3, N2O와 같은 산 화제를 이용해 W의 표면을 산화시킨다. 그 뒤 BCl3 과 같 은 물질과 반응시키면 산화된 WO3는 표면에서 B2O3로 전 환된다. 마지막으로 HF 반응물을 공급하면 표면의 B2O3 가 휘발성의 BF3로 바뀌면서 식각된다[12].
- Fig. 10을 통해 반응온도 207°C에서 W ALE cycle에 따 른 W 박막의 두께 변화를 확인할 수 있고 이로부터 식각 속도가 약 2.56 Å/cycle인 것을 알 수 있다. 그러나 산화- 전환-불소화반응 방법은 각 반응단계에서 반응 물질의 공 급 시간이 충분히 길어야 하는 단점이 있다. 또한, 불소화 반응 과정에서 사용되는 HF는 극성이 큰 물질이기 때문 에 reactor의 벽에 달라붙어 반응 속도가 저하되어 더 긴 퍼지 시간이 필요하다. 그래서 산화-전환-불소화반응과 다 른 방법인 산화-리간드 교환 방법이 연구되었다[20]. 산화 -리간드 교환 방법은 O2, O3, N2O와 같은 산화제를 이용해 W의 표면을 산화시키는 것까지는 앞선 방법과 동일하지 만 이후 WF6, WCl6, Cl2 등의 물질과 WO3를 반응시켜 WOxFy, WOxCly 형태의 휘발성 화합물을 만들어 내어 식 각하는점에서 차이가 있다.
- 여기서 사용되는 WF6는 알짜 쌍극자 모멘트가 0이므로 HF와는 다르게 반응 시 reactor의 벽에 흡착되는 것이 적 고 따라서 반응 후 reactor 퍼지가 용이하다. 그러므로 공 정 시간이 비교적 짧은 리간드 교환 과정에서 사용될 수 있지만 275°C 이상의 고온에서만 휘발성 있는 부산물이 형성될 수 있다는 특징을 가진다. 반면에, WCl6를 사용하 면 상온에서도 부산물인 WOxCly(g)를 형성하는 것이 가능 하고 200°C 부근에서 휘발되기 때문에 WCl6가 WF6보다 선호되는 부식 가스라고 할 수 있다.
- 반도체 공정의 배선 소재로 활용되는 Cu의 ALE는 표면 산화를 통해 CuOx 형성 후 이 산화물을 리간드 교환 방법 으로 제거하는 단계로 진행된다. 각 단계에서 화학종은 target 금속, 산화층 각각에만 반응하므로 선택적인 자기 제한적 식각이 가능하고 표면이 균일한 식각이 가능하다. 이 반응들은 불연속적으로 일어나기 때문에 Cu를 훨씬 정 교하게 식각할 수 있는 방법이다. 또한, 비교적 낮은 압력 에서 쉽게 반응이 가능하다는 특징이 있다.
- 먼저, 산화제로 O2나 O3를 사용해 Cu 표면에 산화물이 형성되면 Hhfac(hexafluoroacetylacetone) 를 반응물로 하 여 휘발성 부산물을 형성함으로써 산화막을 제거하는 메 커니즘을 나타낸다[16]. 여기서 사용되는 Hhfac는 300°C 이하의 낮은 온도에서 반응이 일어나며 Cu의 재증착이 일 어나지 않고 산화된 구리 금속만 식각할 수 있다는 장점 이 있다. Cu는 다양한 산화수를 가지고 있으므로 산화제 에 따라 Cu2O 및 CuO로 산화될 수 있는데 각각의 산화 제에 따른 Cu ALE 식각 반응 메커니즘은 아래와 같다.
- 산화제로 O2를 사용하는 경우,
- 산화제로 O3를 사용하는 경우,
- 3.3. 질화물의 thermal ALE
- GaN의 ALE는 불소화-리간드 교환 메커니즘에 의해 진 행된다. 아래 나타낸 바와 같이 먼저 XeF2를 이용하여 GaN 표면을 불소화시키고, 리간드 교환 반응을 통해 불화 물 층을 제거한다[21].
- GaN ALE는 다양한 온도에서 사이클 수에 따라 선형적 으로 두께가 변화함을 알 수 있는데 170°C에서 0.18 Å/ cycle, 300°C에서 0.72 Å/cycle의 식각 속도를 나타내며 온 도에 비례하여 식각 속도가 증가한다. 이는 온도가 높을수 록 XeF2에 의해 더 두꺼운 불화물 표면층이 형성되기 때 문이다. 이 불화물 층은 이후 BCl3와의 리간드 교환 반응 에 의해 제거된다.
- AlN의 thermal ALE 반응 메커니즘은 Al2O3 ALE 및 HfO2 ALE와 유사하다. 먼저 HF가 AlN 막을 불소화시키 고 표면에 AlF3 층을 생성한다[22]. 그런 다음 금속 전구 체인 Sn(acac)2는 AlF3 층에서 불소를 받아들이고 리간드 교환 반응에서 acac 리간드를 AlF3 층으로 전달한다. 이때 발생 가능한 휘발성 생성물은 SnF(acac) 및 Al(acac)3 또는 AlF(acac)2이다. AlN ALE 반응 사이클 수에 따라 AlN 두 께가 선형적으로 감소하며, 275°C에서 약 0.38 Å/cycle의 식각 속도가 확인되었다.
- Fig. 11은 AlN 박막의 thermal ALE와 Sn(acac)2 노출 후 (a) H2 또는 (b) Ar 플라즈마 노출을 추가한 plasmaenhanced ALE에 의한 식각 효과를 비교하여 보여준다. Thermal ALE AlN의 경우 식각속도가 약 0.36 Å/cycle임 을 알 수 있으나 H2 및 Ar 플라즈마 강화 thermal ALE의 경우 각각 1.96, 0.66 Å/cycle로 식각 속도가 크게 증가함 을 확인할 수 있다. 이는 H2 및 Ar 플라즈마가 표면 부위 를 차단하여 식각을 제한할 수 있는 acac 표면 종을 제거 하기 때문이다. 이러한 차단 종의 제거는 더 많은 HF가 표면을 불소화시키고, Sn(acac)2와 더 많은 리간드 교환을 할 수 있게 한다. 또한, H 라디칼의 재결합에 의해 방출된 열은 acac 표면 종의 탈착을 촉진할 수 있다.
- 불소화-리간드 교환 반응을 이용한 thermal ALE 공정은 TiN과 같은 일부 금속 질화물을 식각할 수 없다. TiN이 식 각되지 않는 이유로는 불소에 의해 TiN 표면은 산화수 +3 을 그대로 유지하여 TiF3로 불소화되는 특징을 가지기 때 문이다. 대부분의 안정적이며 높은 휘발성을 갖는 Ti 화합 물의 경우의 Ti 산화수는 +4이므로 TiF3에 대한 리간드 교 환 과정은 안정적이고 휘발성인 반응 생성물을 생성하지 않는다. 따라서 thermal TiN ALE에는 다른 접근 방식이 필요한데, 새로운 Thermal ALE 공정은 Fig. 12와 같이 산 화-불소화 반응으로 정의할 수 있다. 첫 번째 단계는 오존 노출로 TiN 기판에 산화티타늄(TiO2) 표면층이 생성되는 산화 반응이다[13].
- O3는 Ti의 산화 상태를 +3에서 +4로 전환할 수 있는 강 력한 산화제이며 O3는 안정적인 자기 부동 태화 TiO2 층 을 형성할 수 있다. TiO2층은 확산 장벽을 형성하여 추가 적인 산화를 방해하고 자기 제한적인 산화 반응을 일으킨 다. 이후 다음 단계에서 공급된 HF가 TiO2와 반응하여 휘 발성 TiF4 반응 생성물을 형성한다. TiF4 반응 생성물은 휘 발성이 높으므로 표면에서 제거된다. 이렇게 O3 및 HF 반 응을 반복하여 TiN 기판을 식각할 수 있다. TiN ALE의 반응 메커니즘을 정리하면 아래 식과 같다.
- TiN ALE 반응에서 식각 속도는 사용하는 산화제에 따 라 달라질 수 있다. Fig. 13는 식각 온도 250°C에서 O3/HF 를 반응물로 사용하는 ALE TiN과 H2O2/HF를 반응물로 사용하는 ALE TiN의 사이클 후의 TiN 박막 두께 변화를 보여준다. 산화제 가스와 관계없이 ALE 사이클 수에 따 라 필름 두께가 선형적으로 감소함을 알 수 있으며 O3/HF 를 이용한 ALE TiN의 경우 SE 측정 결과 0.19 Å/cycle의 식각 속도를 나타내었다. 반면 O3 보다 약한 산화제인 H2O2를 사용한 ALE TiN 공정의 경우 같은 온도에서 0.15 Å/cycle의 식각 속도를 나타내었다. O3와 H2O2를 각각 반 응물로 이용했을 때의 식각 속도를 비교하여 보면, 산화력 이 클수록 식각 속도가 더 높음을 알 수 있다. O3/HF와 H2O2/HF의 경우 모두 ALE TiN의 반응은 자기 제한적 포 화 곡선을 나타내었으나 H2O2를 이용한 ALE TiN의 경우 H2O2의 공정 중 농도 변화로 인해 재현 가능한 결과를 얻 는 것이 어려웠고, H2O2/H2O 노출 후 과도한 H2O를 퍼지 하는 것이 어려운 단점이 있음을 알 수 있다. 또한, 고온 공정 시 H2O2의 열분해가 있을 수 있으므로 고온 공정이 제한 된다는 특징이 있다. 이러한 점들로 비추어 볼 때, TiN ALE의 산화제로서 O3가 H2O2보다 더 적합하다고 판 단할 수 있다.
- Si3N4의 ALE는 산화-전환 식각 메커니즘을 기반으로 한 다. 먼저 O2 또는 O3를 산화제로 사용하여 Si3N4를 SiO2 로 산화시키고, 산화되어 표면에 생성된 SiO2 층에 TMA 를 공급하여 Al2O3 또는 규산 알루미늄으로 전환한다. 이 후 공급된 HF는 알루미늄을 불소화하여 AlF3 또는 AlFxOy를 생성하게 되고 불화 알루미늄층은 TMA와 리간 드 교환 반응을 통해 휘발성의 AlF(CH3)2 생성물을 형성 하여 식각되는 원리를 가지고 있다. 이러한 메커니즘의 모 식도를 Fig. 14에 나타내었다[11].
- 앞서 언급하였던 ALE 공정과 마찬가지로 Si3N4 ALE 반응은 공정 온도에 영향을 받아 식각 속도가 변화하며, 산화-전환 식각 메커니즘에 의한 반응이므로 사용되는 산 화제에 따라 식각 속도를 조절할 수 있는 특징을 가지고 있다. Si3N4의 ALE는 관찰된 모든 온도에서 선형적인 식 각 거동을 보이며 210°C에서 약 0.07 Å/cycle, 290°C에서 0.47 Å/cycle의 식각 속도를 나타내었다. 한편 Fig. 15 (a) 와 (b)에서 확인할 수 있듯이, 사용된 산화제가 O2 또는 O3에 따라서 각각 0.25 및 0.47 Å/cycle의 식각 속도가 관 찰되었다. 즉 산화력이 더 클수록 표면에 형성된 SiO2 산 화막 두께가 증가하고 이를 휘발성 부산물의 형태로 제거 하게 됨에 따라 식각 속도가 높아진다는 것을 확인할 수 있다.
3. 산화물, 금속, 질화물의 열 원자층 식각 공정
3.1.1. Al2O3 ALE
Fig. 3
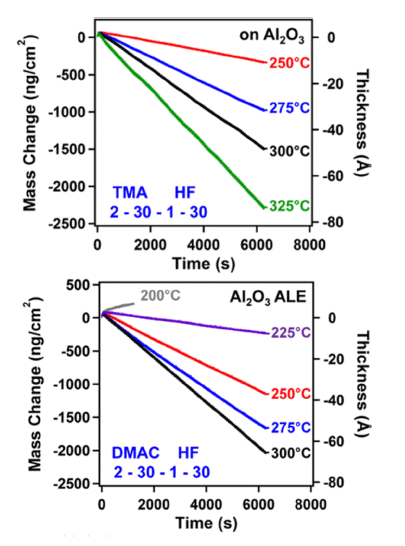
(a) (top) Mass change versus time for Al2O3 ALE using sequential TMA and HF exposures at 250, 275, 300 and 325°C [9]. (b) (bottom) Mass change versus time for Al2O3 ALE using sequential DMAC and HF exposures at 200, 225, 250, 275 and 300°C [17].

Fig. 4
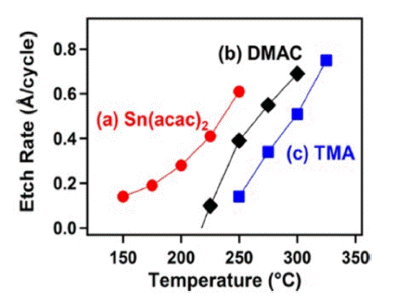
Etch rates of Al2O3 at different temperatures using (a) Sn(acac)2 (1−30−1−30), (b) DMAC (2-30-1-30) and (c) TMA (2-30-1-30) as the metal precursor [8].

3.1.2. HfO2 ALE
Fig. 5
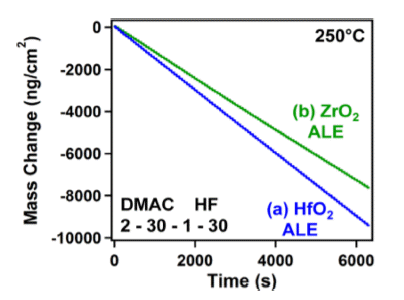
Mass change versus time during 100 cycles of: (a) HfO2 ALE and (b) ZrO2 ALE at 250°C using the reaction sequence of 2−30−1−30 [17].

3.1.3. ZrO2 ALE
Fig. 7
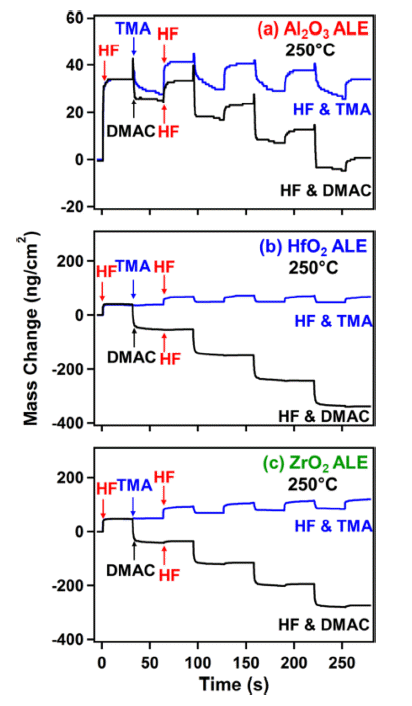
Comparison of mass changes versus time during four sequential exposures of HF and TMA or HF and DMAC on: (a) Al2O3; (b) HfO2; and (c) ZrO2 at 250°C using the reaction sequence of 2−30−1−30 [17].

3.1.4. SiO2 ALE
Fig. 8
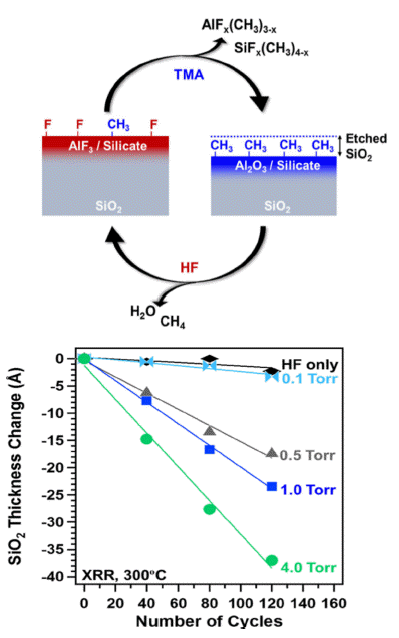
(a) (Top) Schematic of the proposed reaction mechanism for SiO2 ALE showing the sequential TMA and HF reactions [16]. (b) (bottom) SiO2 film thickness change versus number of SiO2 ALE cycles determined by XRR at TMA/HF pressures of 0.1, 0.5, 1.0, and 4.0 Torr [10].

3.1.5. ZnO ALE
Fig. 9
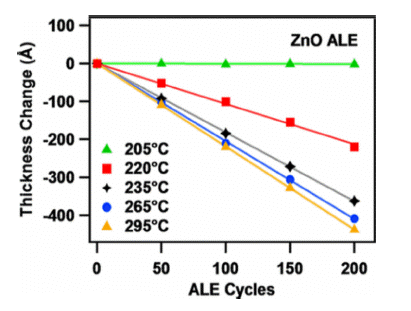
Spectroscopic ellipsometry measurements of the thickness change of the ZnO film versus number of ZnO ALE cycles at a variety of temperatures between 205 and 295°C [19].

3.2.1. W ALE
Fig. 10
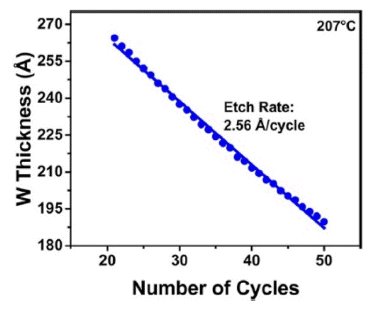
W thickness versus number of cycles during W ALE at 207°C using O2/O3, BCl3, and HF as reactants. Etch rate during W ALE is 2.56 Å/cycle [12].

3.2.2. Cu ALE
3.3.1. GaN ALE
3.3.2. AlN ALE
Fig. 11
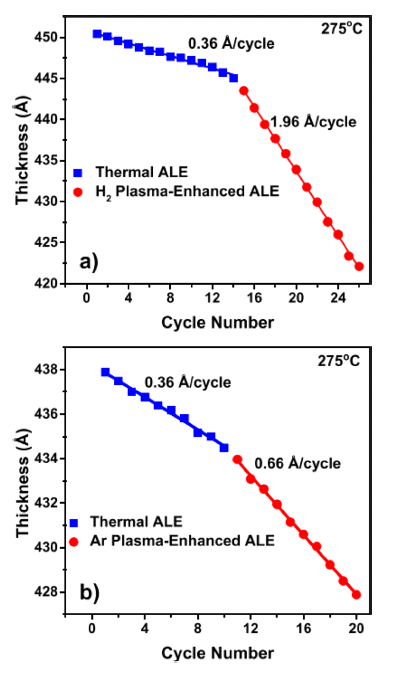
Film thickness vs number of AlN ALE reaction cycles at 275°C in pure AlN region of AlN film showing results for thermal AlN ALE and plasma-enhanced ALE. (a) H2 plasma increases AlN etch rate from 0.36 to 1.96 Å/cycle. (b) Ar plasma increases AlN etch rate from 0.36 to 0.66 Å/ cycle [22].

3.3.3. TiN ALE
Fig. 12
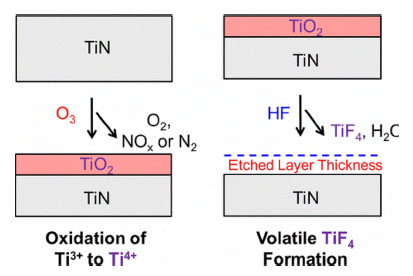
Schematic for TiN ALE using O3 and HF as the reactants. O3 oxidizes the TiN substrate to form a TiO2 layer on the surface. Subsequently, HF removes the TiO2 layer by forming volatile TiF4 and H2O reaction products [13].

Fig. 13
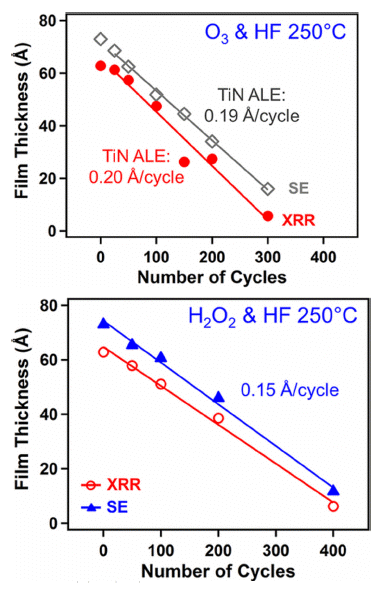
(a) (top) X-ray reflectivity and spectroscopic ellipsometry measurements of TiN film thickness versus number of O3 and HF reaction cycles at 250°C [13]. (b) (bottom) Xray reflectivity and spectroscopic ellipsometry measurements of TiN film thickness versus number of H2O2 and HF reaction cycles at 250°C [13].

3.3.4. Si3N4 ALE
Fig. 14
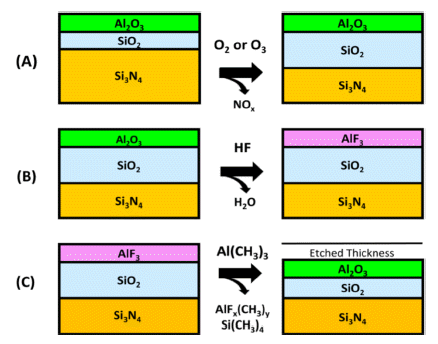
Schematic for thermal Si3N4 ALE based on (a) oxidation by O2 or O3; (b) fluorination by HF; and (c) ligand-exchange and conversion with Al(CH3)3 [11].

Fig. 15
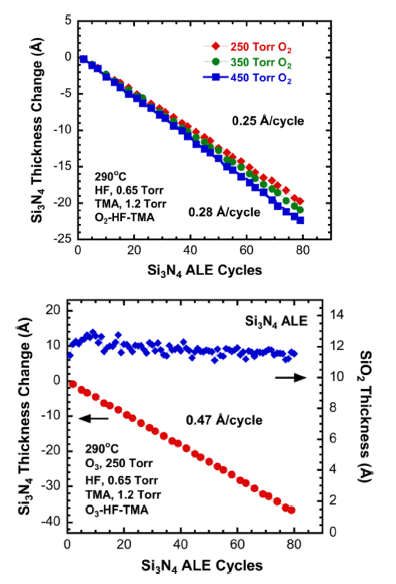
(a) (top) Si3N4 thickness change and SiO2 film thickness vs number of ALE cycles during Si3N4 etching using O2-HF-TMA reactant sequence at 290°C. (b) (bottom) Si3N4 thickness change and SiO2 film thickness vs number of ALE cycles during Si3N4 etching using O3-HF-TMA reactant sequence at 290°C [11].

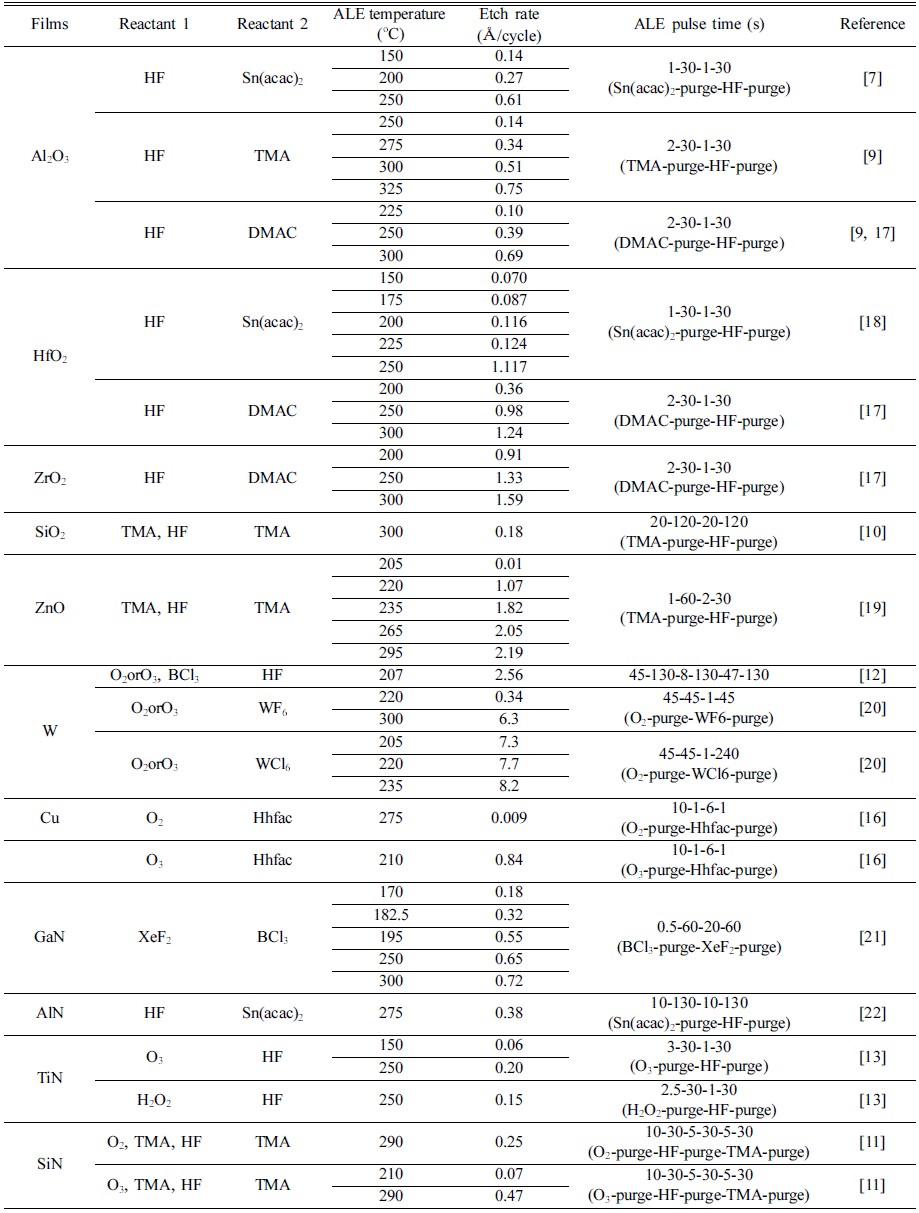
- 본 논문에서는 ALE의 원리 및 다양한 반응메커니즘과, ALE를 이용한 다양한 산화물, 금속, 질화물의 thermal ALE 결과를 연구하였다. Table 1에 정리된 바와 같이 반 도체 산업에서 주로 쓰이는 다양한 산화물, 질화물, 금속 의 ALE 반응을 통한 식각이 가능하며 이러한 물질들은 일반적으로 불소화-리간드 교환 반응, 전환-불소화 반응, 산화-불소화 반응과 같은 메커니즘을 통해 thermal ALE가 진행됨을 알 수 있다. Al2O3, HfO2, ZrO2, GaN, AlN 물질 은 주로 불소화-리간드 교환 반응을 통해 식각되며, ZnO 와 SiO2는 전환-불소화 반응을 통해 ALE 반응이 일어난 다. 또한 금속 및 질화물 박막인 W, Cu, SiN, TiN 물질에 서는 산화-불소화 반응 또는 산화-리간드 교환 반응으로 ALE가 진행된다. 이러한 반응에는 HF, Sn(acac)2, TMA, DMAC, O2, O3, 등 다양한 물질이 반응물로 사용할 수 있다.
- Thermal ALE는 고에너지 이온을 사용하지 않아, RIE 및 Plasma ALE의 단점인 표면 격자 손상 및 전하 결함을 방지해 소자의 신뢰성을 향상시킬 수 있다. 또한, 원자층 단위의 자기 제한적 반응을 통해 균일하고 평평한 표면을 얻을 수 있으며, 3D 구조에서의 정밀한 측면 식각이 가능 함이 입증되었지만 ALE의 낮은 식각 속도 등은 해결해야 할 과제로 남아있다. 이는 반응물 및 부산물에 대한 퍼지 속도와 종횡비 소자의 구조에 따른 반응물의 접근성 등의 어려움을 해결해야만 극복할 수 있을 것으로 보인다.
- 그럼에도 불구하고 thermal ALE기술은 반도체 소자의 미세화를 달성하기 위해 일부 공정에서 반드시 필요한 식 각법으로 RIE를 일부 대체할 수있을 것으로 기대되고 있 다. ALE를 통해 정밀한 공정 제어와 선택적 식각이 가능 하여 원자 수준에 가까운 두께 제어 및 선택비를 필요로 하는 초박형 게이트 유전체, 초박형 채널, FinFET 및 Gate-All-Around CMOS와 같은 새로운 전계 효과 트랜지 스터(FET) 구조 구현에 적절할 것이다. 반도체 소자 뿐 아 니라 마이크로일렉트로닉스, 광전자공학, MEMS(Micro- Electro-Mechanical Systems) 산업에 활용될 수 있을 것으 로 보인다.
4. 결 론
-
Acknowledgements
- 이 연구는 서울과학기술대학교 교내 연구비의 지원으로 수행되었습니다.
감사의 글
- 1. K. Eriguchi and K. Ono: J. Phys. D: Appl. Phys., 41 (2008) 024002..Article
- 2. T. Ivanovm, M. A. Porghaderi, D. Lin, J.-K. Yu, S. Tan, Y. Kimura, D. Hellin, J. Geypen, H. Bender, J. Vertommen, G. Kamarthy, N. Collaert, J. Marks, V. Vahedi, R. Arghavani and A. Thean: Jpn. J. Appl. Phys., 53 (2014) 04EC20..Article
- 3. K. Nojiri: Dry Etching Technology for Semiconductors, Springer International Publishing, (2015)..Article
- 4. K. J. Kanarik, S. Tan and R. A. Gottscho: J. Phys. Chem. Lett., 9 (2018) 4814..ArticlePubMed
- 5. C. Fang, Y. Cao, D. Wu and A. Li: Prog. Nat. Sci., 28 (2018) 667..Article
- 6. A. Fischer, A. Routzahn, S. M. George and T. Lill: J. Vac. Sci. Technol. A, 39 (2021) 030801..Article
- 7. Y. Lee, J. W. DuMont and S. M. George: Chem. Mater., 27 (2015) 3648..Article
- 8. Y. Lee, C. Huffman and S. M. George: Chem. Mater., 28 (2016) 7657..Article
- 9. Y. Lee, J. W. DuMont and S. M. George: Chem. Mater., 28 (2016) 2994..Article
- 10. J. W. DuMont, A. E. Marquardt, A. M. Cano and S. M. George: ACS Appl. Mater. Interfaces, 9 (2017) 10296..ArticlePubMed
- 11. A. I. Abdulagatov and S. M. George: J. Vac. Sci. Technol. A, 38 (2020) 022607..Article
- 12. N. R. Johnson and S. M. George: ACS Appl. Mater. Interfaces, 9 (2017) 34435..ArticlePubMed
- 13. Y. Lee and S. M. George: Chem. Mater., 29 (2017) 8202..Article
- 14. S. M. George: Acc. Chem. Res., 53 (2020) 1151..ArticlePubMed
- 15. A. I. Abdulagatov and S. M. George: Chem. Mater., 30 (2018) 8465..Article
- 16. E. Mohimi, X. I. Chu, B. B. Trinh and J. R. Abelson: ECS J. Solid State Sci. Technol., 7 (2018) P491..Article
- 17. Y. Lee and S. M. George: J. Phys. Chem. C, 123 (2019) 18455..Article
- 18. Y. Lee, J. W. DuMont and S. M. George: ECS J. Solid State Sci. Technol., 4 (2015) N5013..Article
- 19. D. R. Zywotko and S. M. George: Chem. Mater., 29 (2017) 1183..Article
- 20. W. X ie a nd G. N . P arsons: J . Vac. Sci. Technol. A, 38 (2020) 022605..Article
- 21. N. R. Johnson, J. K. Hite, M. A. Mastro, C. R. Eddy Jr and S. M. George: Appl. Phys. Lett., 114 (2019) 243103..Article
- 22. N. R. Johnson, H. Sun and K. Sharma: J. Vac. Sci. Technol. A, 34 (2016) 050603..Article
Figure & Data
References
Citations
Citations to this article as recorded by 

- Atomic Layer Etching for Extreme Manufacturing: Pushing the Limits of Atomic Scale Precision
Yuqun Feng, Bowen Sun, Fan Yang, Kun Cao, Yuan Gao, Bin Shan, Fred Roozeboom, Rong Chen
Nanomanufacturing and Metrology.2026;[Epub] CrossRef - Self-Assembled Monolayers in Area-Selective Atomic Layer Deposition and Their Challenges
Si Eun Jung, Ji Woong Shin, Ye Jin Han, Byung Joon Choi
Journal of Powder Materials.2025; 32(3): 179. CrossRef
Thermal Atomic Layer Etching of the Thin Films: A Review
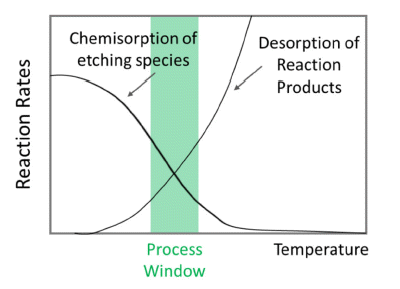
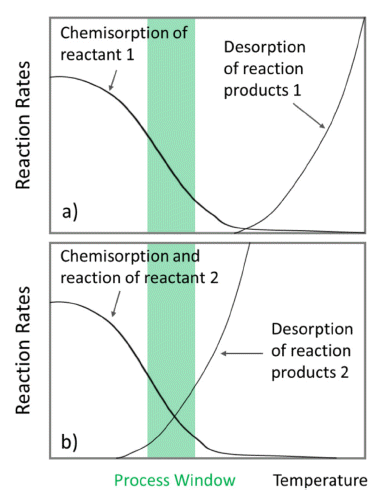
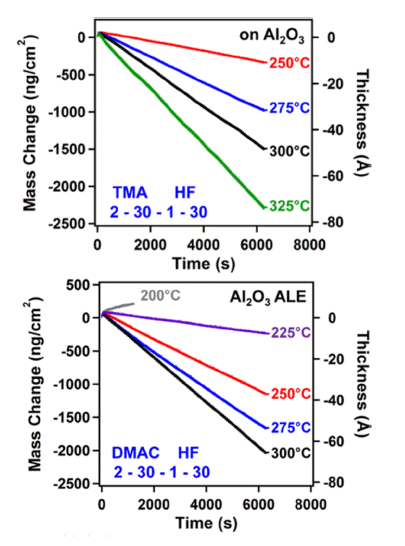
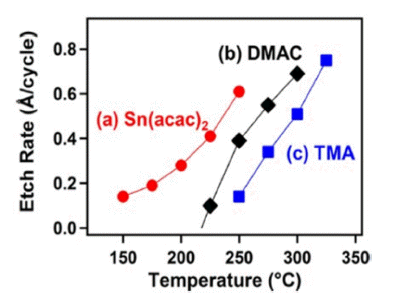
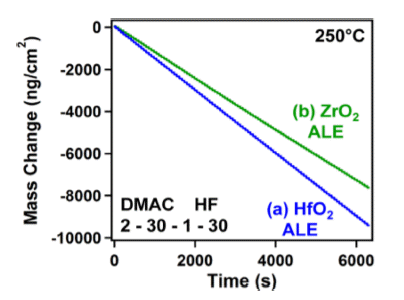
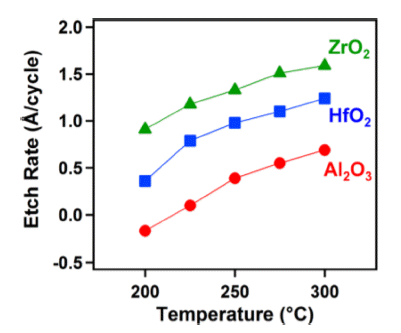
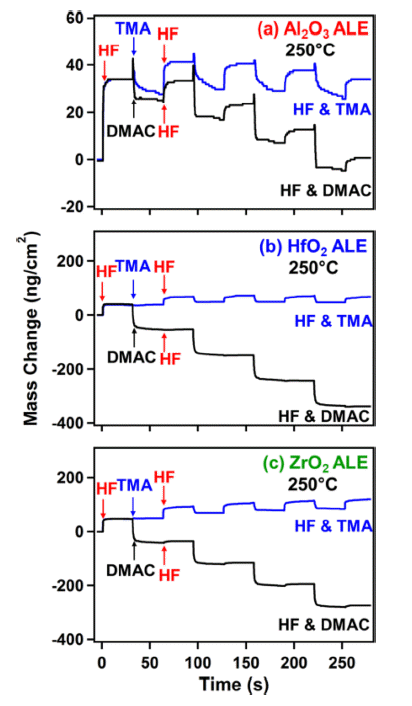
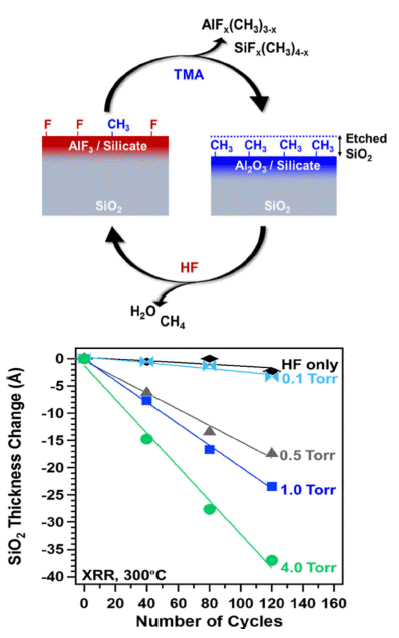
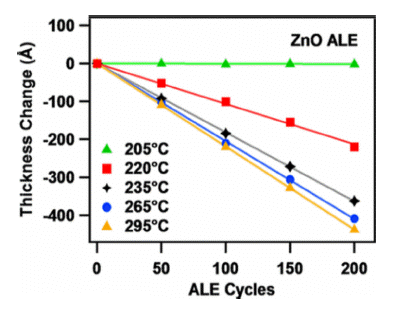
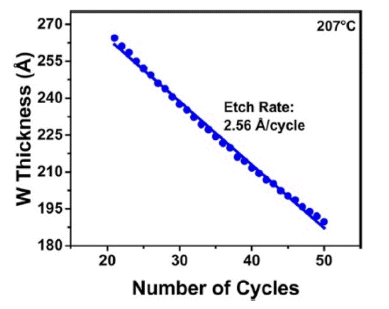
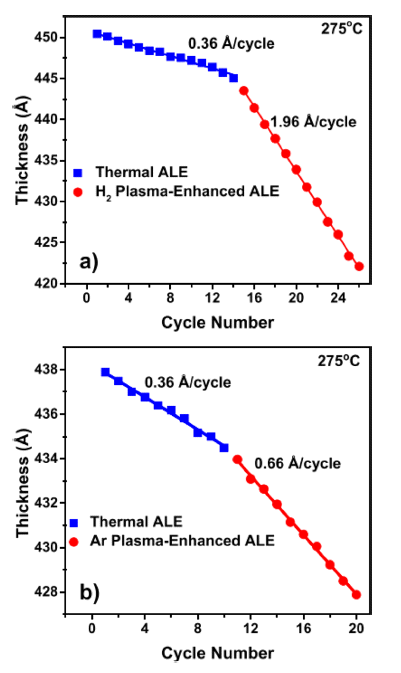
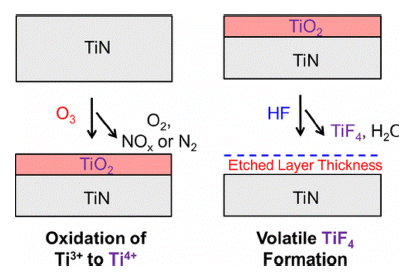
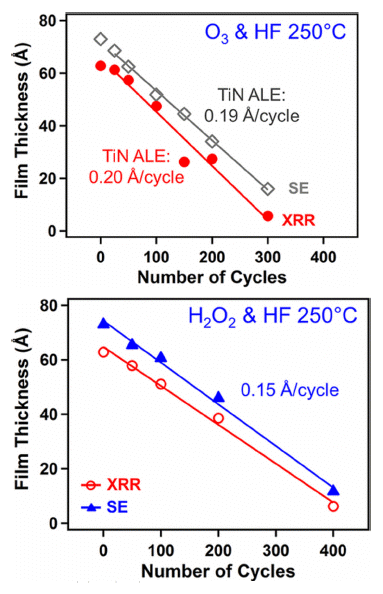
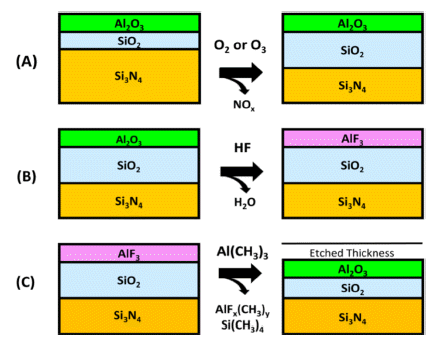
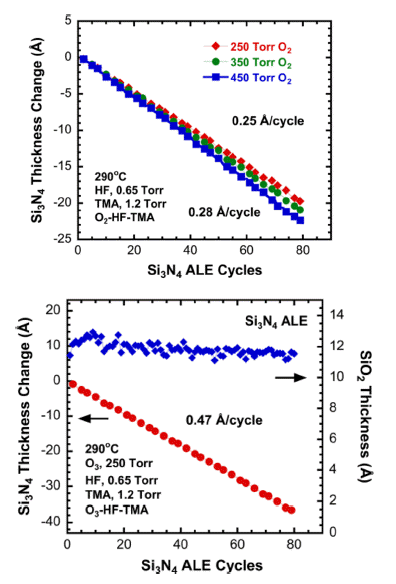
Fig. 1
Schematic illustration of the temperature process window for thermal etching [6].
Fig. 2
Schematic illustration of the temperature process window for thermal isotropic ALE at constant temperature. Panel (a) shows the chemisorption of a reactant 1 without initiating etching representing a modification step in thermal ALE. In panel (b), this modified surface is exposed to a reactant 2, which results in a surface layer that desorbs at the given wafer temperature resulting in etching of the modified layer [6].
Fig. 3
(a) (top) Mass change versus time for Al2O3 ALE using sequential TMA and HF exposures at 250, 275, 300 and 325°C [9]. (b) (bottom) Mass change versus time for Al2O3 ALE using sequential DMAC and HF exposures at 200, 225, 250, 275 and 300°C [17].
Fig. 4
Etch rates of Al2O3 at different temperatures using (a) Sn(acac)2 (1−30−1−30), (b) DMAC (2-30-1-30) and (c) TMA (2-30-1-30) as the metal precursor [8].
Fig. 5
Mass change versus time during 100 cycles of: (a) HfO2 ALE and (b) ZrO2 ALE at 250°C using the reaction sequence of 2−30−1−30 [17].
Fig. 6
Etch rates for Al2O3, HfO2, and ZrO2 ALE at different temperatures using DMAC and HF [17].
Fig. 7
Comparison of mass changes versus time during four sequential exposures of HF and TMA or HF and DMAC on: (a) Al2O3; (b) HfO2; and (c) ZrO2 at 250°C using the reaction sequence of 2−30−1−30 [17].
Fig. 8
(a) (Top) Schematic of the proposed reaction mechanism for SiO2 ALE showing the sequential TMA and HF reactions [16]. (b) (bottom) SiO2 film thickness change versus number of SiO2 ALE cycles determined by XRR at TMA/HF pressures of 0.1, 0.5, 1.0, and 4.0 Torr [10].
Fig. 9
Spectroscopic ellipsometry measurements of the thickness change of the ZnO film versus number of ZnO ALE cycles at a variety of temperatures between 205 and 295°C [19].
Fig. 10
W thickness versus number of cycles during W ALE at 207°C using O2/O3, BCl3, and HF as reactants. Etch rate during W ALE is 2.56 Å/cycle [12].
Fig. 11
Film thickness vs number of AlN ALE reaction cycles at 275°C in pure AlN region of AlN film showing results for thermal AlN ALE and plasma-enhanced ALE. (a) H2 plasma increases AlN etch rate from 0.36 to 1.96 Å/cycle. (b) Ar plasma increases AlN etch rate from 0.36 to 0.66 Å/ cycle [22].
Fig. 12
Schematic for TiN ALE using O3 and HF as the reactants. O3 oxidizes the TiN substrate to form a TiO2 layer on the surface. Subsequently, HF removes the TiO2 layer by forming volatile TiF4 and H2O reaction products [13].
Fig. 13
(a) (top) X-ray reflectivity and spectroscopic ellipsometry measurements of TiN film thickness versus number of O3 and HF reaction cycles at 250°C [13]. (b) (bottom) Xray reflectivity and spectroscopic ellipsometry measurements of TiN film thickness versus number of H2O2 and HF reaction cycles at 250°C [13].
Fig. 14
Schematic for thermal Si3N4 ALE based on (a) oxidation by O2 or O3; (b) fluorination by HF; and (c) ligand-exchange and conversion with Al(CH3)3 [11].
Fig. 15
(a) (top) Si3N4 thickness change and SiO2 film thickness vs number of ALE cycles during Si3N4 etching using O2-HF-TMA reactant sequence at 290°C. (b) (bottom) Si3N4 thickness change and SiO2 film thickness vs number of ALE cycles during Si3N4 etching using O3-HF-TMA reactant sequence at 290°C [11].
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Fig. 7
Fig. 8
Fig. 9
Fig. 10
Fig. 11
Fig. 12
Fig. 13
Fig. 14
Fig. 15
Thermal Atomic Layer Etching of the Thin Films: A Review
Table 1
Thermal ALE of the various thin films from literatures
Table 1
TOP
 KPMI
KPMI

 Cite this Article
Cite this Article