Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 23(6); 2016 > Article
-
ARTICLE
P/M Fecralloy의 성형성 및 전기저항특성 향상에 관한 연구 - 박진우a, 고병현a, 정우영a, 박동규c, 안인섭a,b,*
- A Study on the Development of Compactability and Electrical Resistivity for P/M Fecralloy
- Jin-Woo Parkaa, Byung-Hyun Koa, Woo-Young Junga, Dong-Kyu Parkc, In-Shup Ahna,b,*
-
Journal of Korean Powder Metallurgy Institute 2016;23(6):426-431.
DOI: https://doi.org/10.4150/KPMI.2016.23.6.426
Published online: November 30, 2016
a 경상대학교 나노 신소재 공학부
b 항공기부품 기술연구소
c 경상대학교 링크 사업단
a School of Nano and Advanced Materials Science & Engineering
b ReCAPT
c LINC, Gyeongsang National University, Jinju, Gyeongnam 52828, Korea
- *Corresponding author : In-Shup Ahn, +82-55-772-1662, +82-55-772-1670, ais@gsnu.ac.kr
• Received: October 7, 2016 • Revised: December 15, 2016 • Accepted: December 18, 2016
© The Korean Powder Metallurgy Institute. All rights reserved.
- 734 Views
- 2 Download
Abstract
- The Fe-Cr-Al alloy system shows an excellent heat resistance because of the formation of an Al2O3 film on the metal surface in an oxidizing atmosphere at high temperatures up to 1400°C. The Fecralloy needs an additive that can act as a binder because of its bad compactability. In this study, the green compacts of STS434L and Al powder added to Fecralloy are oxidized at 950°C for up to 210 h. Fecralloy and Al is mixed by two types of ball milling. One is vented to air and the other was performed in a sealed jar. In the case of Al addition, there are no significant changes in the electrical resistance. Before the oxidation test, Al oxides are present in the Fecralloy surface, as determined from the energy dispersive spectroscopy results. The addition of Al improves the compactability because of an increased density, and the addition of STS434L increases the electrical resistivity by forming a composite oxide.
- Fecralloy는 Fe-Cr-Al 합금계로서 일반적으로 많이 사용 되고 있는 고온 저항 발열체이며 내산화성과 부식저항성 이 뛰어나고 최고 사용온도가 1450°C에 이르러 고온안정 성이 매우 좋은 장점이 있다. 또한 금속표면에 Al2O3 보호 피막층을 형성하기 위하여 17% 이상의 높은 Al 함량을 필요로 하는 Fe-Al 계 합금과는 달리 Fe-Cr-Al계 Fecralloy 는 5% 정도의 낮은 Al 함량만으로 보호성 Al2O3 피막층 을 형성하는 데, 그 이유는 Cr이 합금 내에서 산소에 대한 제 2 흡수제의 역할을 하여 내부산화를 효과적으로 억제 하고 표면 쪽으로 확산한 Al이 산소와 반응하여 Al2O3를 형성시키기 때문인 것으로 알려져 있다[1, 2]. 고온에서도 내산화성을 유지하고 고저항, 낮은 열팽창 계수를 충족시 키며, Al을 첨가하여 Al2O3 피막을 형성시켜 내열성의 향 상과 함께 내식성을 확보케 한다. 산화수명은 보호성 산화 피막과 금속기지가 분리되지 않고 결합되어 있는 시간에 의존하는데 산화수명을 증가시키기 위해서 희토류 원소 Y, La, Ce, Hf, Sc 등의 첨가나 Cr, Al 함량의 증가 등이 시 도되고 있다. 또한 내열성 및 내식성 향상에 중요한 피막 과 기지와의 밀착성을 향상시키기 위해 Y, Zr, Ti, Mn, Nb 등을 첨가하기도 한다[3]. 이들 원소들은 기지 안에 안정한 입자를 형성함으로써 고온에서 재결정을 억제하며 뛰어난 고온 가공성과 내열성을 갖게 한다. 희토류 원소를 첨가한 Fe-Cr-Al 합금의 경우 산소가 산화층을 투과하는 내부 확 산에 의해 산화층이 성장한다고 보고되고 있다[4, 5]. 즉, 산화반응은 금속과 산화층의 계면에서 일어나며 계면이 기 지금속 방향으로 진행된다. 성장된 계면은 외부로부터 산 소의 내부 확산속도를 점차 감소시키며 산화반응은 산소 및 Al의 확산에 의해서 진행되기 때문에 산화층의 두께가 증가할수록 이온의 이동거리도 증가되어 포물선 형태로 증가하게 된다[6-8].
- 고온 발열체는 고온내산화성이 우수하여야 하며, 고온 에서 높은 전기저항이 요구된다. 또한 고온에서 장시간 사 용하여도 내산화성이나 전기저항이 감소되지 않는 안정성 이 유지되어야 한다. 그러나 분말야금제품은 주조법으로 만들어진 소재보다 많은 기공 구조를 가지며 이러한 넓은 기공면적이 galvanic couple을 형성하여 부식을 촉진시키 는 원인이 된다[9, 10]. 또한 고온에서 기공의 형상변화에 의해 산화저항 및 전기저항의 변화가 발생하며, 다양한 산 화물상이 생성될 뿐만 아니라 소재표면과 개기공 표면에 생성되는 산화피막의 종류와 분포형태 등에 따라서 산화 안정성 및 전기저항특성의 안정성이 크게 달라진다[11]. 따라서 분말야금법을 고온발열체 제조에 응용할 경우 고 려되어야 할 많은 문제점들을 가지고 있으나 아직까지 이 에 대한 연구는 거의 수행된 바가 없는 실정이다. 특히 Fecralloy는 표면에 형성된 산화피막으로 인해 고온에서 내산화성은 크게 증가할 것으로 기대되지만 분말성형 및 소결성이 나쁘고 높은 전기저항 때문에 고온발열체로 사 용이 어려울 것으로 사료된다. 따라서 고온에서 내산화성 을 유지하면서 분말 성형성을 증가시키고 안정화된 고온 전기저항특성을 얻기 위해서는 금속분말과 혼합된 Fecralloy를 사용할 필요가 있다. 혼합되는 금속분말은 고 온에서 내식성이 양호한 표면에 보호성 산화막이 잘 형성 되어 고온 분위기에서 사용될 때 표면을 보호할 수 있는 분말이어야 하며, 산화피막이 안정하여 잘 깨지지 않으며 Fecralloy분말과도 결합특성이 좋아야한다[9, 12]. 대표적 인 금속으로 Si과 Al이 있는데, Si의 경우는 경도가 높고 인성이 없어 Fecralloy의 성형성 향상에는 크게 도움이 되 지 않을 것으로 사료된다. 반면 Al은 연성도 있고 공기중 에서 쉽게 산화가 되며 산화물은 안정한 고온 내식특성을 가지며[3] 특히 Fecralloy의 표면층에 형성되는 알루미나 층과 쉽게 결합할 수 있는 원소이다. 따라서 본 연구에서 는 분말성형성이 떨어지는 Fecralloy의 내산화성과 고온 전기저항특성은 감소시키지 않으면서 성형성을 향상시키 고자 Al 분말과 Fecralloy 분말을 혼합하되 대기분위기하 에서 볼밀링하면서 Al분말 표면 또는 내부에 산화물층을 in-situ 로 형성시키면서 Fecralloy와 복합분말을 형성시켜 성형한 후 950°C의 대기 중에서 성형체의 고온 내산화성 과 전기저항 특성을 조사하였다. 또한 STS434L 분말을 혼 합한 경우와 비교하여 성형성 및 고온 내산화성과 전기저 항특성에 미치는 영향을 조사하였다.
서 론
- 그림 1과 같이 본 연구에 사용된 Fecralloy 분말은 평균 입도가 30 um 인 구형의 Sandvik Osprey Ltd 사(영국)의 제품이고, Al 분말은 평균입도가 30 um 인 KOJUNDO Chemical Laboratory CO., LTD 사(일본)의 제품이며, STS; stainless steel(Korea Standard) 434L 분말은 평균입 도가 40 um 불규칙형상의 Daido 사(일본)의 제품이다.
- Fecralloy분말은 Al분말 10 wt.%(23 vol.%)와 혼합한 후 직경 10 mm ball 200 g과 혼합분말 100 g을 200 rpm으로 100시간 동안 볼밀링하여 사용하였다. 볼밀링 할 때에는 공기를 유입한 상태에서 밀링한 시편과 공기유입을 차단 한 상태로 볼밀링하여 Al산화물의 형성에 따른 성형성 및 고온 전기저항특성을 비교분석하였다. 또한 비교시편으로 Fecralloy에 434L분말을 25 wt.%(23.5 vol.%) 혼합한 분말 을 사용하였다. -
- 혼합한 분말은 유압식 성형프레스를 이용하여 7.5 ton/ cm2 압력으로 50 × 4 × 4 mm의 크기를 가지는 bar 형태의 성형체를 제조하였다. 성형한 시편의 산화 시간에 따른 고 온 산화 거동 및 전기적 특성을 알아보기 위해서 대기상 태의 950°C에서 210시간 동안 산화시켜 산화시간에 따른 산화 거동을 조사하였다. 시간에 따른 산화실험공정을 그 림 2에 나타내었고 승온시간 30°C/min 으로 300°C까지 가 열하여 10분 예열을 한 다음, 승온시간 15°C/min으로 목 표 온도까지 가열해 주었다. 시편은 각 시간대별로 로에서 꺼내어 공냉을 실시하였으며, 시편의 무게변화율을 측정하 였다. 또한 고온 산화 시험 후 생성된 산화물들의 상변화를 X-선 회절기(X-ray diffraction meter)를 이용하여 조사하였고 성분분석을 위해 EDS(Energy Dispersive Spectroscopy) 측정 하였다. 또한 고온에서의 산화시간에 따른 전기저항을 측정 하였다. 전기저항은 Hioki 3540 모델의 전기저항 측정장치를 이용하여 측정하였으며 표면 접촉저항을 최소화하기 위하여 표면 연삭 후 silver paste를 시편에 바르고 측정하였다.
실험방법
Table 1
Composition of the used powder(wt.%).
| C | Cr | Al | Mo | Si | Mn | Y | Fe | |
|---|---|---|---|---|---|---|---|---|
|
|
||||||||
| 434L | 0.01 | 16.73 | - | 1.09 | 0.8 | 0.17 | - | Bal |
| Fecraloy | 0.1 | 22.3 | 6.6 | - | - | 1 | 0.2 | Bal |
- 그림 3은 Fecralloy 성형체와 Fecralloy에 STS434L 및 Al분말을 혼합하여 제조된 성형체를 950°C에서 210시간 까지 산화시킨 시간에 따른 산화물 증가량을 보여주는 그 래프로 모든 경우에서 무게변화율이 산화시간에 따라 점 진적으로 증가하였다. 모든 경우에 10시간 까지 무게증가 율이 높았는데, 이는 금속입자 표면에 보호 산화피막을 형 성시켜 초기 산화 시 무게 증량을 증가시켰기 때문이다 [12]. 산화반응은 산소 및 Al 확산에 의해서 진행되기 때 문에 산화층의 두께가 증가할수록 이온의 이동거리도 증가 하여 포물선 형태를 보이면서 증가한 것으로 생각된다. Al을 첨가한 경우 무게증가율이 Fecralloy나 Fecralloy+STS434L 경우보다 산화시간이 길어짐에 따라 좀더 많이 증가하였다. 특히 Fecralloy 보다는 2배 이상 큰 폭으로 증가함을 볼 수 있다. 산화에 의한 무게증가율은 성형체의 밀도에 의해서 도 크게 좌우되기 때문에 밀도의 변화와 연계하여 해석이 되어야 할 것이다.
- 또한 밀폐시킨 상태로 Al과 Fecralloy를 혼합하여 볼밀 링한 시편의 경우가 공기유입을 시킨 상태에서 볼밀링한 시편보다 다소 많은 산화량이 나타났는데 이는 볼밀링 시 산소유입으로 Al분말이 이미 충분히 표면 산화되어 상대 적으로 산화될 수 있는 면적이 적어졌기 때문인 것으로 사료된다.
- 그림 4는 산화시간에 따른 밀도변화를 보여주는 그래프 로 Fecralloy에 434L 첨가로 초기의 밀도가 73%에서 75% 정도로 증가하였으나 성형성을 크게 개선할 수는 없었다. Fecralloy 및 Fecralloy+STS434L인 경우는 산화시간에 따 라 밀도변화가 유사하였으며 Al을 첨가한 Fecralloy의 경 우는 이들 시편보다 초기 밀도가 다소 높게 나타났다. 따 라서 Fecralloy+Al 시편의 경우 산화량이 크게 증가한 것 은 밀도의 영향보다는 혼합분말 자체의 내부산화에 의한 영향인 것으로 판단된다. 즉, 950°C의 고온에서 산화시험 초기에 용융된 Al의 지속적인 산화과정에 의한 무게증가 인 것으로 사료된다.
- Fecralloy는 선행연구결과에서 보여주듯이 상대밀도가 비슷하더라도 산화시간 30시간 이후에 Fecralloy표면에 안 정한 산화보호피막이 형성되면서 낮은 무게증가율을 나타 낸다[13]. 반면에, Al이 혼합성형체인 경우는 초기밀도는 물론 산화시간이 길어지면서 높은 상대밀도를 보여주었는 데도 산화량이 더 많이 증가 하는 것은 Al과 Fecralloy 계 면 또는 입계에 용융상태로 networking 된 Al이 기지내로 철이나 크롬 등의 합금원소의 확산이동에 의한 지속적인 산화 때문인 것으로 사료되어 이에 대한 분석이 필요하다 고 생각된다.
- 그림 5는 대기 중의 950°C에서 210시간까지 산화시험을 진행한 후 각 성형체의 산화시간에 따른 X선 회절패턴을 보여주는 그림이다. 그림 5 (a), (c) 그리고 (d)에서 보면 210시간 산화되는 동안 Al2O3 피크가 명확해지는 것을 확 인할 수 있었다. 이외에 Fe 계열의 산화물은 발견되지 않 았으며, 이는 함유된 Y가 산화물의 박리를 억제하고 안정 한 Al2O3 산화물을 형성시켜 연속적인 산화피막이 만들어 진 것으로 예측된다[3]. Al을 첨가한 Fecralloy의 경우는 앞 의 두 시편보다는 다소 강한 알루미나 피크가 나타났다. 특 히 공기유입을 시킨 상태로 Al과 Fecralloy를 혼합하여 볼 밀링한 시편의 경우 더 강한 알루미나 피크가 관찰되었는 데 이는 볼밀링 시 산소유입으로 Al분말이 충분히 산화되 어 알루미나/Al 복합분말이 형성되었기 때문으로 사료된 다. 그러나 Fecralloy와 STS434L을 혼합한 경우 (b)는 30 시간 산화시험 이후부터는 Fe2O3, Fe-Cr 복합 산화물, Cr2O3 및 Al2O3 등 다양한 산화물들이 생성되었음을 알 수 있다. 이때부터 생성된 산화물은 산화시험이 길어짐에 따라 다소 강도가 증가하였으며 다른 상은 새로 출현하지 않았다. Fecralloy와 Al 첨가 시 Al2O3 피크의 차이 외엔 다른 산화물상이 발견이 되지 않았지만 초기 무게변화 기 울기는 상당한 차이를 보였다. 이는 앞서 언급했듯이, 산 화시험 초기단계에 첨가된 Al이 입계에 용융상태로 networking 되어 유입된 산소와 산화반응을 하여 산화층 계면을 형성하고, 성장된 계면은 외부로부터 산소의 내부 확산을 점차 감소시킴으로써 초기단계 이후 무게변화 기 울기가 완만해짐으로 무게변화율 그래프가 포물선 형태를 보이면서 증가한 것으로 판단된다[14, 15].
- 그림 6은 성형체 그리고 210시간 산화시험 후 Al과 Fecralloy 혼합 성형체의 EDS 분석결과이다. 밀폐시킨 상 태로 Al과 Fecralloy를 혼합하여 볼밀링한 시편의 경우 Al 이 입계에 편석이 되어있었고, Al의 산화가 진행되지 않 은 것을 확인할 수 있었다. 반면, 공기를 유입하면서 볼밀 링한 시편은 비교적 Al이 편석되지 않고 산소와 반응하여 입계에 Al 스케일을 형성하여 기공 채널에 의한 외부 산 소 유입을 억제한 것으로 판단된다. 산화시간 210 시간 후 에도 연속적인 Al 보호피막이 형성되어있는 것을 알 수 있었다. 이는 산화성이 강한 Al이 입계로 확산되어 Cr 산 화층을 형성하는 Cr의 임계농도를 줄여 Cr이온의 결핍을 줄이고 선택적으로 Al 산화물을 형성하여 Fe 이온과 Cr 이온의 외부확산을 억제한 것으로 생각된다[13].
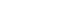
- 그림 7은 위의 시편을 각각의 산화시간별로 전기비저항 을 측정한 그래프이다. 소결이 진행되면 전기저항의 감소 가 일어나므로 전기저항을 측정하여 고온 안정성에 대한 검토를 하였다. 모든 시편에서 산화시험 초기에는 높은 비 저항 값이 나타났으며, 산화시험이 진행됨에 따라 비저항 값이 감소되는 것을 관찰할 수 있었다. Fecralloy보다 434L과 Fecralloy를 혼합한 경우가 다소 높은 전기저항 값 을 보여주었고, Al을 혼합한 시편의 경우는 보다 낮은 값 을 보여주었다. Al을 첨가하였을 때 밀도는 다소 상승하 나 저항에는 큰 변화가 없는 것으로 보아 Al2O3 상이 전 기저항에는 효과가 미비한 것으로 생각된다. 산화시험 초 기 30시간 까지 비저항 값이 감소되었지만 이후에는 큰 변화를 보여주지 않았고 산화시간이 증가함에 따라 산화 계면 성장으로 인한 치밀화는 진행되고 있으나 산화에 의 한 무게 및 전기저항 변화율이 완만한 것으로 보아 안정 화 단계에 도달한 것으로 판단된다. Fecralloy에 434L 첨 가 시 20시간 이후 Fe 및 Fe-Cr 복합 산화물이 형성되어 Fecralloy에 비해 밀도 상승과 함께 비교적 높은 전기저항 값을 얻을 수 있었다.
실험결과 및 고찰
Fig. 3

Weight change ratio of STS434L or Al added Fecralloy specimens after oxidation tests at 950°C for 210 hrs in air.

Fig. 4

Relative density of STS434L or Al added Fecralloy specimens after oxidation tests at 950°C for 210 hrs in air.

Fig. 5

X-ray diffraction patterns of respective specimens after different periods of exposure at 950°C in air: (a) Fecralloy, (b) Fecralloy+25 wt.% STS434L, (c) Fecralloy+10 wt.% Al(in air) (d)Fecralloy+10 wt.% Al (sealed).

Fig. 6

EDS mapping results of green compacts (a, c) and the compacts exposed for 210 hours at 950°C in air (b, d): (a), (b) Fecralloy+10wt.% Al(sealed) and (c), (d) Fecralloy+10wt.% Al (in air).

- Fecralloy에 STS434L 및 Al을 첨가하여 950°C에서 210 시간까지 산화시험을 한 결과 다음과 같은 결론을 얻을 수 있었다.
- Fecralloy에 Al 첨가 시 초기 밀도는 다소 증가하였고 434L을 첨가한 경우는 성형성을 크게 개선할 수는 없었다. 또한 Al 첨가에 따라 산화초기에 급격한 무게변화율 거동을 보였고 이는 networking 된 Al이 연속적인 산화피막의 형성 으로 인한 것으로 판단된다. 434L을 첨가했을 때는 복합산 화물의 형성으로 전기저항을 향상시킬 수 있었고, Fecralloy 에 Al을 혼합했을 경우 밀도의 증가로 성형성을 개선할 수 있었다.
결 론
-
Acknowledgements
- 본 논문은 한국연구재단(NO. NRF-2013R1A1A2063036)의 지원으로 수행되었으며 이에 감사드립니다.
감사의 글
- 1. H W Pickering: J. Electrochem. Soc., (1972) 119 641.Article
- 2. N Birks, G H Meier and F S Pettit, Introduction to the High Temperature Oxidation of Metals, (1983) Cambridge University Press, London 118.
- 3. S J Han, M.S. Thesis Influence of Y element on the heat resistance of the Fe-Cr-Al alloy. (2015) Inha Univerisity, Incheon.
- 4. P Y Hou and J stringer: Oxid. Met., (1992) 38 323.ArticlePDF
- 5. B Pieraggi and R A Rapp: J. Electrochem. Soc., (1993) 140 2844.ArticlePDF
- 6. B Pieraggi, R A Rapp and J P Hirth: Oxid. Met., (1995) 44 63.ArticlePDF
- 7. B A Pint: Oxid. Met., (1996) 45 1.ArticlePDF
- 8. H J Grabke, M Steinhorst, M Brumm and D Wiemer: Oxid. Met., (1991) 35 199.ArticlePDF
- 9. A V C Sobral, C V Franco, M P Hierro, F J Perez and Jr W Ristow: Mater. Corros., (2000) 51 791.Article
- 10. I S Lee: J. Korean Inst. Met. Mater., (2009) 47 716.
- 11. B U Koo, S I Lee, D H Park, J Y Yun and B K Kim: J. Korean Powder Metall. Inst., (2015) 22 100.Article
- 12. F H Stott and F I Wei: Oxid. Met., (1989) 31 369.ArticlePDF
- 13. J Stringer, B A Wilcox and R I Jaffee: Oxid. Met., (1972) 5 11.ArticlePDF
- 14. J W Park, B H Koo, W Y Jung, D K Park and I S Ahn: J. Korean Powder Metall. Inst., (2016) 23 240.Article
- 15. F H Stott, G C Wood and F A Golightly: Corros. Sci., (1979) 19 869.Article
Figure & Data
References
Citations
Citations to this article as recorded by 

A Study on the Development of Compactability and Electrical Resistivity for P/M Fecralloy






Fig. 1
SEM images of the used powder.
Fig. 2
Cycle of oxidation test.
Fig. 3
Weight change ratio of STS434L or Al added Fecralloy specimens after oxidation tests at 950°C for 210 hrs in air.
Fig. 4
Relative density of STS434L or Al added Fecralloy specimens after oxidation tests at 950°C for 210 hrs in air.
Fig. 5
X-ray diffraction patterns of respective specimens after different periods of exposure at 950°C in air: (a) Fecralloy, (b) Fecralloy+25 wt.% STS434L, (c) Fecralloy+10 wt.% Al(in air) (d)Fecralloy+10 wt.% Al (sealed).
Fig. 6
EDS mapping results of green compacts (a, c) and the compacts exposed for 210 hours at 950°C in air (b, d): (a), (b) Fecralloy+10wt.% Al(sealed) and (c), (d) Fecralloy+10wt.% Al (in air).
Fig. 7
Electrical Resistivity of Fecralloy and STS434L and Al added specimens after oxidation tests at 900°C for 210 hrs in air.
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Fig. 7
A Study on the Development of Compactability and Electrical Resistivity for P/M Fecralloy
| C | Cr | Al | Mo | Si | Mn | Y | Fe | |
|---|---|---|---|---|---|---|---|---|
|
|
||||||||
| 434L | 0.01 | 16.73 | - | 1.09 | 0.8 | 0.17 | - | Bal |
| Fecraloy | 0.1 | 22.3 | 6.6 | - | - | 1 | 0.2 | Bal |
Table 1
Composition of the used powder(wt.%).
Table 1
TOP
 KPMI
KPMI




 Cite this Article
Cite this Article