Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 25(4); 2018 > Article
-
ARTICLE
수열합성을 이용한 나노분말 합성 및 연료감응태양전지 응용 - 임진영, 안정석, 안중호*
- Synthesis of Nanopowders by Hydrothermal Method and their Application to Dye-sentisized Solar Cell Materials
- JinYoung Lim, Jeongseok Ahn, Jung-Ho Ahn*
-
Journal of Korean Powder Metallurgy Institute 2018;25(4):309-315.
DOI: https://doi.org/10.4150/KPMI.2018.25.4.309
Published online: July 31, 2018
안동대학교 신소재공학부
School of Advanced Materials Engineering, Andong National University, 1375 Gyeongdong-ro, Andong, Gyeongbuk 760-749,Republic of Korea
- *Corresponding Author: Jung-Ho Ahn, TEL: +82-54-820-5648, FAX: +82-54-820-5621, E-mail: jhahn@anu.ac.kr
© The Korean Powder Metallurgy Institute. All rights reserved.
- 877 Views
- 2 Download
Abstract
- In the present work, we synthesize nano-sized ZnO, SnO2, and TiO2 powders by hydrothermal reaction using metal chlorides. We also examine the energy-storage characteristics of the resulting materials to evaluate the potential application of these powders to dye-sensitized solar cells. The control of processing parameters such as pressure, temperature, and the concentration of aqueous solution results in the formation of a variety of powder morphologies with different sizes. Nano-rod, nano-flower, and spherical powders are easily formed with the present method. Heat treatment after the hydrothermal reaction usually increases the size of the powder. At temperatures above 1000°C, a complete collapse of the shape occurs. With regard to the capacity of DSSC materials, the hydrothermally synthesized TiO2 results in the highest current density of 9.1 mA/cm2 among the examined oxides. This is attributed to the fine particle size and morphology with large specific surface area.
- 수열합성법(hydrothermal method)은 금속 이온을 함유 하는 수용액을 고온, 고압으로 반응시켜 다양한 나노 및 마이크론 급 분말을 합성하는 방법이다. 이 합성법은 반응 의 온도, 압력, 용해도, 용매의 조성 및 농도에 따라 크게 다른 분말을 합성할 수 있다[1-3]. 그러나 수열반응은 결 정의 성장 메커니즘이 매우 복잡하므로, 최종 생성물의 형 상 및 크기를 이론적으로 예측하기가 어렵다. 그럼에도 불 구하고 비교적 용이한 공정으로 다량의 나노분말을 제조 할 수 있는 큰 장점이 있다. 본 연구에서는 가격이 저렴한 금속 염화물 수용액을 이용한 수열반응으로 금속 산화물 나노 분말을 제조하였다. 합성한 금속 산화물 분말은 ZnO, SnO2 및 TiO2이었다. 특히 수용액의 농도, 온도에 따 른 생성 입자의 형상 및 크기 등의 상관관계에 대해 조사 하였다[4, 5].
- 또한 이렇게 합성된 분말의 응용 가능성을 알아보기 위 해 염료감응형 태양전지(dye-sentisized solar cell; DSSC) 의 전극재료로서의 기초 특성도 조사해보았다. 주지하는 바와 같이, 태양전지는 원료물질에 따라 실리콘 태양전지, 화합물 반도체 태양전지, 유기분자 태양전지 및 염료감응 형 태양전지로 나눌 수 있다. 이 중에서 전극재 표면에 염 료가 흡착된 염료감응형 태양전지는 실리콘계 전지 보다 성능은 다소 미흡하나 염가의 양산에 유리한 측면이 있다. 특히 이 타입의 태양전지에 산화물 나노입자를 사용하면 높은 에너지 변환 효율과 함께 저렴한 제조 단가(실리콘 태양전지 가격의 약 1/4)가 가능하다고 알려져 있다[6, 7]. 이러한 배경에서 수열합성 분말의 연료감응형 태양전지 재료로의 응용 가능성 타진은 매우 필요한 것으로 생각되 어 본 연구를 행하였다.
서 론
- ZnO, SnO2 및 TiO2를 합성하기 위해 본 연구에서는 사용 한 용액은 기본적으로 금속 염화물 0.1M(TiCl4, SnCl2,. ZnCl2)의 수용액이었다. 수열반응은 압력용기의 온도와 수 용액의 조성 및 농도를 주요 변수로 두었으며, 이에 따라 합성된 분말의 형태 및 크기, 수율 등을 조사하였다. 사용 된 금속 염은 ZnCl2 (Aldrich, 99.9%, ~100 μm), SnCl2 (Junsei, 98.0%), TiCl4(Aldrich, 99.9%), 그리고 첨가제인 수산화나트륨(NaOH, Duksan, 98.0%)이었다. 본 실험에 사용된 수용액의 조성 및 공정조건은 표 1에 나타냈다. 먼 저, 염화물만 사용한 수용액으로 예비실험을 행하였다. 추 가 실험에서는 3~8M의 NaOH 수용액을 첨가하였다. 준비 한 수용액은 100 ml의 압력용기(autoclave)에 장입하였다. 수열반응은 기본적으로 150oC에서 24시간 동안 행하였다. 반응 후 압력용기는 상온으로 서냉하였다. 냉각 후 용기 내에 남은 생성물은 에탄올과 증류수를 이용하여 다섯 차 례 세척한 후 원심분리기로 분리하고, 이를 다시 오븐에서 100°C, 10시간 유지하여 건조하였다. 최종적으로 세척과 건 조 공정을 거친 분말은 FE-SEM(Field-emission scanning electron microscope, Jeol JSM-6700F)을 이용해 형상 및 입자 크기를 관찰하였다. 상 분석은 XRD(X-ray diffractometer, Rigaku D/MAX 2000)을 이용해(Cu Kα: 1.541 Å) 조사하였 다. 그리고 일부 합성된 분말의 열적 안정성과 상 변화를 조사하기 위해 TG/DTA (Differential thermal analysis; Thermal Analysis System:TG-8120)로 분석하였다. 금속 산화물의 비표면적은 Brunauer-Emmett-Teller(BET)법을 이용하여 Accelerated Surface Area and Porosimetry (ASAP 2010)로 분석했다.
- 합성된 분말은 연료감응 형 태양전지로서의 기초특성을 조사했다. 이를 위해 전도성 유리(ITO glass)에 산화물 분 말을 습식으로 코팅 후 건조하여 전극을 준비하였다. 사용 된 염료는 염가의 천연의 라즈베리 액을 사용하였다. 반대 극은 전도성 유리에 탄소를 코팅해 준비하였다. 염료감응 형 태양전지 셀의 I-V curve 및 변환효율 측정은 lab view 8.5 (solar simulator) 프로그램을 이용했다. 사용된 광원은 1.5 필터가 내장된 150 W Xenon Lamp의 100 mW/cm² 세 기 빛이었다. 태양전지의 효율에 영향을 미치는 중요한 요 소인 충진요소(fill factor: FF)는 개방전압(Voc)와 단락전류 (Jsc)의 곱에 대한 출력의 비로 정의하여, I-V곡선의 최대 면적으로 구했다.
실험 방법
- 3.1 수열반응에 의한 분말 형상의 변화
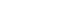
- 그림 1은 예비실험으로 ZnCl2 수용액을 사용하여 150°C 에서 24시간 수열합성 하였을 때 생성된 분말의 모습이다. ZnCl2 수용액만을 사용했을 때는 ZnO 상이 형성되었지만, 그림 1(a)서 보는 바와 같이 분말의 형상이 일정치 않고 입도도 매우 불균일했다. 따라서 이후의 본 분말에서는 다 양한 형상을 얻기 위해 추가로 NaOH를 첨가하였다. NaOH의 첨가는 분말의 형상을 크게 변화시켰다. 이는 ZnCl2 수용액을 ZnCl2수용액에 5M의 NaOH수용액을 추 가하여 100~200°C에서 24시간 동안 수열 반응한 생성물 의 SEM 형상에서 잘 나타나있다(그림 1(b~d)). 사진에서 보듯이 온도에 따라 형상의 큰 변화가 관찰되었다. 먼저, 100°C에서는 분말의 형상이 제대로 형상되지 않았다. 이 는 수열 반응의 온도가 충분하지 않아 분말의 형태가 제 대로 형성되지 않는 것으로 생각된다. 온도를 올려 150°C 에서는 수~수 십 μm의 길이를 가지는 막대형상이 형성되 었다. 200°C에서는 막대 형상도 생성되었으나 일부는 불 규칙한 분말도 형성되었다. 즉, 150°C에서 가장 균질 한 막대형상의 분말을 얻었다. 이는 수열합성 온도에 따라 입 자의 크기와 형상, 균질을 적절하게 조절할 수 있음을 보 여준다. XRD 분석 결과에 의하면 합성된 분말은 모든 온 도에서 JCPDS번호 00-036-1451의 ZnO 산화물이었다(그 림 2). 이 실험에 이어 NaOH 수용액 농도에 대한 영향을 조사해보았다. 그림 3은 3M~8M NaOH 수용액을 150°C 에서 24시간 동안 수열 반응한 생성물을 SEM 형상이다. NaOH 수용액의 농도가 3M인 경우 사진과 같이 막대 형 상을 가지긴 했지만, 분말의 형상이 다소 불 균일했다. 반 면 NaOH 수용액의 농도가 5M로 증가하면 훨씬 균일한 막대 형태의 분말이 합성되었다. 마지막으로 NaOH 수용 액의 농도가 8M로 증가할 경우 분말 입자의 크기가 성장 한 것을 볼 수 있다. 한편, 그림 4는 NaOH 수용액의 농도 변화에 따른 비표면적을 BET로 측정한 결과이다. 5M에 서 측정된 비표면적이 6.0068 m2/g로 가장 큰 값을 가졌음 을 알 수 있다. 그러나 XRD 패턴을 분석한 결과, NaOH 의 조성에 무관하게 모두 ZnO 상이었으며, 이외의 불순물 은 관찰되지 않았다. 그림 2
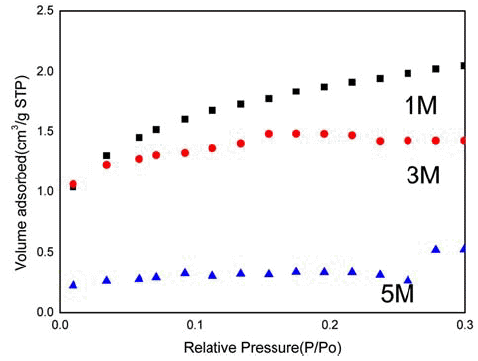
- 한편, SnO2 산화물을 얻기 위해 SnCl2 수용액에 NaOH 수용액 첨가해 150°C에서 24시간 동안 수열반응 시킨 생 성물의 농도에 따른 SEM 형상이 그림 5에 예시되어 있다. 형상에서 보듯이 모든 조성에서 수~수 십 μm의 길이를 가지는 판상의 분말이 형성되었다. 특히, NaOH 수용액의 농도가 1M인 경우 미세한 크기의 꽃 형태의 판상이 형성 되었다. 농도가 3M로 증가하면 판상의 형태는 유지되었지 만 입자 크기가 성장하고 불규칙 형상도 함께 관찰되었다. NaOH 수용액의 농도가 5M로 증가하면 3M의 경우 보다 분말 입자가 더욱 성장한 것을 볼 수 있다. 그림 6은 수용 액의 농도 변화에 따른 생성물의 비표면적을 BET로 측정 한 결과이다. 1M 분말에서 측정된 비표면적은 6.6468 m2/ g로 합성된 SnO2 중 가장 큰 값을 가졌다. NaOH가 과포 화 됨에 따라 분말의 비표면적이 감소하였으며, 5M의 경 우 그 값이 크게 감소하였다. 이 경우도 수열반응후의 생 성물은 모든 조성에서 XRD 분석결과 SnO2 이었으며, 불 순물은 나타나지 않았다.
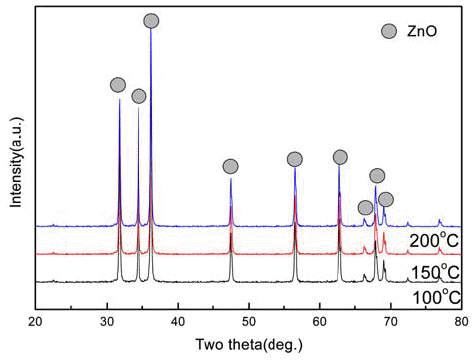
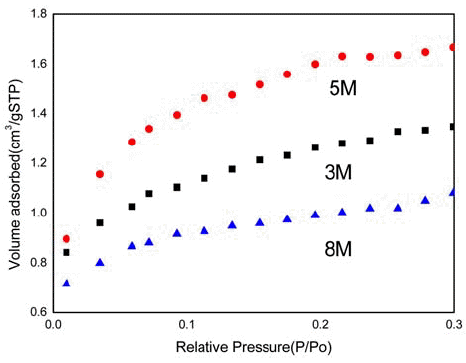
- 세 번째로 조사한 계는 TiO2였다. TiCl4 수용액에 NaOH 수용액을 추가하여 150°C에서 24시간 동안 수열반응 한 생성물의 형상이 그림 7에 예시되어 있다. 사진에서처럼 NaOH의 농도 변화에 따라 형상에 큰 차이가 나타났다. 3M인 경우 수십~수백 nm 크기의 꽃 형태가 나타나기 시 작했다. 그러나 입자의 형상이 뚜렷하지는 않았다. NaOH 수용액의 농도가 5M로 증가하면 잘 발달된 미세한 입자 의 나노꽃 형태가 형상되었다. NaOH 수용액의 농도를 8M로 증가할 경우 분말 입자의 형상이 구형으로 변했다. 분말의 BET 비표면적도 NaOH 5M을 추가해 얻은 미세한 꽃 모양의 경우가 52.0735 m2/g로 가장 높은 값을 보여주 었다(그림 8). 이로부터 염화물 수용액에 NaOH를 추가 함 으로써 생성물의 형상과 입도크기 및 분포가 크게 영향을 받음을 알 수 있었다. XRD 분석 결과, 생성물은 모든 조 성에서 TiO2 아나타제(anatase)상이었다. 표 1
- 3.2 수열합성 분말의 후열처리 영향
- 수열반응으로 합성된 생성물을 열적 안정성과 상변화를 조사하기 위해 생성된 분말들을 400°C~1000°C, Ar 분위 기에서 1시간 동안 후속 열처리 하여 보았다. 조사한 3계 모두에서 후속 열처리의 온도가 400°C~500°C 이하의 중 저온에서는 수열 합성된 형상이 대체로 유지 되었다. 그러 나 1000°C 전후의 고온에서는 원래의 형상이 붕괴되고 구 형화되는 경향이 있었다. 이러한 경향은 ZnO 및 SnO2에 서도 유사했다. 그림 9에는 열처리 후 얻어진 SnO2 분말 의 SEM 형상이 예시되어 있다. 사진에서 보듯이 1000°C 의 후속 열처리 후에는 판상의 형상이 완전히 붕괴되어 등축(equi-axed) 형상으로 변화하였다. 그러나 두 계 모두 1000°C의 열처리 후에도 형상만 변화했을 뿐 원래의 생성 상인 JCPDS번호 00-036-1451의 ZnO 및 JCPDS번호 41- 1445의 SnO2가 잘 유지됨을 XRD로 확인할 수 있었다(그 림 10).
- 반면, TiO2계의 경우, XRD 분석결과 600°C~800°C 사이 에서도 아나타제 TiO2상이 고온 안정상인 루타일(rutile) TiO2로 변화했다(그림 11). 이는 수열 합성한 산화물의 DTA 측정결과 630°C에서 1100°C 사이에 나타난 흡열반 응과 대략 일치 하였다. 그러나 형상 면에서는 ZnO 및 SnO2 계에서처럼 고온에서 입자 조대화와 수열합성된 원 래의 형태가 붕괴되는 현상을 관찰했다(그림 12). 사진에 서 보듯이 분말의 형상은 400°C에서 입자의 큰 변화가 나 타나지 않았으나, 700°C에서 일부 입자가 조대화가 시작 되었다. 1000°C 열처리 후에는 분말의 형상이 완전히 등 축으로 변화하였다. 그림 10
- 3.3 수열합성 분말의 광 전극 특성 및 DSSC 효율
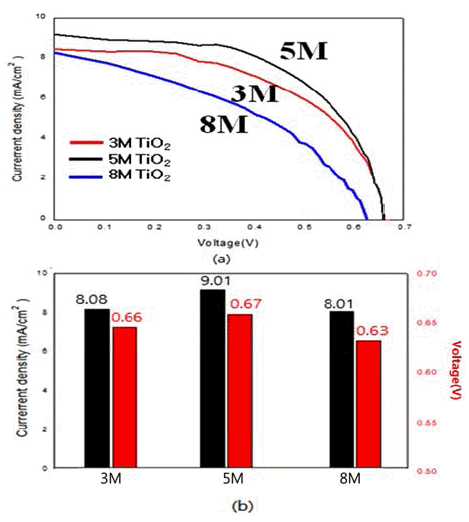
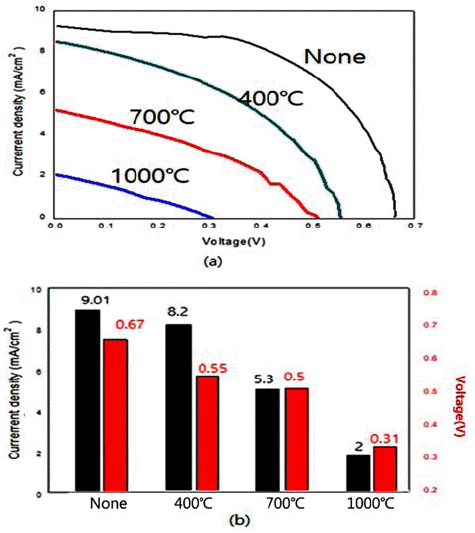
- 이렇게 수열합성 및 후속 열처리로 제조한 분말들은 연 료 감응형 전지로서의 응용 가능성을 알아보기 위해 기초 적인 DSSC 특성을 조사하였다. 먼저, 과전류밀도-전압 (Jc-I)곡선을 측정하여 대략적인 경향을 살펴보았으며, 아 울러 전류밀도와 개방전압(open circuit voltage)도 조사하 였다. 그림 13~15에는 NaOH 수용액의 농도변화에 따른 ZnO, SnO2 및 TiO2계의 DSSC 특성이 요약되어 있다. 결 과에서 보듯이 광전류밀도와 효율은 SnO2→ZnO→TiO2 의 순으로 높았다. 특히, 모든 시편에서 NaOH 수용액의 농도에 따라 광전류밀도의 값에 큰 차이를 보여주었다. 수 열합성으로 제조된 ZnO의 경우 NaOH 5M에서 가장 높은 8.01 mA/cm²의 전류 밀도와 개방전류 값 0.53 V 값을 얻 었다. 이는 그림 4의 분말형상에서 볼 수 있는 잘 발달된 꽃 모양으로 비표면적이 가장 높은 경우와 일치하였다. 비 표면적에 대한 DSSC의 효율 증가 경향은 타 연구에서도 보고된 바 있다[8]. 비슷한 경향이 광전류밀도가 다소 낮 았던 SnO2계에서도 관찰되었다. 나노 판상이 잘 발달되어 큰 비표면적이 가장 컸던 1M NaOH 농도에서 가장 높은 값인 5.01 mA/cm² 와 0.33 V를 얻었다. 조사한 계 중에서 는 TiO2 계에서 가장 우수한 DSSC 특성을 얻었다. 그림 15에 예시된 대로 5M NaOH 농도로 합성한 시편에서 광 전류밀도 9.01 mA/cm2, 개방전압 0.67 V 값을 얻었다. 이 경우 역시 잘 발달된 나노꽃 모양에 비표면적이 가장 높 은 경우에 해당했다. TiO2계의 경우, 수열 합성된 분말의 후속 열처리가 DSSC 특성에 미치는 영향도 조사하여 보 았다. 그 결과 그림 16에 예시되었듯이 후속 열처리의 온 도가 증가 함에 DSSC 특성이 감소 함이 뚜렷했다. 이는 온도 증가에 따라 높은 비표면적을 가진 막대, 혹은 꽃 모 양의 나노 형상이 등축 혹은 구형화 되는데 기인하는 것 으로 사료된다. 그림 14
- 4 결 론
- 본 연구에서는 금속 염화물(TiCl4, SnCl2, ZnCl2) 수용액 을 사용한 수열합성법으로 다양한 형상의 분말을 제조하 였다. 아울러 이들 분말의 염료 감응형 태양전지 전극재료 로서의 응용 가능성을 타진하기 위해 기초 물성도 조사하 였다. 그 결과 다음과 같은 결론을 얻을 수 있었다. 그림 16
-
(1) 염화물(TiCl4, SnCl2, ZnCl2) 수용액의 수열반응으로 다양한 형상의 금속 산화물(ZnO, SnO2, TiO2)을 합성할 수 있었다. 특히, NaOH 수용액을 추가함으로써 형상의 다양 화가 가능했다. 또한, 실험 변수로 사용된 압력, 온도, 수 용액의 농도를 조절함으로써 구형 나노분말, 나노로드, 나 노꽃, 판상 등의 다양한 형태의 분말을 합성할 수 있었다. 합성된 분말 중에서는 TiO2의 입도가 가장 작았으며, 일부 는 비표면적이 52.0735 m2/g에 달했다.
(2) 수열 합성한 분말의 후속 열처리를 행한 결과, 조사 한 분말들은 중온에서 열적 안정성이 있었다. 그러나 고온 에서는 입자 크기의 증가에 이어 형상의 붕괴나 일부 상 변화가 일어났다. TiO2 수열합성 분말의 경우 630°C 이상 에서 아나타제 상에서 루타일 상으로 변화했으며, 형상도 나노꽃 형태가 1000°C에서 붕괴되었다.
(3) 본 연구에서 수열 합성된 분말의 연료감응전지용 재 료로서의 기초 특성 조사 결과, 5M NaOH 수용액을 추가 하여 얻은 나노꽃 형태의 TiO2 분말이 측정치 9.1(mA/ cm²), 0.67(V)으로 가장 우수한 특성을 보여주었다.
- 이상의 결과, 금속 염화물 수용액의 수열합성 공정 변수 를 조절함으로써 비교적 용이하게 다양한 형상과 크기가 다른 나노분말을 합성할 수 있었다. 특히 이들 중 일부 분 말은 특성이 우수한 연료감응형 태양전지 재료로 활용 가 능성이 확인되었다.
결과 및 고찰
SEM images of products formed after hydrothermal reaction of ZnCl2.: (a) without NaOH, and with additive solution of 5M at 100°C(b), 150°C(c), and 200°C(d).

XRD patterns of products formed after hydrothermal reaction of ZnCl2 and 5M NaOH solution at different temperatures.
SEM images of products formed after hydrothermal reaction of ZnCl2 with different concentration of NaOH solution: (a) 3M, (b) 5M and (c) 8M solution.

The SEM images of SnO2 particles obtained at different concentration of additive NaOH solution: (a) 1M, (b) 3M and (c) 5M.

The SEM images of TiO2 particles obtained after hydrothermal reaction with different concentration of additive NaOH solution: (a) 3M, (b) 5M and (c) 8M.

BET surface area of TiO2 obtained after hydrothermal reaction with different concentration of additive NaOH solution.
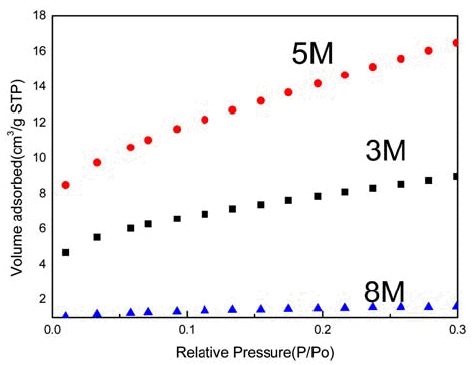
Composition and heat-treatment condition of examined systems (the hydrothermal reaction was carried out at 150°C for 24h).
|
The morphological changes of hydrothermally processed SnO2 particles after a subsequent heat-treatment at different temperatures: (a) un-treated powders, (b) 400°C, (c) 700°C and (d) 1000°C.

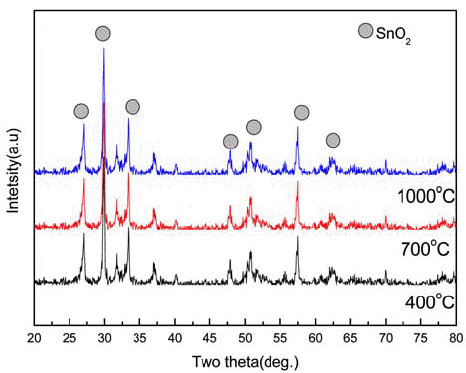
The XRD patterns of hydrothermally processed SnO2 particles after a subsequent heat-treatment at different temperatures.
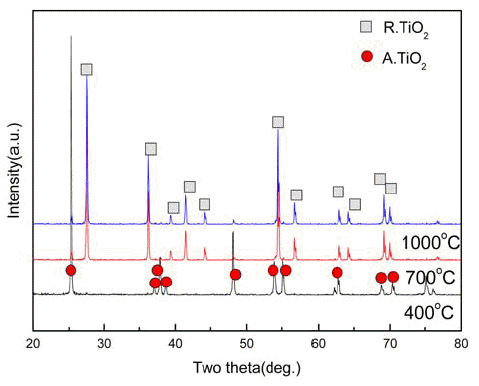
The XRD patterns of hydrothermally processed TiO2 particles after a subsequent heat-treatment at different temperatures.
The morphological changes of hydrothermally processed TiO2 particles after a subsequent heat-treatment at different temperatures: (a) un-treated powders, (b) 400°C, (c) 700°C and (d) 1000°C.

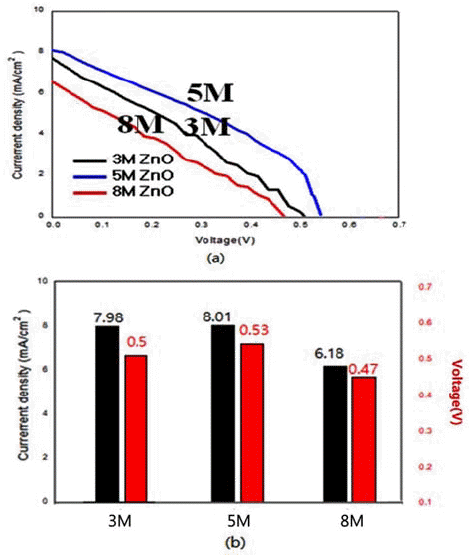
Photocurrent density-voltage (Jc-V) curve: (a) the values of current density, and (b) open circuit voltage of DSSC made by hydrothermally synthesized ZnO particles obtained with different concentration of NaOH solution.
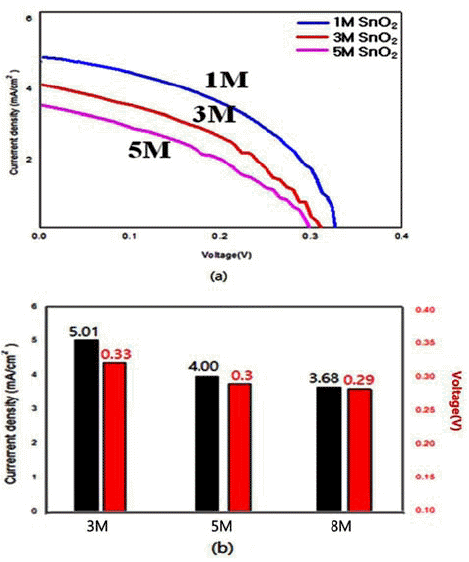
Photocurrent density-voltage (Jc-V) curve: (a) the values of current density, and (b) open circuit voltage of DSSC made by hydrothermally synthesized SnO2 particles obtained with different concentration of NaOH solution.
Photocurrent density-voltage (Jc-V) curve: (a) the values of current density, and (b) open circuit voltage of DSSC made by hydrothermally synthesized TiO2 particles obtained with different concentration of NaOH solution.
Photocurrent density-voltage (Jc-V) curve: (a) the values of current density, and (b) open circuit voltage of DSSC made by hydrothermally synthesized TiO2 particles obtained after heat treatment at different temperature.
-
Acknowledgements
- 이 논문은 안동대학교 기본연구지원사업에 의하여 연구 되었습니다.
감사의 글
- [1] . H. Gleiter : Prog. Mater. Sci.., 33 (1989) 2230079-6425.Article
- [2] . H. Gleite : Nanostruct. Mater.., 1 (1992) 10965-9773.Article
- [3] . C. Suryanarayana and F.H. Froes: Metall. Trans.., 23A (1992) 10710026-086X.Article
- [4] . R.W. Siegel , E. Hu and M.C. Roco, (1998).
- [5] . J.H. Huang , V.P. Dravid, M.H. Teng, J.J. Host, B.R. Elliott, D.L. Johnson and T.O. Mason: J. Mater. Res.., 12 (1997) 10760884-2914.Article
- [6] . S. E. Gledhill , B. Scott and B. A. Gregg: J. Mater. Res.., 20 (2005) 31670884-2914.Article
- [7] . N. Kopidakis , K.D. Benkstein, J. van de Lagemaat and A.J. Frank: J. Phys. Chem. B., 107 (2003) 113071520-6106.Article
- [8] . Y. J. Son , J. S. Kang, J. J. Yoon, J. Kim, J. W. Jeong, J. H. Kang, M. J. Lee, H. S. Park and Y. E. Sung: J. Phys. Chem. C., 122 (2018) 70511932-7447.Article
Figure & Data
References
Citations




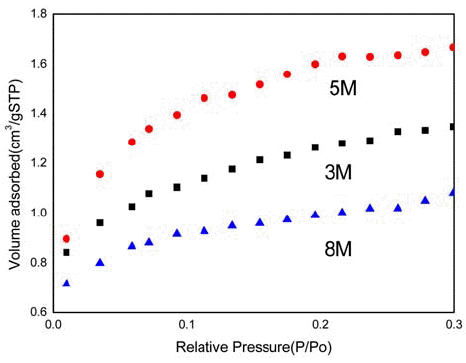

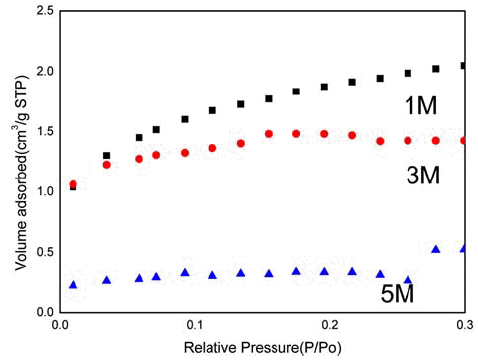

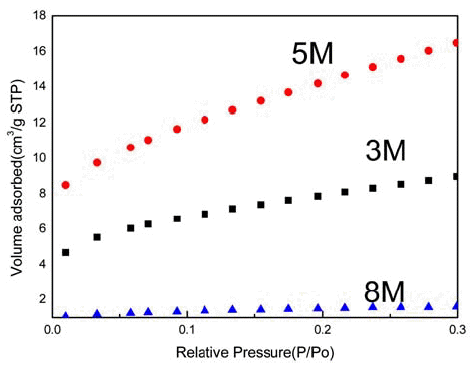

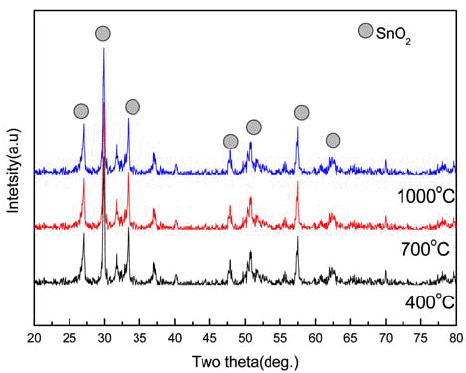
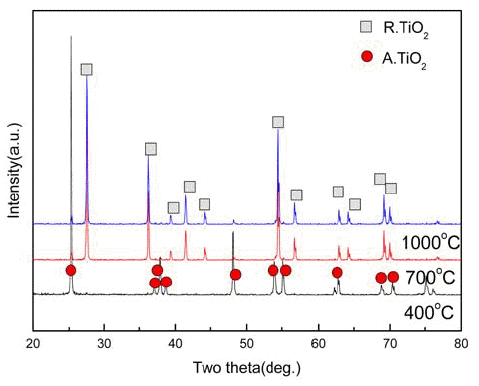


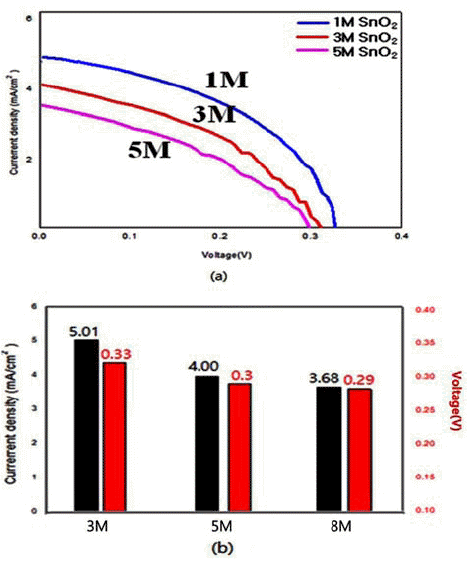
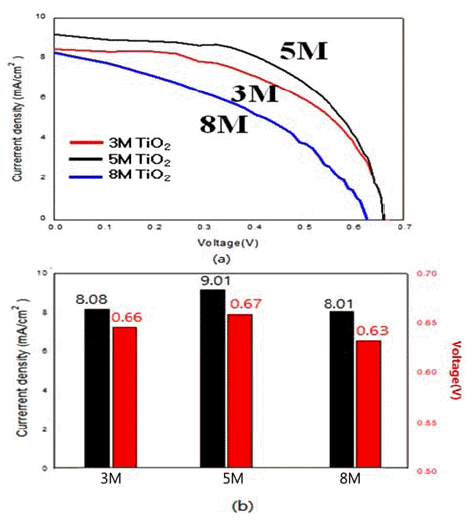
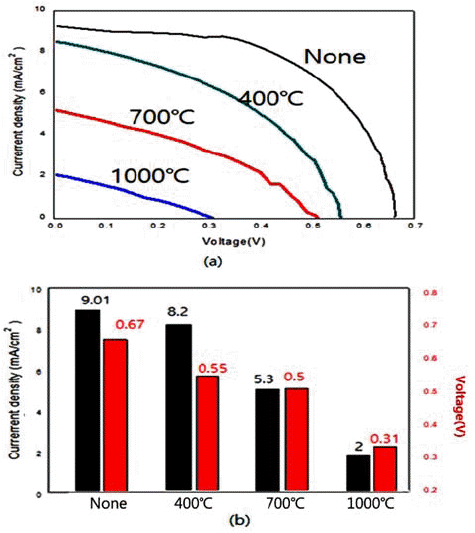
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Fig. 7
Fig. 8
Fig. 9
Fig. 10
Fig. 11
Fig. 12
Fig. 13
Fig. 14
Fig. 15
Fig. 16
Table 1
TOP
 KPMI
KPMI

 Cite this Article
Cite this Article