Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 26(4); 2019 > Article
-
ARTICLE
고순도 TiCl4 제조 및 이를 활용한 고순도 Ti 분말 제조 공정 연구 - 이지은, 윤진호, 이찬기*
- Study on Manufacture of High Purity TiCl4 and Synthesis of High Purity Ti Powders
- Jieun Lee, Jin-Ho Yoon, Chan Gi Lee*
-
Journal of Korean Powder Metallurgy Institute 2019;26(4):282-289.
DOI: https://doi.org/10.4150/KPMI.2019.26.4.282
Published online: July 31, 2019
고등기술연구원 융합소재연구센터
Materials Science and Chemical Engineering Center, Institute for Advanced Engineering, Yongin 17180, Republic of Korea
- *Corresponding Author : Chan Gi Lee, TEL: +82-31-330-7495, FAX: +82-31-330-7116, E-mail: cglee@iae.re.kr
- - 이지은: 연구원, 윤진호: 책임연구원, 이찬기: 수석연구원
• Received: June 20, 2019 • Revised: August 8, 2019 • Accepted: August 9, 2019
© The Korean Powder Metallurgy Institute. All rights reserved.
- 1,756 Views
- 33 Download
Abstract
- Ti has received considerable attention for aerospace, vehicle, and semiconductor industry applications because of its acid-resistant nature, low density, and high mechanical strength. A common precursor used for preparing Ti materials is TiCl4. To prepare high-purity TiCl4, a process based on the removal of VOCl3 has been widely applied. However, VOCl3 removal by distillation and condensation is difficult because of the similar physical properties of TiCl4 and VOCl3. To circumvent this problem, in this study, we have developed a process for VOCl3 removal using Cu powder and mineral oil as purifying agents. The effects of reaction time and temperature, and ratio of purifying agents on the VOCl3 removal efficiency are investigated by chemical and structural measurements. Clear TiCl4 is obtained after the removal of VOCl3. Notably, complete removal of VOCl3 is achieved with 2.0 wt% of mineral oil. Moreover, the refined TiCl4 is used as a precursor for the synthesis of Ti powder. Ti powder is fabricated by a thermal reduction process at 1,100ºC using an H2-Ar gas mixture. The average size of the Ti powder particles is in the range of 1-3 μm.
- 타이타늄(Ti)은 경량화 소재로 항공, 국방, 자동차 및 방 열소재와 같이 견고하면서 내식성을 중요시 하는 산업에 서 주로 사용된다[1]. 최근에는 반도체 산업 및 의료산업 까지 활용범위가 증가하였으며, 해당 산업에서는 고순도 Ti을 필요로 하므로 Ti 제조 공정 시 불순물 제어가 필수 적이다. Ti 생산의 95%가 크롤(Kroll) 법을 이용하여 생산 되며 Kroll법은, 사염화타이타늄(TiCl4)을 전구체로 이용하 여 마그네슘(Mg)과의 열환원을 통해 최종적으로 Ti 스폰 지 형태로 생산하는 공정이다[2]. 또한 TiCl4은 Ti 뿐만 아 니라 안료 및 도료 제조를 위한 이산화타이타늄(TiO2)의 전구체로도 사용된다[1]. 이와 같이 Ti 및 TiO2의 제조를 위해서는 TiCl4이 필수적이며, 고순도의 Ti 및 TiO2 제조 를 위해서는 TiCl4 내의 불순물 제거가 필수적이다. TiCl4 를 제조하기 위한 원료로서 루타일(Rutile)을 주로 이용하 는데 rutile 내에는 주로 철(Fe), 알루미늄(Al), 바나듐(V), 실리콘(Si) 등과 같은 불순물이 존재한다. TiCl4 내의 불순 물은 공정상에서의 문제뿐만 아니라 최종 산물인 Ti 및 TiO2에서도 문제점을 야기한다. 염화공정을 거친 Fe의 경 우 염화제이철(FeCl3) 및 염화제일철(FeCl2)로 존재하는데, 염화공정을 거친 FeCl3의 경우 유사한 녹는점(300ºC)과 끓는점(317ºC)으로 인해 녹는점 근처에서는 겔상태로 존 재하게 된다. 따라서 공정 중에 온도구배가 발생하면 겔상 태의 FeCl3로 인해 관막힘 현상이 발생하게 된다. Fe 외로 TiCl4 내에 Al과 Si, V계열의 불순물이 존재할 경우 노란 색을 띄기 때문에 안료로써 적합하지 않게 된다. 뿐만 아 니라 Al과 V불순물은 생체재료로 이용시 세포에 대한 독 성 및 치매 유발의 가능성을 지님으로서 합금화에 대해 논란이 되고 있는 물질이다. 이러한 불순물은 각각의 정제 공정을 거치는데, FeCl3의 경우 응축공정을 통해, Al과 Si 염화물은 증류 공정을 거쳐 TiCl4과 분리 후 정제된다. 반 면 V불순물인 바나듐옥시트리염화물(VOCl3)의 경우 TiCl4과 유사한 물리적 특성으로 인해 증류 및 응축으로 제거되지 않는다[3-7]. 일반적으로 TiCl4에 함유되어 있는 VOCl3을 제거하기 위해서는 agent를 이용한 화학적 처리 를 이용하여 증류 및 분류된다[4, 9-11]. TiCl4의 경우 산 소(O2) 및 수분(H2O)과 접촉시 염산(HCl)과 TiO2이 생성 되므로, 대기 노출 공정으로는 불순물 처리가 불가능하다. 따라서 닫은 계에서 금속 및 유기물질과 같은 agent를 이 용한 VOCl3 제거 연구가 그동안 진행되어왔다. 이 연구에 대한 결과로 VOCl3 제거를 위한 agent의 특징 및 종류를 표 1과 같이 정리하였다. VOCl3 제거를 위한 agent로는 mineral oil, H2S, Al 및 Cu 분말을 이용한 연구가 진행되 었다[9-11]. H2S의 경우 가스 형태로 반응시킴에 따라 안 전상에 문제가 있으며 Al 분말의 경우 반응 공정에서 TiCl4가 삼염화타이타늄(TiCl3)으로 전환됨에 따라 TiCl4의 손실을 야기한다. 또한 부식성을 지닌 염화알루미늄 (AlCl3)로 인한 장비손상 및 AlCl3과 같은 불순물 유입 가 능성이 존재하므로 배제하였다. Mineral oil의 경우 Residue를 형성한다는 단점이 있으나, 값이 저렴하다는 장 점이 있으며, 구리(Cu)의 경우 ppb단위의 VOCl3 제거에 매우 효율적이라는 장점이 있다[10]. 따라서 본 연구에서 는 Ti 및 TiO2의 생산에 필요한 전구체인 고순도 TiCl4를 제조하고자 Cu분말과 mineral oil을 이용하여 TiCl4 내 불 순물 중 VOCl3 제거 조건을 최적화 하였다. 또한 TiCl4의 활용 및 Ti 소재화에 대한 연구로써, TiCl4을 이용하여 Ti 분말을 제조하는 연구를 진행하고자 하였다. 이전 TiCl4을 이용하여 Ti을 제조하는 방법으로는 앞서 언급한 크롤법 을 주로 이용하였으나, 크롤법은 스폰지를 만드는 공정으 로 분말을 제조하기 위해서는 추가 공정이 필요하였다. 따 라서 TiCl4로부터 추가공정을 거치지 않고 분말을 제조하 기 위한 연구가 진행되어왔으며, 주로 플라즈마를 이용한 연구가 진행되었다[12]. 하지만 플라즈마의 경우 장치 제 조까지 고비용이 소요될 뿐만 아니라, TiCl4을 이용할 경우 재질 선정, 내부 분위기 조절 등 장치 제작을 위한 많은 제 약이 존재하였다. 본 연구에서는 간단한 장치를 통해 Ti 분 말 제조 가능성을 확인하고자 하였으며, 이를 위한 방안으 로 열환원을 이용하여 Ti 분말 합성 연구를 실시하였다.
1. 서 론
- 2.1 고순도 TiCl4 제조 연구
- 일반적으로 rutile로부터 염소화공정을 거쳐 생성된 TiCl4 내에는 약 0.1 wt% VOCl3이 함유되어 있다[8]. 하지 만 시중에 판매하고 있는 TiCl4 내에는 VOCl3를 제거하기 때문에 모사용액을 제조하여 VOCl3 제거 연구를 진행하 였다. 본 연구에서 사용한 TiCl4와 VOCl3는 각각 Junsei (99%), Sigma-aldrich(99%) 제품을 이용하였다. VOCl3와 TiCl4의 경우 유사한 물리화학적 특성을 가지므로 혼합에 용이하므로 상용 TiCl4 내에 VOCl3을 첨가하여 0.1 wt% 의 VOCl3을 지니는 TiCl4을 제조하였으며, 확실한 초기 농도 확인을 위해 Microwave Plasma-Atomic Emission Spectrometer(MP-AES, Agilent, MP-AES 4200)을 이용하 여 TiCl4 내에 0.1 wt%의 VOCl3이 존재함을 확인하였다. VOCl3 제거를 위한 agent는 mineral oil(Base stock 130, Nynas)과 Cu 분말(99.999%, 100 mesh, Sigma aldrich)을 이용하였으며 agent 첨가량 및 반응시간 온도에 따른 경향 성을 확인하였다. Agent 첨가량의 경우 TiCl4 내에 존재하 는 VOCl3의 농도값에 비례하여 0.1, 0.15, 0.2 wt%의 농도 로 첨가하였으며, 반응온도는 TiCl4의 끓는점을 고려하여 100, 110, 120, 130ºC로 설정하여 연구를 실시하였다.
- TiCl4 정제를 위한 실험은 그림 1과 같이 Reactor, Condenser, Reservoir, Scrubber로 구성된 장치를 이용하였 다. TiCl4가 대기 중에 노출될 경우 H2O과 O2와 급속하게 반응하여 TiO2와 HCl이 발생하기 때문에 관막힘 현상 및 TiCl4의 손실과 장비손상을 유발할 수 있다. 이를 최소화 하기 위해 실린지 펌프를 이용하여 TiCl4를 반응기에 주입 하였다. 또한 장치 내부 H2O 및 O2 제거를 위해 TiCl4 주 입 전에 질소(N2)를 이용하여 내부 분위기를 불활성 분위 기로 조성하였다. 주입된 TiCl4은 reactor에서 VOCl3제거 agent와 일정 온도 및 시간 동안 반응하게 되고 반응한 TiCl4은 150ºC 이상의 온도에서 30 min 동안 증류하여 생 성된 침전물 및 반응 후 잔류 agent와 분리하였다. 증류된 TiCl4은 10ºC의 condenser를 통과하며 응축되어 최종적으 로 reservoir에서 정제된 TiCl4을 얻을 수 있었다. 응축되지 않은 기상의 TiCl4은 scrubber를 통과시킴으로써 대기의 노출을 최소화하였다.
- 2.2 Ti 분말 제조 연구
- VOCl3 제거 공정을 통해 정제된 TiCl4을 이용하여 Ti 분 말 합성 연구를 실시하였다. TiCl4과 수소(H2)사이의 열환 원 반응을 이용하여 Ti 분말을 제조하고자 하였으며, Ti 분말 제조 연구를 진행하기 위해 Canister, Furnace, Reservoir 로 구성된 그림 2의 장치를 이용하였다. 기상의 TiCl4과 H2반응을 위해 canister에서 130ºC로 TiCl4을 가열하였으 며, carrier gas로 알곤(Ar)을 사용하여 0.1 L/min의 조건으 로 furnace로 이송하였다. Argon분위기에서 furnace로 이 송된 TiCl4은 수소혼합가스(Ar : H2= 1 : 1, 유량: 0.2 L/min) 와 1,100ºC의 조건에서 반응시켰으며, H2와 TiCl4 사이의 격렬한 반응이 일어날 것으로 염려하여 수소혼합가스를 이용하여 합성을 실시하였다. 반응 후 합성된 Ti의 경우 자연 발화 가능성이 존재하므로, 대기와의 접촉을 방지하 기 위해 에탄올(ethanol) 용액이 담긴 reservoir에 회수하 였다.
- 2.3 물성 평가
- TiCl4은 대기 중에 노출될 경우 H2O 및 O2와 반응하여 TiO2와 HCl이 생성되어 장비 손상을 일으키므로, 전처리 가 이루어지지 않은 TiCl4의 분석은 불가능하다. 전처리가 이뤄지지 않은 TiCl4이 장치내의 H2O 및 O2와 반응시 다 량의 열과 HCl, TiO2 등을 생성하여 관막힘, 부식등과 같 은 문제를 유발한다. 따라서 대기 중에서의 안정적인 TiCl4 분석을 위해서는 타이타늄옥시클로라이드(TiOCl2) 및 TiCl4 수용액의 형태로 안정화 시킨 후 분석을 실시한 다[13]. TiCl4 수용액을 제조하기 위해서는 유기용매와 TiCl4를 혼합한 후 물을 첨가하면 유가용매가 물과의 급격 한 반응을 차단하여 결과적으로 안정적인 TiCl4 수용액 제 조가 가능하다. 이 외로도 고농도의 HCl과의 전처리 이후 분석을 실시하나 이는 발열량이 높으며, TiO2과 같은 석출 물이 순간적으로 존재하게 된다. 반면 유기용매를 이용하 여 제조된 TiCl4 수용액 내에는 TiO2와 같은 석출물이 발 생하지 않으며 HCl을 이용한 전처리 대비 발열량도 적음 을 확인할 수가 있었다. 본 연구에서는 유기용매로 n-헵탄 을 사용하였으며, TiCl4과 1:2의 비율로 반응 후 증류수를 첨가하여 TiCl4 수용액을 제조하였다. 제조된 수용액을 이 용하여 VOCl3 제거율을 확인하였으며, 순도분석을 위한 장치로는 위해 Microwave Plasma-Atomic Emission Spectrometer( MP-AES, Agilent, MP-AES 4200)을 이용하였다. VOCl3 제거 후 잔류 agent의 결정상 확인을 위해 XRD(Xray diffraction, Shimadzu XRD-6100) 분석을 실시하였다. 또한 TiCl4으로부터 열환원 공정을 이용하여 제조된 Ti 분 말의 표면 형상 및 입도 확인을 위해 TEM(Transmission Electron Microscope, JEOL, JEM-2100F) 및 PSA(Particle Size Analyzer, Microtrac, Microtrac Zetatrac) 분석을 실시 하였다.
2. 실험 방법
- 3.1 고순도 TiCl4 제조 연구
- 그림 3은 agent 사용 유무 및 비율에 따른 VOCl3 제거 전후 용액 색상 변화 결과이다. 그림 3에서와 같이 TiCl4 모사용액의 경우 VOCl3로 인해서 노란색을 띄고 있으며, agent를 사용하여 VOCl3이 제거됨에 따라 최종적으로 무 색의 TiCl4이 생산된다. 130ºC, 1시간 조건에서 약 0.2 wt%의 Mineral oil, Cu 분말+Mineral oil, Cu분말을 이용 하여 VOCl3을 제거한 결과, 그림 3에서 보는 바와 같이 Cu분말 이용하여 VOCl3을 제거할 경우 색상 변화가 미미 하며, VOCl3이 완전히 제거되지 않고 잔류하는 것을 확인 할 수가 있다. Cu분말과 mineral oil을 혼입하여 사용한 경 우에도 VOCl3은 제거되지 않았지만, Cu분말을 단독으로 사용한 것과 비교하였을 때, 색상이 옅어진 것을 보아 mineral oil을 혼용하여 사용함에 따라 제거율이 증가하는 것으로 예상하였다. 정확한 VOCl3의 제거율을 확인하기 위하여 MP-AES를 이용하여 agent 종류 및 첨가량에 따른 제거율을 분석하였으며, 이러한 결과는 표 2에 나타냈다. 0.2 wt% Cu 분말을 이용하여 VOCl3제거 연구를 실시한 결과 제거율이 19.06%로 매우 저조하였으나, 0.1 wt% mineral oil과 0.1 wt%의 Cu 분말을 혼용하여 사용할 경우 97% 이상의 제거율을 보였다. Cu 분말 대신 mineral oil을 첨가함에 따라 VOCl3 제거율은 증가하였으며, Cu 분말 농도의 영향을 크게 받지 않는 것으로 확인되었다. 따라서 VOCl3의 제거를 위해서는 mineral oil 사용이 지배적이며, Cu 분말을 이용한 연구의 경우 소량의 VOCl3 제거만 가 능한것으로 확인되었다. Mineral oil의 첨가량이 증가함에 따라서 VOCl3 제거율은 증가하였으며 0.2 wt%의 mineral oil을 첨가하였을 때, 제거율이 100%에 도달함을 확인할 수가 있었다. 실험 결과와 열역학적 거동 비교를 위해서 agent별 VOCl3 제거 거동과 관련된 열역학적 data를 HSC chemistry 7을 이용하여 계산한 결과를 그림 4과 같이 나 타내었다[4, 9]. 그림 4(a)와 그림 4(b)는 각각 mineral oil, Cu 분말과 VOCl3 사이의 반응에 대한 깁스 자유에너지 변화 ΔG(Gibbs-free energy) 값을 나타낸 결과이며, 그림 4(c)는 agent별 ΔG값이 가장 우수한 반응식을 정리한 결 과이다. 그림 4(a)의 반응식에 따르면 VOCl3 제거를 위해 서는 다양한 반응식이 존재하며 mineral oil을 이용하여 VOCl3을 제거하기 위해서는 mineral oil의 열분해로 인해 생성된 탄소(C)가 VOCl3과 반응하여 바나듐계 염화물 (VCl2, VCl3, VOCl2)의 형태로 침전되는 반응이 지배적이 었다. 하지만 반응을 위한 ΔG값은 대부분 양의 값을 지니 므로 원활한 반응이 이뤄지기 어려움을 확인할 수가 있었 으며, VCl3을 생성하는 반응식의 경우 130ºC 부근에서의 열분해로 인해 생성된 탄소와 VOCl3가 반응함에 따라 VCl3의 형태로 침전되고 이때 ΔG값은 음의 값을 지니게 된다. 따라서 해당 반응식에 의해서 VOCl3가 제거되는 것 으로 판단되었다. 반면 Cu분말의 경우 그림 4(b)의 반응식 에 따르면 VOCl3로부터 Cl결합을 통해 염화구리(CuCl)을 형성하고, VOCl3은 Cl을 잃고 VOCl2를 형성하게 된다 [14]. 이렇게 생성된 생성물은 액상이 아닌 고상으로 존재 하여 증류를 통해 TiCl4로부터 분리된다. 그림 4(b)의 그래 프를 살펴보면 Cu 분말은 VOCl3뿐만 아니라 TiCl4과도 반응하여 TiCl3를 형성하므로 TiCl4 손실 가능성이 존재한 다. 하지만 TiCl4 대비 VOCl3과의 반응성이 더 우수하여 우선적으로 VOCl3제거가 가능하다. 그림 5는 Cu 분말을 이용한 VOCl3제거 실험 후 회수된 Cu분말의 결정상 변화 를 나타낸 결과이다. 그림 5의 XRD 결과 VOCl3이 제거 됨에 따라서 CuCl이 생성됨을 확인할 수가 있었으며, 뿐 만 아니라 앞의 실험 결과를 바탕으로 판단해 볼 때 Cu분 말을 이용하여 VOCl3 제거가 가능함을 확인하였다. 그림 4(c)의 agent별 주요 반응식과 표 2의 제거율을 비교하면 Cu 분말 대비 mineral oil이 VOCl3 제거에 우수하며, 특히 그림 4(c)에서와 같이 ΔG값이 음의 값을 지니며 안정적인 반응을 하고 있음을 확인할 수 있었다. ΔG값을 바탕으로 제거율을 예상하였을 때, Cu분말과 mineral oil의 제거율 차이는 미미할 것으로 예상되었다. 하지만 ΔG값은 반응 유무 및 가역-비가역을 판단하기 위한 것으로 실질적인 제 거율 및 반응속도는 ΔG값 외적인 요소들(반응물 상태, 반 응 표면적, 주변 요소간의 상호작용 등)에 기인하게 된다. 따라서 고체-액상 반응인 Cu 분말보다 액상-액상의 반응 인 mineral oil의 반응이 더욱더 우수하게 나타났으며, 최 적화를 위해 mineral oil을 이용하여 반응온도 및 시간, 첨 가량 변화에 따른 바나듐 제거 연구 실시하였다.
- Color of TiCl4 after removal of VOCl3 (Pure TiCl4, purified TiCl4 when using agent and crude TiCl4).
- Gibbs free energy for reaction using agent [4, 9, 14] (a) Mineral oil, (b) Cu powder, (c) possible reaction of Mineral oil and Cu powder.
- Cu 분말과 mineral oil의 VOCl3 제거율 비교 결과 mineral oil이 우수하였으며, 최적화를 위해 mineral oil을 이용하여 반응온도 및 시간, 첨가량에 따른 VOCl3 제거 거동을 확인하였다. 반응온도가 130ºC 일 때, mineral oil 첨가량(0.1, 0.15, 0.2 wt%) 및 시간(15, 30, 45, 60 min)에 대한 VOCl3 제거 거동을 살펴보았으며, 결과는 그림 6과 같이 나타내었다. 반응 시간 및 mineral oil 첨가량이 증가 함에 따라서 VOCl3 제거율이 증가하였으며, 0.2 wt%의 결 과에서는 시간에 관계없이 VOCl3 제거율이 100%로 나타 났다. 0.15 wt%의 조건에서는 45 min 이상의 반응하였을 때 제거율이 100%로 나타났으며, 0.1 wt%의 경우 시간이 증가함에도 VOCl3가 100% 제거되지 않았다. 0.1 wt% 조 건에서 시간이 증가함에 따라서 VOCl3 제거율은 증가하 였으나 반응시간 45 min 지남에 따라 더 이상 제거율이 증가하지 않는 것으로 보아, VOCl3 제거를 위한 mineral oil의 양이 부족한 것으로 판단되었다. 이를 바탕으로 VOCl3의 제거를 위해서는 0.15 wt% 이상의 mineral oil이 첨가되어야 하며, 단시간의 반응을 성립시키기 위해서는 0.2 wt%의 조건이 안정적임을 확인하였다. 추가적으로 반 응온도가 VOCl3 제거에 미치는 영향력을 알아보기 위해 반응온도 및 시간에 따른 VOCl3 제거 연구를 실시하였다. Mineral oil 첨가량에 따른 제거율을 바탕으로 mineral oil 의 첨가량은 1.5, 2 wt%로 진행하였으며, 반응온도(100, 110, 120, 130ºC) 및 시간(15, 30, 45, 60 min)에 따른 VOCl3 제거 거동 결과를 그림 7과 같이 나타내었다. 반응 온도 및 시간에 따른 VOCl3 제거 결과 그림 7에서 확인 할 수 있듯이 130oC 조건에서 1.5 wt%, 2 wt% 모두 제거 율이 가장 우수하였다. 반면 100oC의 경우 1.5 wt%, 2 wt% 조건에서 모두 20% 미만의 VOCl3 제거율을 나타남에 따 라 VOCl3 제거를 위한 온도로는 낮은 것으로 판단되었다. 또한 온도가 증가함에 따라 110oC에서 130oC로 증가함에 따라 제거율이 증가하였으며, 1.5 wt%의 경우 130ºC, 2 wt%는 120ºC 이상의 조건에서 VOCl3 제거율이 100%를 나타냈다. 이와 같이 온도 및 시간에 증가함에 따라서 제 거율이 증가하였으며, 시간 대비 온도 변수에 따른 제거율 변화폭이 큰 것으로 나타났다. 이는 온도가 증가함에 따라 mineral oil로부터 C의 분해속도가 빨라지게 되고, 분해된 C는 인해 VOCl3 제거 요소로 작용하게 된다. 따라서 VOCl3 제거 속도를 증가시키기 위해서는 빠른 C의 분해 가 필수적이다. 이를 바탕으로 VOCl3 제거 반응 속도를 증가시키기 위한 방법으로는 온도 증가가 적합한 것으로 판단되었다. 온도, 시간, 첨가량에 따른 VOCl3 제거 연구 결과, 효율성을 바탕으로 2 wt% mineral oil 첨가한 15분 의 조건을 최적 조건으로 선정하였고, 해당 시료를 이용하 여 Ti 제조에 적용하고자 하였다.
- Removal efficiency of VOCl3 with variation of the contents of mineral oil at the reaction temperature of 130ºC.
- 3.2 열환원을 이용한 Ti 분말 합성 거동
- 위의 연구 결과를 바탕으로 VOCl3이 제거된 TiCl4을 회 수하였으며, 이를 활용하여 Ti 분말 제조 연구를 실시하였 다. 플라즈마의 경우 고비용이 소요되므로 수소 열활원 공 정을 이용한 Ti 분말 합성 거동을 확인하였다. 수소의 경 우 폭파가능성이 존재하고 TiCl4와 반응 시 그 위험이 커 질것으로 판단되어 수소와 알곤 혼합가스를 이용하여 합 성 연구를 실시하였다. 열환원 공정을 통해 합성된 Ti분말 의 경우 TiCl4과 수소간의 빠른 반응성으로 인해 수um 단 위의 분말이 합성될 것으로 예상하였으며, 회수하는 과정 에서 자연 발화 가능성이 존재하였다. 자연 발화 현상은 일정 크기 이하의 금속분말이 산소와의 급격한 접촉으로 인해 나타나는 현상으로, 특히 Ti의 경우 약 3 um 이하에 서 자연발화가 발생하게 된다[15, 16]. 따라서 합성된 Ti 분말의 경우 자연 발화를 방지하고, 표면에 얇은 산화막 형성을 위해 에탄올을 통해 포집을 하였다. 그림 8은 포집 된 Ti 분말로써 구형의 형태를 지녔으며 3 um 이하의 입 도를 가진 것으로 확인되었다. 또한 내부와는 다르게 표면 에 흰색의 얇은 막이 형성된 것으로 보아, 에탄올을 이용 하여 포집함에 따라 Ti 분말 표면에 얇은 산화막이 형성 된 것으로 판단되었다. Ti 분말의 명확한 표면 산화 여부 를 판단하기 위한 Energy dispersive spectrum(EDS)를 이 용하여 성분분석을 실시하였으며, 표 3과 같이 나타났다. 표 3의 결과 회수된 Ti 분말은 Ti와 O 구성되었으며, 분 말의 표면만 분석함에 따라 O의 함량이 높음을 확인할 수 가 있었다. 또한 표면에 산화막이 형성됨에 따라 Ti의 자 연발화가 억제됨을 확인하였다. 이렇게 형성된 분말의 크 기 분포를 확인하기 위해 PSA를 분석을 실시하였으며, 합 성된 Ti는 1~3 um의 입도 분포를 지니고 있었다. 1~3 um 의 분포를 지니는 Ti 분말의 경우 자연 발화 가능성이 입 자 분포로 에탄올에 포집됨에 따라 자연 발화가 발생하지 않았으며, 에탄올과의 반응에 따라 표면에 얇은 산화막이 형성됨이 확인되었다. 구형의 입자 형성과 1~3 um의 입자 분포를 지니는 것으로 보아, 수소와 TiCl4간의 반응은 격 렬히 일어났으며, 열환원 공정을 이용하여 Ti 분말을 합성 가능성을 확인하였다. 그림 9
3. 결과 및 고찰
3.1.1 Agent별 VOCl3 제거 거동 확인
Fig 3


Fig 4


3.1.2 반응 온도/시간 및 첨가량에 따른 바나듐 제거 연구
Fig 6


- TiCl4 내의 VOCl3를 제거하기 위해 Cu 분말 및 mineral oil을 이용한 불순물 제거 연구를 실시하였다. Cu 분말과 mineral oil의 VOCl3 제거를 위한 열역학적 거동을 비교하 였으며 Cu 분말 대비 mineral oil을 사용하였을 때 안정적 인 ΔG값을 가지는 것을 확인할 수가 있었다. 이를 바탕으 로 Cu 분말과 mineral oil의 제거율은 비교한 결과 mineral oil이 우수함을 확인할 수가 있었다. Mineral oil을 이용한 VOCl3 제거 효율을 향상시키기 위해 온도/반응시간/첨가 량에 따른 VOCl3 제거 거동을 확인하였다. 그 결과 1.5 wt% 이상의 조건에서 100%의 VOCl3 제거가 가능하였으 며, 2 wt%의 함량에서 15 min/ 130ºC의 조건일 때 반응 효 율이 가장 우수하며, VOCl3이 100% 제거되었다. 최종적 으로 2 wt%의 조건을 바탕으로 scale-up 실험을 실시한 결 과, 본 연구와 동일한 결과를 얻을 수 있었다. 뿐만 아니 라 mineral oil을 사용함에 따라 발생하는 residue는 향후 열전달 방해요소로 작용할 수가 있다. 따라서 scale-up에 따른 공정 추가 및 수정을 진행함으로써 문제를 해결하고 자 하였다. 잔류 residue의 경우 점성이 높으므로 잔류하 는 소량의 TiCl4와 함께 배출 후 폐기 처리함에 따라 향후 공정상에 열전달 방해요소로 작용하지 않았다. 또한 정제 된 TiCl4를 이용하여 수소 열환원 공정을 이용한 Ti 분말 합성 연구를 실시하였다. 회수된 분말은 최종적으로 1~3 um의 입자분포를 보였으며, 빠른 반응에 의해 구형의 형 태를 지니는 것으로 확인되었다. 따라서 VOCl3 제거 공정 을 바탕으로 정제된 TiC4을 이용하여 수소 열환원을 실시 하였으며 Ti 분말 합성가능성을 최종적으로 확인 할 수 있 었다.
4. 결 론
-
Acknowledgements
- 2019년도 산업통상자원부의 재원으로 한국산업기술평 가관리원의 지원을 받아 수행된 연구임(No.10052719, 산 업핵심기술개발사업).
Acknowledgement
- 1. G. G. Lee, S. K. Jo, M. S. Choi, J. Y. Jung and M. C. Kim: Trends in Metals & Materials Engineering, 22 (2009) 19..
- 2. S. D. Choi, S. Y. Hwang, J. Y. Jung and M. C. Kim: Trends in Metals & Materials Engineering, 21 (2008) 17..
- 3. Y. T. Lee and D. G. Lee: Trends in Metals & Materials Engineering, 21 (2008) 8..
- 4. L. Hockaday and A. Kale: Tenth International Heavy Minerals Conference, 1 (2016) 63..
- 5. H. H. Schaumann: USA, US2689781A (1954)..
- 6. A. Kale and K. Bisaka: J. South Afr. Inst. Min. Metall., 111 (2011) 193..
- 7. E. W. Nelson: USA, US3495383A (1970)..
- 8. G. J. Dooley III: JOM, 27 (1975) 8..Article
- 9. S. Xiong, Z. Yuan, Z. Yin and W. Yan: Hydrometallurgy, 119 (2012) 16..Article
- 10. J. Goddard and M. Litwin: USA, US20020179427A1 (2002)..
- 11. G. Sironi, R. Sacerdote and F. Ferrero: USA, US3627481A (1971)..
- 12. A. B. Murphy: J. Phys. D: Appl. Phys., 37 (2004) 2841..Article
- 13. M. Horikawa, A. Matsuda and T. Kamiya: Japan, JP3734687B2 (2000)..
- 14. X. Wang, L. Zhang, G. Shang, G. Zhang, J. Yuan and S. Gong: Hydrometallurgy, 99 (2009) 259..Article
- 15. J. K. Park and J. P. Ahn: J. Korean Powder Metall. Inst., 9 (2002) 1..Article
- 16. J. H. Park, D. W. Lee and J. Kim: J. Korean Powder Metall. Inst., 17 (2010) 385..Article
Figure & Data
References
Citations
Citations to this article as recorded by 

Study on Manufacture of High Purity TiCl4 and Synthesis of High Purity Ti Powders
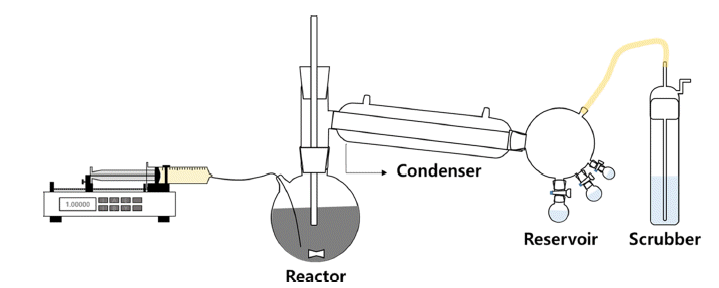








Fig 1
TiCl4 refining system for removal VOCl3.
Fig 2
Schematic diagram of Ti powder synthesis apparatus.
Fig 3
Color of TiCl4 after removal of VOCl3 (Pure TiCl4, purified TiCl4 when using agent and crude TiCl4).
Fig 4
Gibbs free energy for reaction using agent [4, 9, 14] (a) Mineral oil, (b) Cu powder, (c) possible reaction of Mineral oil and Cu powder.
Fig 5
XRD data of Cu powder after removing VOCl3.
Fig 6
Removal efficiency of VOCl3 with variation of the contents of mineral oil at the reaction temperature of 130ºC.
Fig 7
Reaction temperature dependent removal efficiency of VOCl3: (a) 1.5 wt%, (b) 2 wt%.
Fig 8
Surface morphology of synthesizeds Ti powder.
Fig 9
Size distribution of synthesized Ti powder.
Fig 1
Fig 2
Fig 3
Fig 4
Fig 5
Fig 6
Fig 7
Fig 8
Fig 9
Study on Manufacture of High Purity TiCl4 and Synthesis of High Purity Ti Powders
Table 1
Specification of purifying agent for VOCl3
Table 2
Comparison of removal efficiency of VOCl3 using Cu powder and mineral oil
Table 3
Composition of synthesized Ti powder
Table 1
Table 2
Table 3
TOP
 KPMI
KPMI










 Cite this Article
Cite this Article