Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 26(6); 2019 > Article
-
ARTICLE
난각으로부터 합성된 초미립 CaO 분말을 이용한 C3S, C2S, C3A 분말 합성 및 혼합 경화체에 미치는 C3A 함량의 영향 - 공헌a, 권기범b, 박상진b, 노효섭b, 이상진a,c,*
- Synthesis of C3S, C2S, C3A Powders using Ultra-fine Calcium Oxide Powder Synthesized from Eggshell and Effect of C3A Content on Hardened Mixed Aggregates
- Heon Konga, Ki-Beom Kwonb, Sang-Jin Parkb, Whyo-Sub Nohb, Sang-Jin Leea,c,*
-
Journal of Korean Powder Metallurgy Institute 2019;26(6):493-501.
DOI: https://doi.org/10.4150/KPMI.2019.26.6.493
Published online: November 30, 2019
a 국립목포대학교 세라믹산업기술연구소
b 드림소재(주)
c Department of Advanced Materials and Engineering, Mokpo National University, Muan 58554, Republic of Korea
a The Research Institute of Ceramic Industry Technology in Mokpo National University, Muan 58554, Republic of Korea
b Research Center, Dreamsojae Co., Ltd, Mokpo 58618, Republic of Korea
c 국립목포대학교 신소재공학과
- *Corresponding Author: Sang-Jin Lee, TEL: +82-61-450-2493, FAX: +82-61-450-2498, E-mail: lee@mokpo.ac.kr
- - 공 헌: 실장, 권기범: 과장, 박상진: 대리, 노효섭: 대표이사, 이상진: 교수
© The Korean Powder Metallurgy Institute. All rights reserved.
- 1,332 Views
- 18 Download
Abstract
- In this work, ultra-fine calcium oxide (CaO) powder derived from eggshells is used as the starting material to synthesize mineral trioxide aggregate (MTA). The prepared CaO powder is confirmed to have an average particle size of 500 nm. MTAs are synthesized with three types of fine CaO-based powders, namely, tricalcium silicate (C3S), dicalcium silicate (C2S), and tricalcium aluminate (C3A). The synthesis behavior of C3S, C2S and C3A with ultra-fine CaO powder and the effects of C3A content and curing time on the properties of MTA are investigated. The characteristics of the synthesized MTA powders are examined by X-ray diffraction (XRD), field emission-scanning electron microscope (FE-SEM), and a universal testing machine (UTM). The microstructure and compressive strength characteristics of the synthesized MTA powders are strongly dependent on the C3A wt.% and curing time. Furthermore, MTA with 5 wt.% C3A is found to increase the compressive strength and shorten the curing time.
- 치과용 충전 재료는 소재 자체 독성이 없고, 조직액에 용해가 없으며, 습윤한 환경에서의 우수한 밀폐효과가 있 는 등 생체친화성이 뛰어나야 한다[1]. 치수복조술의 전통 적인 재료인 수산화칼슘(Calcium hydroxide, Ca(OH)2)은 시간경과에 따라 수용성에 기인한 용해와 미세누출이 발 생되는 단점을 가지고 있다[2]. 이에 대한 대체재로 사용 되는 Mineral Trioxide Aggregate(MTA)는 1990년대 미국 Loma Linda 치과대학의 Torabinejad에 의해 고안되었으며, 근관치료 시술의 치근단 역충전 재료로 개발되었다[3-6]. 이후 미국 특허 및 Federal Drug Administration(FDA) 인 증이 완료되어 ProRoot MTA라는 상품이 출시되었다.
- MTA는 기본적으로 포틀랜드 시멘트(Portland cement)의 유독성 금속복합체를 배제한 후 제작되기 때문에 포틀랜 드 시멘트와 주요 성분이 동일하다. MTA는 3가지 필수 성분인 정제된 포틀랜드 시멘트와 방사선 불투과를 위한 조영제의 혼합물로서, 규산삼칼슘(tricalcium silicate, C3S), 규산이칼슘(dicalcium silicate, C2S), 알루민산삼칼슘 (tricalcium aluminate, C3A), 산화비스무트(bismuth oxide) 로 구성된다[7]. MTA는 치근 천공 재료로 적용 시, Intermediate Restorative Material(IRM)이나 아말감에 비해서 미세 누출이 적어 색소의 침투가 적고, 과충전 경향이 낮 음이 보고된 바 있다[8]. 이러한 특성이 보고된 후, MTA 는 치수복조술(pulp capping), 치수절단술(pulpotomy), 치 근단유도술(apexogenesis)과 더불어 천공치료(perforation repair) 및 이상 근관 충전재까지 치과용 재료로 폭넓게 적 용되고 있다[9]. 이처럼 MTA는 뛰어난 항균성, 밀폐성과 더불어 생체적합성이 우수한 재료로서, 다양한 치과용 제 품으로의 개발이 활발히 진행되고 있다. 하지만 MTA는 고 가이면서 조작성이 떨어지고, 긴 경화시간으로 인하여 광 범위한 치과용 재료로의 응용에 한계점을 보이고 있다[10].
- 우수한 물성의 MTA 제조를 위하여 반응성이 뛰어난 C3S, C2S, C3A 분말이 필수이며, 이러한 분말의 합성은 기존 고상 분말합성법으로는 합성이 원활히 이루어지지 않아 용융 후 급랭시키는 방법이 사용되고 있다. 하지만, 이 경우, 공정이 까다롭고 분말의 수율이 낮아 양산화에 문제가 따르게 된다.
- 본 연구에서는 MTA의 주요성분인 C3S, C2S, C3A 분 말합성 제조 시 가장 많은 양을 사용하는 산화칼슘(Calcium oxide, CaO) 분말을, 저가이면서 공급이 수월한 난각 (eggshell)을 이용하여 초미립 CaO 분말을 제조 후 이를 기존 상업용 CaO 대신 사용하였다. 반응성이 뛰어난 초미 립 CaO 분말을 사용함으로써 용융없이 고상 분말합성 방 법으로 C3S, C2S, C3A 분말합성이 가능함을 고찰하였다. 제조공정을 통하여 초미립 CaO 분말을 기반으로 제작된 C3S, C2S, C3A 합성분말의 구조 특성을 평가하였고, 이 들로 이루어진 MTA 경화체를 제조하였다. 이때, C3A 함 량 및 경화시간에 따른 MTA의 미세구조, 압축강도 평가 를 통하여 물리적 성질 변화를 고찰하였다.
1. 서 론
- 2.1 난각을 이용한 초미립 CaO 분말 제조
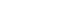
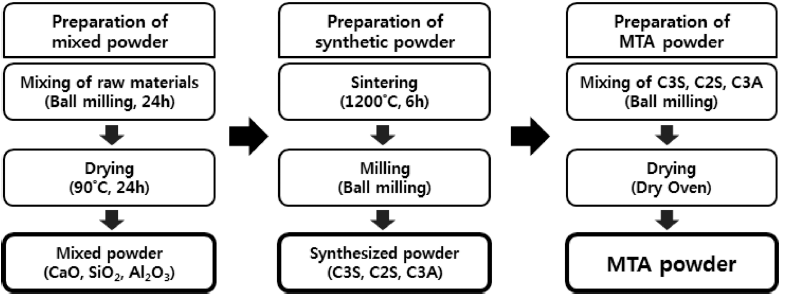
- 난각 기반 초미립 CaO 분말을 제조하기 위한 공정도는 그림 1과 같다. 먼저 난각을 미온수와 베이킹소다를 사용 하여 세척을 진행하였다. 세척 완료 후, 난막과 같은 유기 물이 탄화되지 않는 온도인 100°C에서 24시간 동안 건조 를 진행하였다. 건조 완료된 난각은 알루미나 도가니에 넣 어 3°C/min로 1000°C에서 2시간 동안 열처리하였다. 일반 적으로 난각은 대부분 CaCO3로 구성되어 있고 CaCO3의 열분해 온도는 일반적으로 900°C로 알려져 있으며, 그 반 응식은 다음과 같다[12, 13].
- 최종적으로 열처리 완료된 난각은 3 mm 지르코니아 볼 과 비수계 용매(98% Ethanol, 99.5% IPA 등)를 사용하여 볼밀링 방법(350 RPM / 12h)으로 분쇄 후 초미립 CaO 분 말을 제조하였다. 일반적으로 Calcium oxide는 물과 반응 하여 수산화칼슘(Ca(OH)2)을 생성하기 때문에 볼밀링 진 행 시 비수계 용매를 사용하여야 한다[14, 15].
- 2.2 C3S, C2S, C3A 합성분말 제조
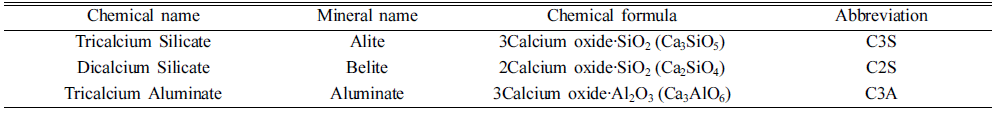
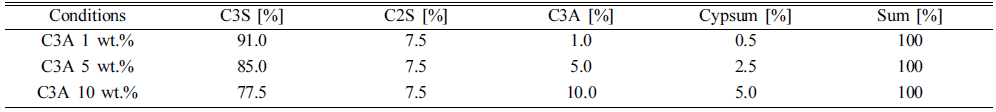
- MTA의 기본 구성 물질인 C3S, C2S, C3A 합성분말은 난각으로부터 제조된 초미립 CaO 분말을 사용하였다. 본 연구에서 합성하고자 하는 물질인 C3S, C2S, C3A는 각각 3CaO·SiO2, 2CaO·SiO2, 3CaO·Al2O3와 같은 화학식으로 표기된다. C3S, C2S, C3A 합성분말에 대한 화학명, 광물 명, 화학식, 약호는 표 1에 나타내었다. 또한 MTA 분말을 제조하기 위한 공정도는 그림 2에 나타내었다. 각각의 C3S, C2S, C3A 분말을 제조하기 위하여, 첫 번째로 난각 으로부터 제조된 초미립 CaO 분말과 상용 SiO2(Sigmaaldrich, 99%, 1~5 μm), Al2O3 분말(KC, 99%, 0.6~1 μm)을 주요 성분으로 하여 3 mm 지르코니아 볼과 비수계 용매 (IPA)를 사용하여 300 rpm으로 24시간 동안 볼밀링 방법 으로 혼합하였다. 이 후 혼합된 각 C3S, C2S, C3A 분말 들은 90°C에서 24시간 동안 건조를 진행하였으며, 1200°C 온도에서 6시간 유지하여 열처리를 진행하였다. 제조된 각 C3S, C2S, C3A 분말과 소량의 석고 분말을 볼밀링 방 법으로 혼합하여 최종적으로 MTA 분말을 제조하였다. C3A 분말은 수화반응이 가장 빠르기 때문에 너무 빨리 굳 어 사용하기 어렵다. C3A 분말의 수화속도를 해결하기 위 하여 C3A 분말의 수화 억제 효과를 나타내는 석고 분말 을 소량 첨가하였으며, 첨가된 석고 분말은 C3A 분말 대 비 50 wt.%로 하였다. C3A 첨가효과를 알아보기 위하여 C3S, C2S, C3A 합성분말 내의 C3A 분말의 함량을 1, 5, 10 wt.%로 증가시켜 각각 다르게 제조하였으며, 경화시간 은 1, 3, 5일로 변화 시켰다. C3A 분말의 함량변화에 따 른 조성은 표 2에 나타내었다. 비교실험을 위하여 상업용 시약급 CaO 분말을 사용하여 C3S, C2S, C3A를 합성 후 그 결과를 비교·분석하였다.
- 2.3 특성분석
- 난각을 사용하여 제조된 초미립 CaO 분말과 상용 CaO 분말의 미세구조는 전계방출주사전자현미경(FE-SEM, JEOL, JSM-7100F)을 사용하여 분석하였고, 합성된 CaO 분말의 결정상은 X선 회절분석기(XRD, PANalytical, X'Pert PRO Multi Purpose X-Ray Diffractometer)를 사용 하여 10°~90° 범위에서 측정하였다. 난각 기반 초미립 CaO 분말과 상용 CaO 분말의 성분 분석을 위하여 EDAX(EDX, Horiba, EX-200), XPS(XPS, VG, Multilab- 2000) 분석을 진행하였다. 초미립 CaO 분말의 입도분포는 입도분석기(Beakman, LS 13 320)를 사용하여 3회 측정한 평균값을 도출하였다. 또한, C3S, C2S, C3A 분말들의 결 정상은 X선 회절 분석기를 사용하여 10°~90° 범위에서 분 석하였다. C3S, C2S, C3A 분말들을 혼합한 MTA 합성분 말에서의 C3A 함량 및 경화시간에 따른 미세조직 관찰을 위하여 전계방출주사전자현미경을 사용하였으며, 압축강 도 변화를 관찰하기 위하여 만능재료시험기(R&B, RB 301 Unitech T)를 사용하였다. 압축강도는 지름 10 mm에 두께 5 mm 크기의 시편을 사용하였다. 정확한 분석을 위 하여 각 조건별로 5개의 시료를 측정하여 평균값을 계산 하여 비교 분석하였다.
2. 실험방법
Flow chart of diverse steps involved in the manufacture of ultra fine CaO powders derived from eggshells.
- 난각으로부터 합성된 CaO 분말과 상용 CaO 분말의 미 세구조 분석 결과를 그림 3에 나타내었다. 난각으로부터 합성된 CaO 분말의 경우(그림 3 (a)), 분말은 대략 500 nm 크기의 분말들과 분말들끼리 응집된 형태를 보인다. 또한, 상용 CaO 분말의 경우(그림 3 (b)), 수 μm에서 수십 μm의 분말들이 angular 형태로 불균일하게 분포하고 있다. 난각 으로부터 합성된 CaO 분말은 상용 CaO 분말과 비교하여 입자 사이즈가 작아 비표면적이 우수하다고 할 수 있다.
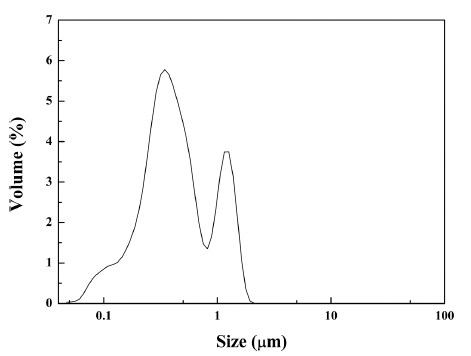
- 난각으로부터 합성한 CaO 분말의 입도분석 결과는 그 림 4에 나타내었다. 입도분석 결과 D50 기준 500 nm의 입 자크기를 나타내어, 초미립 CaO 분말이 제조되었음을 확 인할 수 있었다. 입도분포의 경우 400~500 nm와 1.0~1.5 μm 부근에서 bimodal 분포를 나타내는데 이는 합성된 분 말의 분쇄시간이 충분하지 않아 부분적 응집이 발생하여 나타난 현상으로 판단된다. 그림 4
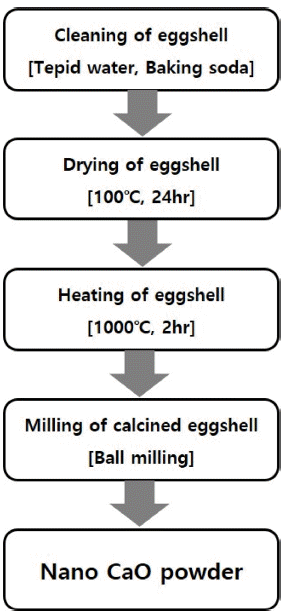
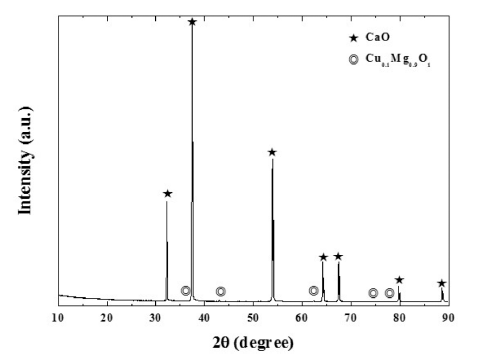
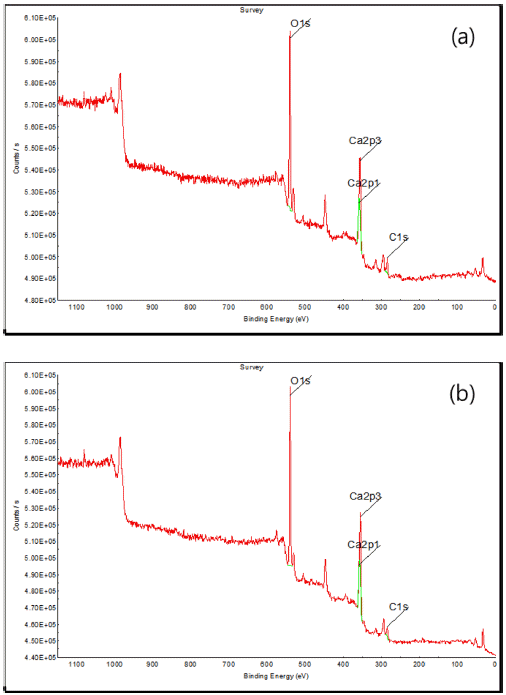
- 그림 5는 난각으로 제조된 초미립 CaO 분말의 XRD 분 석 결과이다. 결정상 분석 결과 주피크인 CaO 피크와 극 미량의 Cu0.1Mg0.9O1 피크가 동시에 확인되었다. CaO 피 크는 32.2°, 37.4°, 53.9°, 64.2°, 67.4°, 79.7°, 88.6°에서 나 타났으며, Cu0.1Mg0.9O1 피크는 36.9°, 42.9°, 62.3°, 74.7°, 78.6°에서 나타났다. 검출된 극미량의 Cu0.1Mg0.9O1 존재 유무를 명확하게 확인하기 위하여 상용 CaO 분말과 난각 으로 제조한 CaO 분말에 대하여 EDAX 분석과 XPS 분 석을 진행하였다. EDAX 분석결과를 그림 6에 나타내었 다. EDAX 분석결과 상용 시약급 CaO 분말과 난각으로 제조한 CaO 분말 모두 Ca, O만 검출되었고, Cu, Mg 성 분은 검출되지 않았다. XPS 분석결과를 그림 7에 나타내 었으며, XPS 분석 결과 EDAX 분석결과와 마찬가지로 상 용 CaO 분말과 난각으로 제조한 CaO 분말 모두 Ca, O만 검출되었고, Cu, Mg 성분은 검출되지 않았다. EDAX 분석 과 XPS 분석 결과를 바탕으로 Cu0.1Mg0.9O1 물질은 존재하 지 않는 것으로 판단되며, XRD 검출 오류로 판단된다.
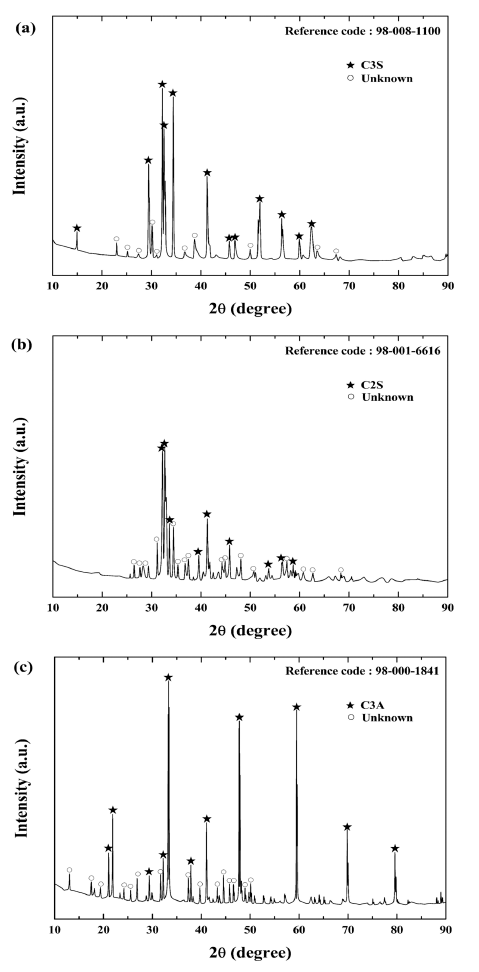
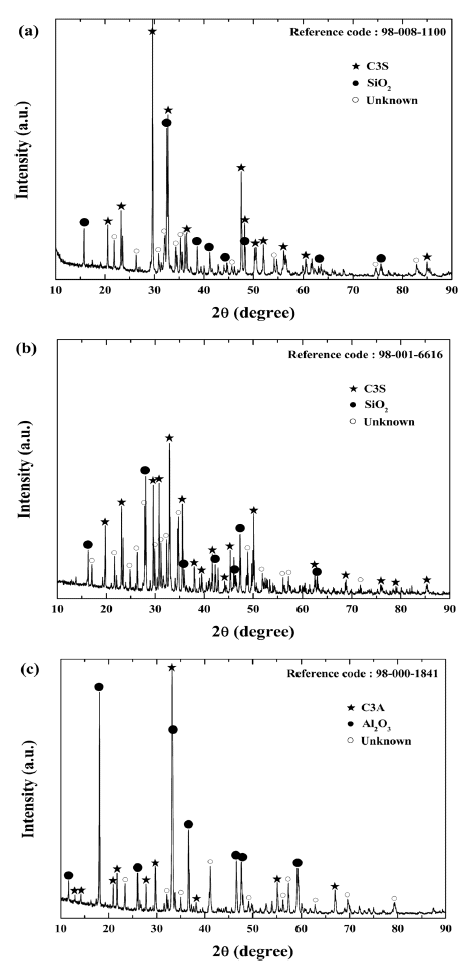
- C3S, C2S, C3A 합성분말은 제조된 초미립 CaO 및 상 용 CaO 분말과 상용 SiO2, Al2O3 분말을 혼합하여 제조하 였다. 난각으로부터 제조된 초미립 CaO 분말을 이용하여 제조된 C3S, C2S, C3A 합성분말에 대한 XRD 분석 결과 는 그림 8에 나타내었다. XRD 분석 결과 그림 8 (a), (b), (c)에 해당하는 피크는 각각 3CaO·SiO2(Ca3SiO5), 2CaO· SiO2(Ca2SiO4), 3CaO·Al2O3(Ca3Al2O6)로 확인되었다. 또한 미 반응된 CaO, SiO2, Al2O3 결정상들이 관찰되지 않은 것 으로 보아 MTA를 구성하는 C3S, C2S, C3A 물질이 잘 합 성된 것을 확인할 수 있었다. 상용 CaO 분말을 이용하여 제조된 C3S, C2S, C3A 합성분말에 대한 XRD 분석 결과 는 그림 9에 나타내었다. 분말의 입도분포가 넓고 초미립 사이즈가 아닌 상업용 CaO 분말을 사용할 경우, 미 반응 된 SiO2, Al2O3 결정상들이 관찰되었다. 두 경우 모두 unknown 결정상이 검출되는데, 이것은 종래의 용융법으 로 제조된 경우에도 피할 수 없는 현상으로, 화학양론적인 결정상을 얻는 것은 사실상 불가능 한 것으로 알려져 있 다[10].
- 합성된 초미립 CaO 기반 C3S, C2S, C3A 합성분말로 이루어진 MTA 분말에 대하여 C3A 함량 및 경화시간이 특성변화에 미치는 영향을 평가하였다. C3A 함량은 기존 MTA 조성에서 1, 5, 10 wt.% 추가로 변화시켰고, 각 C3A 함량 변화에 따른 샘플들의 경화시간은 1, 3, 5 일로 변화 시켰다. 그림 10은 C3A 함량 및 경화시간 변화에 따른 FE-SEM 이미지를 나타낸다. 미세구조 분석 결과, C3A 1 wt.%인 경우에는 입자모양이 불규칙한 형상을 나타내고 있었으며, 경화시간이 증가할수록 미세조직이 점차 치밀 해지는 경향성을 나타내었다(그림 10 (a)~(c)). C3A 4 wt.%인 경우에는 불규칙한 입자형상을 나타내고 있었으며, 경화시간이 증가함에 따라 미세하게 치밀도가 증가하는 형상을 나타내었으나 거의 유사한 미세구조를 나타내었다 (그림 10 (d)~(f)). 특이하게 C3A 5 wt.%의 경화시간 1일 차의 미세조직과 C3A 1 wt.%의 경화시간 5일차의 미세조 직이 매우 유사한 형상을 나타내었다. C3A 10 wt.%인 경 우에는 경화시간 1일부터 5일까지의 모든 샘플에서 침상 및 판상 형상이 다량 존재하였으며, 경화시간이 증가함에 따라 점차 미세조직이 치밀해지는 경향성을 나타내었다( 그림 10 (g)~(i)). 이는 C3A의 수화는 석고(CaSO4·2H2O) 존재에 따른 C3A-CaSO4-H2O계 복염을 생성하게 되고, C3A-CaSO4-H2O계 복염은 Trisulfate형인 C3A·3CaSO4· 32H2O와 Monosulfate형인 C3A·CaSO4·12H2O의 2종으로 존재하기 때문으로 사료된다[16]. 전자인 Trisulfate형은 침 상, 후자인 Monosulfate형은 육각판상의 형상을 나타낸다. 특히, Trisulfate는 Ettringite라고도 불리며, 천연에서도 산 출된다.
- 그림 11은 C3A 함량이 1, 5, 10 wt.%로 제조된 MTA 분 말의 경화시간 1, 3, 5일 변화에 따른 압축강도 변화를 나 타낸다. 경화시간이 1일에서 5일까지 경과함에 따라, C3A 1 wt.% 샘플은 8.83, 9.38, 14.42 MPa로 변화하였고, C3A 5 wt.% 샘플은 15.1, 14, 15.5 MPa로 변화하였으며, C3A 10 wt.% 샘플은 5.96, 6.9, 9.77 MPa로 변화하였다. 이렇게 강도가 증가하는 경향은 C3A를 첨가함으로써 일반적으로 발현되는 현상이지만, 초미립 CaO 분말을 이용하여 제조 된 MTA는 이러한 현상이 더욱 두드러지는 결과를 보였다.
- 압축강도 분석결과는 C3A 함량 변화와 경화시간 변화 에 따른 두 가지 결과로 나눠 고찰해 볼 수 있다. 먼저, C3S, C2S, C3A 합성분말에서 C3A 함량 변화가 미치는 영향은, C3A 함량이 5 wt.%일 때 가장 높은 압축강도 특 성을 나타내었으며, C3A 함량이 10 wt.%로 증가한 경우 에 가장 낮은 압축강도 특성을 나타내었다. 즉, C3A 함량 이 1 wt.%에서 5 wt.%로 증가한 경우 압축강도도 증가하 는 경향성을 나타내었으나, 5 wt.%에서 10 wt.%로 증가한 경우에는 오히려 압축강도가 감소하는 경향성을 나타내었 다. 일반적으로 석고 양이 과잉되면 Ettringite의 양이 많아 져서 조직을 팽창시키고, 오히려 강도발현을 저해하게 된 다. 따라서, C3A 함량 10 wt.%의 경우 석고 분말의 첨가 량 또한 상대적으로 증가하여 석고의 양이 많은 상태이기 때문에 Ettringite 양의 증가에 따른 강도발현이 저해되었 기 때문으로 판단된다. 다음으로 C3S, C2S, C3A 합성분 말에서 경화시간 변화가 미치는 영향은, 경화시간이 증가 할수록 압축강도는 전반적으로 증가하는 경향성을 나타내 었다. C3A 1 wt.%와 10 wt.%인 경우에는 5일차에 급격한 압축강도 증가를 나타내어 각각 14.4, 9.8 MPa의 압축강도 값을 나타내었다. 이에 반해 C3A 5 wt.%인 경우에는 1일 에서 5일까지 약 14~15.5 MPa의 압축강도 값을 나타내어 유사한 값을 보였다. 위에서 언급한 C3A 함량 및 경화시 간 변화에 따른 압축강도 결과는 그림 10에서 제시한 미 세구조와 치밀도 이미지와 잘 일치하였다. MTA 분말의 주요성분인 C3S, C2S, C3A 합성분말에서 C3A 함량 및 경화시간 변화가 압축강도에 미치는 결과를 종합적으로 판단하였을 때, C3A 5 wt.% 첨가한 샘플은 경화시간을 1 일 이내로 빠르게 단축시키는 효과와 더불어 미세한 압축 강도 증가 효과도 있는 것으로 판단된다.
3. 결과 및 고찰
EDAX spectra of (a) ultra fine CaO powder derived from eggshell and (b) commercial CaO powder.
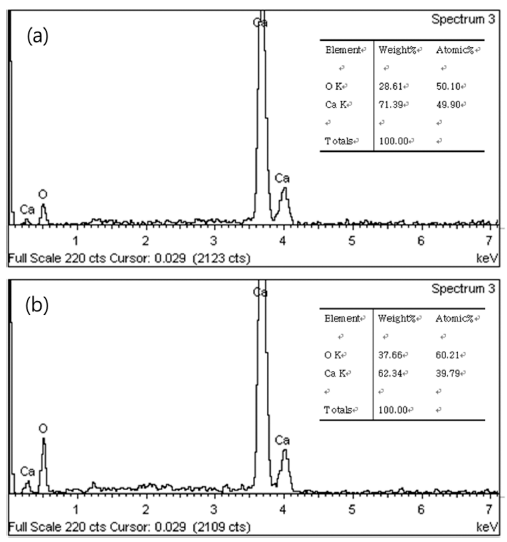
XRD patterns of (a) C3S, (b) C2S and (c) C3A powders synthesized using synthesized ultra fine CaO powder.
Compressive strength of various MTA specimens with three types of C3A contents (1, 5 and 10 wt.%) as a function of different curing times (1, 3 and 5 days).

- 난각으로부터 제조된 초미립, 고순도의 CaO 분말을 활 용하여 MTA의 필수 구성성분인 C3S, C2S, C3A 합성분 말을 제조하였다. 상업용 CaO 분말을 사용하였을 경우에 비하여 미반응 결정상이 관찰되지 않았다. 제조된 각각의 C3S, C2S, C3A 합성분말과 소량의 석고 분말을 혼합하여 MTA 분말을 제조하였다. 최종적으로 MTA 분말에 대하 여 C3A 함량(1, 5, 10 wt.%) 및 경화시간(1, 3, 5일) 변화 에 따른 물리적 특성 변화를 고찰하였다. MTA 분말의 미 세구조는 경화시간이 증가함에 따라 점차 치밀해지는 경 향을 보였으며, C3A 함량이 5 wt.%에서 가장 치밀함을 보 였다. MTA 분말의 압축강도는 경화시간이 증가함에 따라 전반적으로 증가하는 경향을 보였으며, C3A 함량이 5 wt.%에서 가장 높은 값을 보였다. C3A 함량이 10 wt.% 로 다른 실험조건 대비 상대적으로 높은 샘플에서는 침상 (Trisulfate형, C3A·3CaSO4·32H2O) 및 판상(Monosulfate형, C3A·CaSO4·12H2O) 형상의 존재가 확인되었으며, 가장 낮 은 압축강도를 보였다. 이는 C3A의 수화 시 석고 존재에 따른 C3A-CaSO4-H2O계 복염 생성과 석고 분말 첨가량 증가에 따른 Ettringite 양 증가로 강도발현의 저해에 기인 한다고 판단된다. 이와 같은 결과를 바탕으로 C3A를 5 wt.% 첨가한 경우, 경화시간을 1일 이내로 매우 빠르게 단 축시키는 효과를 확인하였으며, 압축강도 또한 미세한 증 가 효과가 있음을 확인하였다.
4. 결 론
-
Acknowledgements
- 본 연구는 전남테크노파크에서 지원하는 지역수요맞춤 형연구개발사업 연구개발성과사업화지원사업(No. B00812 14000214) 연구비 지원으로 수행되었습니다.
감사의 글
- 1. M. Torabinejad and M. Parirokh: J. Endod., 36 (2010) 190. .ArticlePubMed
- 2. Y. H. Song, N. Y. Lee, S. H. Lee and M. K. Jih: J. Korean Acad. Pediatr. Dent., 45 (2018) 344. .Article
- 3. M. Torabinejad, C. U. Hong, S. J. Lee, M. Monsef and T. R. Pitt Ford: J. Endod., 21 (1995) 603. .Article
- 4. G. Bogen and S. Kuttler: J. Endod., 35 (2009) 777. .ArticlePubMed
- 5. M. A. H. Duarte, M. A. Marciano, R. R. Vivan, M. T. Filho, J. M. G. Tanomaru and J. Camilleri: Braz. Oral Res., 32 (2018) 111. .ArticlePubMed
- 6. Y. B. Cho: Kor. J. Dent. Mater., 42 (2015) 51. .Article
- 7. H. J. Moon, J. H. Lee, J. H. Kim, J. C. Knowles, Y. B. Cho, D. H. Shin, H. H. Lee and H. W. Kim: J. Tissue Eng., 9 (2018) 1. .ArticlePubMedPMC
- 8. D. J. Kim, J. H. Cho, E. J. Gwak, W. S. Park, B. Y. Jung, K. D. Kim and N. S. Pang: J. Korean Academy of Advanced General Dentistry, 5 (2016) 67. .
- 9. M. Parirokh and M. Torabinejad: J. Endod., 36 (2010) 16. .ArticlePubMed
- 10. J. Lim, J.-G. Guk, B. Singh, Y.-C. Hwang, S.-J. Song and H.-S. Kim: J. of the Kor. Ceram. Soc., 56 (2019) 403. .Article
- 11. L. Habte, N. Shiferaw, D. Mulatu, T. Thenepalli, R. Chilakala and J. W. Ahn: Sustainability, 11 (2019) 3196. .Article
- 12. S. Lin, T. Kiga, Y. Wang and K. Nakayama: Energy Procedia, 4 (2011) 356. .Article
- 13. R. S. Putra, A. Liyanita, N. Arifah, E. Puspitasari, Sawaludin and M. N. Hizam: Energy Procedia, 105 (2017) 289. .Article
- 14. H. Ogura, T. Yamamoto, H. Kage, Y. Matsuno and A. S. Mujumdar: Chem. Eng. J., 86 (2002) 3. .Article
- 15. I. Fujii, K. Tsuchiya, M. Higano and J. Yamada: J. Sol., 34 (1985) 367. .Article
- 16. J. Havlica and S. Sahu: Cement Concrete Res., 22 (1992) 671. .Article
Figure & Data
References
Citations

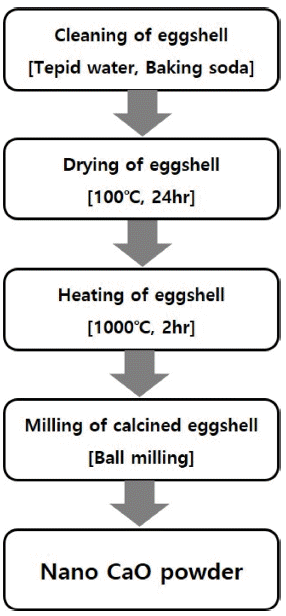
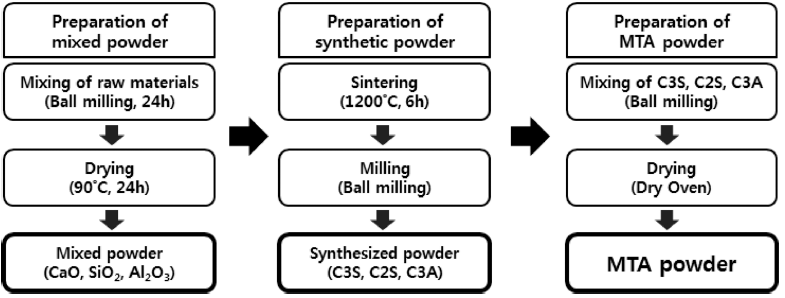

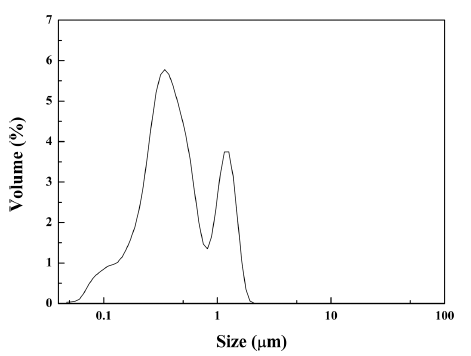
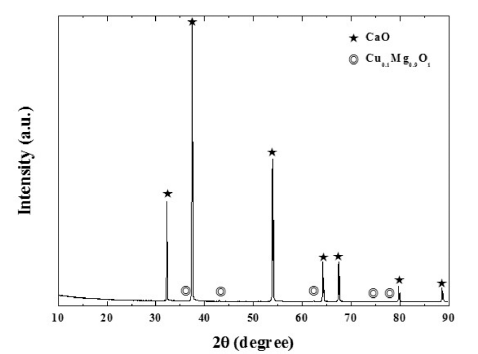
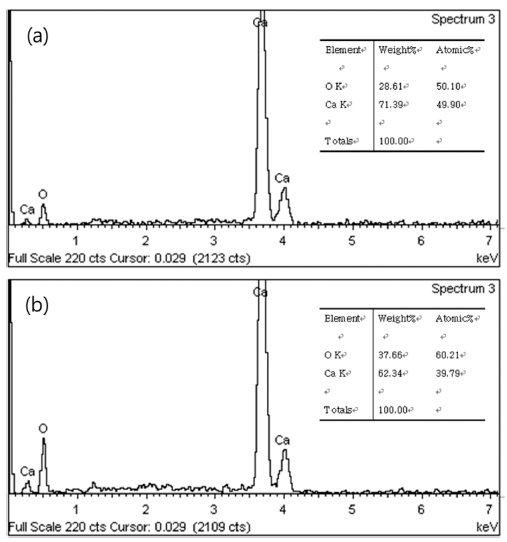
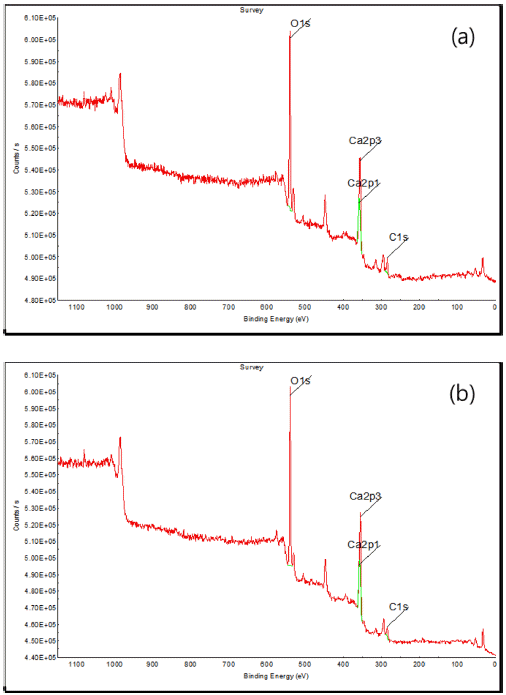
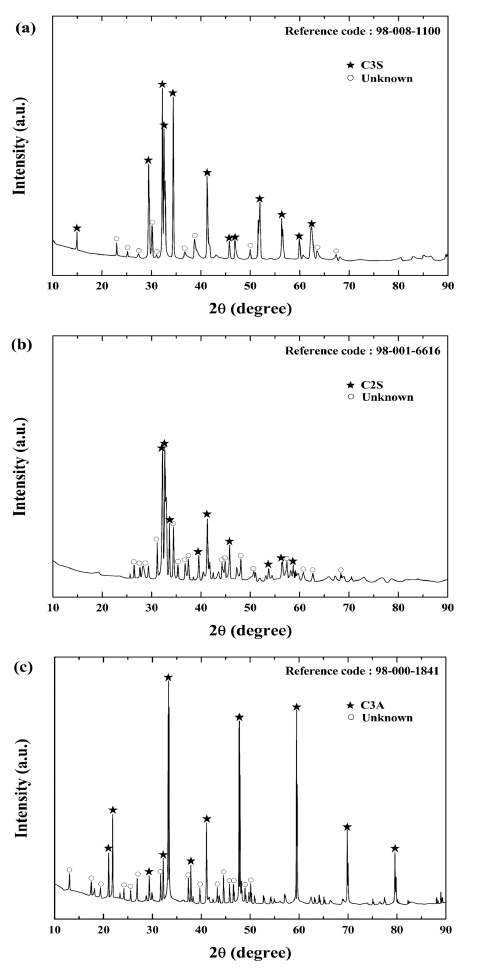
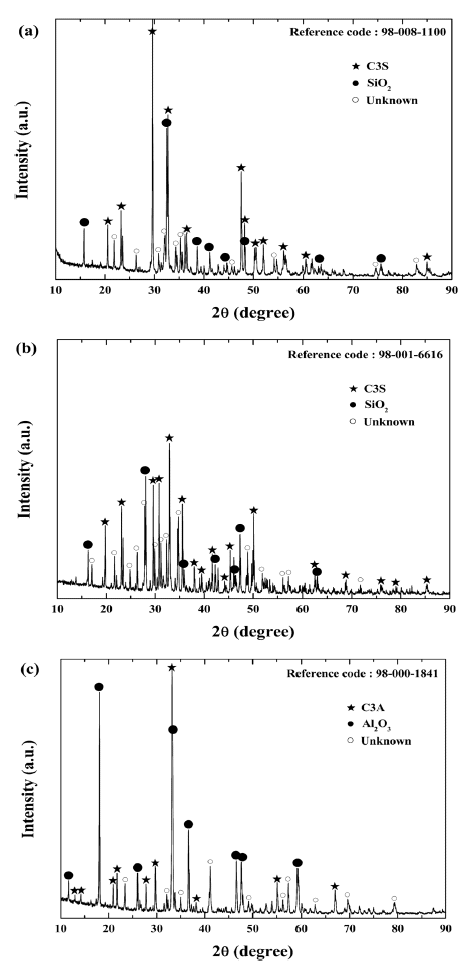

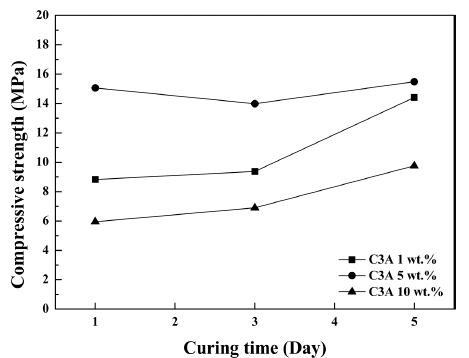
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Fig. 7
Fig. 8
Fig. 9
Fig. 10
Fig. 11
Table 1
Table 2
TOP
 KPMI
KPMI



 Cite this Article
Cite this Article