Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 28(1); 2021 > Article
-
Article
글루타티온이 캡핑된 ZnSe 나노 입자 발광 특성에 미치는 합성 조건의 영향 - 백금지, 송하연, 이민서, 홍현선*
- Effects of Synthesis Conditions on Luminescence Characteristics of Glutathione Capped ZnSe Nano particles
- Geum Ji Back, Ha Yeon Song, Min Seo Lee, Hyun Seon Hong*
-
Journal of Korean Powder Metallurgy Institute 2021;28(1):44-50.
DOI: https://doi.org/10.4150/KPMI.2021.28.1.44
Published online: January 31, 2021
성신여자대학교, 청정융합에너지공학과
Department of Environment & Energy Engineering, Sungshin Women’s University, Seoul 01133, Republic of Korea
- *Corresponding Author: Hyun Seon Hong, TEL: +82-2-920-2753, FAX: +82-2-920-2786, E-mail: hshong@sungshin.ac.kr
- - 백금지· 송하연·이민서: 학생, 홍현선: 교수
• Received: February 12, 2021 • Revised: February 24, 2021 • Accepted: February 25, 2021
© The Korean Powder Metallurgy Institute. All rights reserved.
- 1,426 Views
- 10 Download
- 2 Crossref
Abstract
- Zinc selenide (ZnSe) nanoparticles were synthesized in aqueous solution using glutathione (GSH) as a ligand. The influence of the ligand content, reaction temperature, and hydroxyl ion concentration (pH) on the fabrication of the ZnSe particles was investigated. The optical properties of the synthesized ZnSe particles were characterized using various analytical techniques. The nanoparticles absorbed UV-vis light in the range of 350-400 nm, which is shorter than the absorption wavelength of bulk ZnSe particles (460 nm). The lowest ligand concentration for achieving good light absorption and emission properties was 0.6 mmol. The reaction temperature had an impact on the emission properties; photoluminescence spectroscopic analysis showed that the photo-discharge characteristics were greatly enhanced at high temperatures. These discharge characteristics were also affected by the hydroxyl ion concentration in solution; at pH 13, sound emission characteristics were observed, even at a low temperature of 25°C. The manufactured nanoparticles showed excellent light absorption and emission properties, suggesting the possibility of fabricating ZnSe QDs in aqueous solutions at low temperatures.
- 양자점(quantum dot)은 입자 직경이 10 nm 이하인 나노 반도체 입자이고, 통상적으로 1~4 eV 내외의 에너지 밴드 갭을 가지고 있다. 양자점은 외부에서 에너지를 흡수하게 되면 입자크기에 따라 파장 크기가 다른 빛을 방출할 수 있다. 발광되는 빛은 색 순도와 효율성 면에서 우수하여 차세대 광학소재로 관심을 받고 있다[1-3]. 초창기에 개발 된 카드뮴 계 양자점은 합성이 쉽고 가시광선 모든 영역 에서 발광할 수 있어 많은 연구가 진행되었다[4-7]. 카드 뮴 양자점은 디스플레이 등 여러 산업분야에 적용이 가능 하지만, 환경과 인체에 해롭다는 단점이 있어 광범위한 사 용에 제한이 있다.
- 현재 카드뮴 계 양자점 이외에, III-V 족 반도체 양자점 또는 II-VI 족 반도체 양자점이 연구되고 있는데, 인화 인 듐(InP)과 셀렌화 아연(ZnSe)이 대표적인 예이다. III-V족 반도체인 InP 양자점은 공유결합이 강한 편이어서 합성과 표면제어가 쉽지 않으나 코어/쉘 구조를 통해 효율이 향상 되는 것으로 보고되고 있다[8-10]. 또한 InP는 에너지 밴 드 갭이 상온에서 1.35eV 이기 때문에 청색 발광의 양자 점을 합성하기가 어려운 특성이 있다. 반면에, II-VI족 반 도체인 ZnSe는 에너지 밴드 갭이 2.7 eV(460 nm)로 청색 발광이 가능한 특징이 있는데, 다양한 색의 발광을 위해 전이 금속을 도핑하여 발광되는 빛의 파장을 조절하는 연 구도 진행되고 있다[11-16].
- 초창기에 ZnSe 합성은 기존 카드뮴 계 양자점 합성 방 법과 유사하게 유기용매를 이용하여 콜로이드를 합성하였 다. 이후 ZnSe 양자점은 수계 용매에서도 제조가 가능함 이 보고되었다. 현재 수계 합성은 공정 최적화를 위해 환 원제와 캡핑제(capping agent)의 역할에 대한 연구가 진행 되고 있다. 저자들은 이전 연구에서 ZnSe 양자점 합성에 미치는 환원제의 영향을 조사하였는데, 하이드라진(N2H4) 보다 수소화 붕소 나트륨(NaBH4)이 환원제로 첨가된 수 용액에서 Se이 빠르게 용해되어 Se 전구체가 용이하게 생 성되는 것을 보고하였다. 따라서 환원 시약으로 NaBH4를 사용하면 상온에서도 ZnSe가 성공적으로 합성되는 것을 밝힌 바 있다[17, 18].
- 한편 양자점 합성 시 캡핑제를 첨가하여 나노 입자의 표 면을 개질하려는 연구가 진행되고 있다. 표면 개질은 나노 입자의 응집을 막기 위해 리간드(ligand)를 나노 입자 표 면에 결합시켜 입자 표면의 전하상태를 안정시키기 위함 이다. 최근 리간드를 사용하여 양자점의 전기적, 광학적 성질을 제어하는 연구도 활발히 진행되고 있다[19]. 또한 수성 양자점 합성의 경우 구조적 및 광학적 특성에 대한 일부 유형의 표면 리간드의 영향이 연구되었으며 가장 대 표적으로 사용된 표면 리간드는 thioglycolic acid(TGA), 3-mercaptopropionic acid(MPA), glutathione(GSH)이다[20]. 이들은 티올기를 포함한 리간드로 양자점에 수용성을 부 여하여 특정 용매에 부유시키고 표면을 화학적으로 부동 태화하여 전기적 및 광학적 특성을 변경한다[21]. 이처럼 리간드는 양자점 제조 시 나노 물질 분산과 광학물성에 중요한 역할을 함에도 불구하고 아직까지 다양한 리간드 에 대한 체계적인 연구가 이루어지지 못하고 있다.
- 따라서 본 연구에서는 수계 합성 공정을 위해 deionized water(DIW)를 용매로 사용하였고, 환원제로서 NaBH4를 사용하여 나노 입자를 제조하였다. 또한 리간드가 ZnSe 수계 합성에 미치는 영향을 확인하기 위해 GSH 등 여러 리간드의 성능을 비교하였고, 그 중 효율이 가장 좋은 리 간드를 선정하였다. 선정된 리간드의 함량, 합성 온도, pH 를 변화시켜 ZnSe 나노 입자를 합성하였고 제조된 나노 입자의 흡수와 발광 특성에 미치는 영향을 조사하였다.
1. 서 론
- 2.1. 시료
- 본 연구에서 사용된 시료는 znic acetate(Zn(CH3COO)2, 99.99%), Se 분말(Se, 99.99%), sodium borohydride(NaBH4, 99.99%), sodium hydroxide(NaOH, 97%), glutathione (C10H17N3O6S, 98%), thioglycolic acid(C2H4O2S, 99%), 3- mercaptopropionic acid(C3H6O2S, 99%) 이다. 모든 시약은 Sigma-Aldrich에서 구매했다. 모든 화학물질은 분석시약 등급이다.
- 2.2. ZnSe 나노 입자 합성
- ZnSe 나노 입자의 합성 과정은 Fig. 1에 제시하였다. 모 든 전구체는 DIW를 용매로 사용하였다. Zn 전구체 합성 은 DIW 5 0mL에 zinc acetate 0.5m mol을 완전히 녹인 뒤, GSH 0.6 mmol을 용해시켰다. 이후 5M NaOH를 주입해 pH 12로 조정했다. 캡핑제 종류의 영향 실험에서는 리간 드로 MPA, TGA, GSH를 사용하였고 모두 0.6 mmol을 첨 가하였다. 캡핑제 GSH의 함량 실험에서는 범위를 0.2, 0.4, 0.6, 0.8, 1 mmol로 조정하였다. 또한 pH 농도 실험에 서는 범위를 pH 9, 10, 11, 12, 13, 14로 조정하였다. Se 전구체 합성을 위해 먼저 pH 12인 DIW 10mL를 제조했 다. 다음으로 1mL를 바이알에 옮겨 NaBH4 0.835m mol 을 용해시켰다. NaBH4가 녹은 후 Se분말 0.2 mmol을 첨 가한다. Se 분말은은 초음파 세척기를 통해 분산시켰다. 이때, 바이알의 입구를 파라필름으로 막고 기체 순환을 위 해 구멍을 뚫어준다. 마지막으로 Se 분말이 용해되어 투 명해진 1mL의 용액을 남은 9mL의 용액에 혼합했다.
- ZnSe 코어 합성은 각각의 전구체를 N2 분위기 하에 합 성한다. 빠르게 교반하고 있는 Zn 전구체에 Se 전구체를 천천히 부었다. 이렇게 합성된 ZnSe는 90°C에서 1시간 동 안 교반하며 가열시켰다. 가열 후, 글러브 박스에서 천천 히 냉각시켰다. 전구체 가열 온도 영향 실험에서는 25, 50, 60, 70, 80, 90, 100°C로 범위를 조정하였다.
- 2.3. 특성 분석
- ZnSe 나노 입자의 광흡수 특성은 자외선-가시 광선 분 광기인 UV-vis spectroscope(SPECORD PLUS, Analytikjenatk 사, 독일)를 통해 분석하였고 발광 특성은 Photoluminescence( PL) spectroscope(FP-8500, Jasco사, 일본)을 이용하 여 분석하였다. 또한 입도 분석은 Particle size analyzer (PSA, Nano Plus HD, Micromeritics사, 미국)를 사용하여 측정하였다.
2. 실험방법
- 3.1. 캡핑제 종류의 영향
- 본 연구에서는 캡핑제 역할을 하는 리간드로 TGA, MPA, GSH를 사용하여 ZnSe 합성에 미치는 영향을 조사 하였다. 따라서 Zn 전구체에 각각의 리간드를 첨가하고 Se 전구체와 동일하게 pH 12로 조정하여 실험하였다. Fig. 2-(a)는 캡핑제 종류에 따른 ZnSe 나노 입자의 광 흡수 특 성을 UV-vis 분광기로 관찰한 결과이다. 리간드를 주입하 지 않고 합성한 경우 흡수단(absorption edge)이 명확하지 않은 형태의 그래프가 관찰되었다. 이는 흡수가 전 파장대 에서 제대로 이뤄지지 않았음을 보여준다. 리간드가 첨가 된 경우, 흡수 파장이 짧은 쪽으로 이동하여 blue-shift가 일어났고, 다른 리간드 보다 GSH를 사용했을 때 가장 짧 은 파장에서 흡수가 일어났다. Fig. 2-(b)는 리간드 종류에 따른 광 발광 특성 결과이다. GSH를 첨가한 경우 다른 리 간드를 첨가했을 때 보다 월등히 높은 강도를 보였고, 가 장 짧은 파장인 375 nm에서 발광 피크(emission peak)가 발생함을 알 수 있었다. MPA와 TGA를 사용한 경우 400~410 nm에서 발광 피크가 발생하였으나 GSH에 비해 매우 낮은 발광 강도를 나타냈다. 안정화제를 안 넣은 경 우 460 nm 파장에서 매우 약한 발광이 broad하게 나타났 는데, 이 파장대는 벌크 ZnSe가 가지고 있는 밴드 갭 에 너지에 해당하기 때문에 나노 크기의 입자가 형성되지 않 은 것으로 보인다. 전반적인 발광 피크를 분석했을 때 리 간드를 사용하면 blue-shift가 일어났고, GSH의 효과가 가 장 컸다. Fig. 2-(c)는 UV light를 조사하였을 때, 각 샘플 의 발광 사진이다. 리간드를 사용하지 않았을 경우 DIW 와 마찬가지로 발광이 되지 않음을 확인할 수 있다. 또한, GSH를 사용한 ZnSe의 발광이 가장 우수하였다.
- Fig. 3은 리간드 종류에 따른 ZnSe 입자크기를 분석한 결과이다. GSH를 사용하여 합성된 ZnSe 코어는 평균 입 자크기가 3.6 nm로 나노 입자가 양호하게 만들어졌다. TGA와 MPA를 사용하여 제조한 경우 평균 입자크기가 각 각 26.4 nm, 183.0 nm으로 10 nm 이상의 입자 직경을 가 져 나노 입자 사이에서 aggregation 현상이 발생한 것으로 판단된다. 특히, 리간드를 첨가하지 않은 ZnSe 입자의 경 우 평균 입자크기가 약 1991 nm인 벌크 형태에 해당하는 크기로 존재하였다. 이때 발광 피크 파장은 460 nm이었으 며, 이는 벌크 ZnSe 의 밴드 갭 에너지에 해당한다. GSH 는 이외의 리간드 보다 DIW 내에서 나노 입자의 분산성 이 뛰어나고 aggregation을 효과적으로 막아 광학 특성이 우수한 것으로 판단된다. 결과적으로 GSH가 캡핑된 ZnSe 는 10 nm 이하로 가장 작은 입자 크기가 측정되었다.ZnSe 양자점의 경우 엑시톤 보어 반경이 4.5nm이다[22]. 평균 입자 크기가 3.6 nm로 제조된 ZnSe-GSH는 엑시톤 보어 반지름 이하의 나노 입자들로, 양자 구속 효과를 가 지는 양자점이 합성되었음을 알 수 있다.
- 3.2. GSH 몰 수의 영향
- 캡핑제로 GSH를 사용하였을 때, ZnSe 나노 입자의 광 흡수/발광 특성이 우수한 것으로 나타났다. GSH 농도의 영향을 알아보기 위해 ZnSe합성 과정에서 Zn과 Se 전구 체의 pH를 12로 고정하고 GSH를 0.2 mmol부터 1 mmol 까지 변화시키며 흡수/발광 특성을 관찰하였다. Fig. 4-(a) 는 GSH의 몰 수에 따른 UV-vis 특성을 관찰한 결과이다. GSH의 함량이 0.2 mmol, 0.4 mmol로 적은 경우, 그래프가 불안정한 양상을 보이며 흡수단의 급격한 red-shift가 일어 났다. 반면에 GSH가 0.6 mmol 이상 첨가된 경우 UV-vis 그래프에서 보듯이 380 nm에서 흡수단이 안정하게 나타 났으며 함량 별로 유사한 그래프 형태를 보였다. Fig. 4- (b)는 GSH의 함량에 따른 ZnSe PL 특성을 관찰한 결과이 다. GSH 몰 수가 0.4 mmol 이하인 경우 intensity가 매우 낮고, 특히 0.2 mmol인 경우 발광 피크가 명확히 나타나 지 않았다. Fig. 4-(b)의 발광 사진을 보면 0.4 mmol 이하 인 경우, DIW와 유사하며 발광이 관찰되지 않았다. 함량 이 0.4 mmol 보다 적은 경우 충분한 양의 리간드가 존재 하지 못해 효과적인 리간드 캡핑 층을 형성할 수 없었던 것으로 보인다[23]. GSH 몰 수가 0.6~1 mmol인 경우 370~380 nm에서 mono-dispersive한 특성을 갖는 발광 곡 선을 보이며 특히 0.6 mmol일 때 가장 높은 intensity가 관 찰되었다. 하지만 0.6 mmol 이상인 경우 intensity가 급격 히 감소한다. 리간드가 과도하게 초과되면 Zn(GSH)2+ 복 합체의 농도가 상대적으로 감소하고 Zn(GSH)2 농도가 증 가한다. 이는 안정된 ZnSe 코어 합성을 방해한다[23]. 결 론적으로 GSH를 0.6 mmol 내외로 첨가할 경우, UV-vis 흡수 특성과 PL 발광 특성이 안정적이고 높은 발광 세기 를 나타내는 것으로 판단된다.
- 3.3. 전구체 가열 온도의 영향
- ZnSe 나노 입자를 합성하는 과정 중 가열 온도가 광 흡 수 및 발광 특성에 미치는 영향을 알아보기 위해 Zn과 Se 전구체의 pH를 12로 고정하고 실험을 진행하였다. Fig. 5- (a)는 온도에 따른 ZnSe 입자의 UV-vis 특성 변화를 보여 주고 있다. 그래프에 따르면 온도가 증가할수록 UV-vis 흡 수단이 짧은 파장대에서 긴 파장대로 이동하여 red-shift가 일어났다. Fig. 5-(b)는 온도에 따른 PL 특성에 대해 관찰 한 결과이다. 25, 50°C 저온의 경우 매우 낮은 intensity를 나타냈다. 이는 낮은 온도에서는 나노 입자 합성이 원활하 게 이뤄지지 않음을 보여준다. 반면에, 70~100°C에서 가 열할 경우 저온에 비해 높은 intensity를 보이는 데 특히 90°C와 100°C에서 현저히 높은 intensity를 관찰할 수 있 었다. 90°C에서 합성할 경우 100°C보다 짧은 파장에서 발 광 피크가 발생하며 가장 높은 intensity를 보였다. 온도가 높을수록 Zn이 용매에 용해될 수 있는 임계 크기와 임계 값이 증가하여 입자가 용해되는 원동력이 증가했기 때문인 것으로 보인다[24]. UV-vis 특성과 PL 특성을 종합하여 분 석한 결과, GSH 리간드와 pH 12 조건에서 전구체 합성을 위한 최적의 온도 조건은 90°C 내외인 것으로 판단된다.
- 3.4. pH의 영향
- 일반적으로 OH-는 Zn2+와 HSe-의 반응에 의한 ZnSe 핵 생성을 유리하게 하기 때문에 pH 값에 따라 적절한 입자 크기로 ZnSe 나노 입자를 합성할 수 있다[25]. 따라서 pH 가 ZnSe 나노 입자에 미치는 영향을 알아보고자 온도 별 로 pH 범위를 설정하여 실험을 진행하였다. Fig. 6-(a)는 각 온도에서 pH에 따른 ZnSe의 UV-vis 흡수단을 분석한 결과로, 그래프에 따르면 모든 온도 조건에서 pH 값이 증 가함에 따라 흡수단이 장파장으로 이동하였다. Fig. 6-(b) 는 온도 별 pH에 따른 ZnSe 발광 피크의 파장을 분석한 결과이다. 동일한 온도에서 pH가 증가할수록 단파장에서 장파장으로 이동하여 red-shift되고 동일한 pH 값일 때 온 도가 높을수록 파장이 길어져 red-shift가 일어난다. Fig. 6-(b) 내부에 삽입된 발광 사진은 각 온도마다 가장 높은 intensity를 보이는 조건에 UV-light를 조사한 것이다. Fig. 6-(c)는 ZnSe의 PL intensity를 분석한 결과이다. 상대적으 로 저온인 5 0°C 이하의 pH 9~12 사이에서는 거의 발광하 지 않았으나, pH 13에서는 발광이 나타났다. 반면에 90°C 에서는 pH 10~12 사이에서 발광하였으나 pH 13에서는 발광이 나타나지 않았다. Fig. 6-(d)는 Fig. 6-(c)에서 pH 10인 90°C, pH 13인 25°C와 5 0°C의 PL 발광 특성을 나타 낸 그래프이다. 저온인 25°C와 5 0°C에 해당하는 발광 피 크의 파장과 강도가 고온인 90°C의 결과와 유사함을 확인 할 수 있다. OH-가 증가할 경우, Se2-와 Zn(GSH)2+ 복합 체의 결합이 에너지 측면에서 안정적이게 되어 저온에서 도 발광이 가능했던 것으로 판단된다[25]. 일반적으로 ZnSe 나노 입자는 70°C 이상의 고온에서 합성될 경우 발 광 특성이 우수하나, pH 값에 따라 저온에서 발광이 가능 하다는 것을 확인하였다.
3. 실험결과 및 고찰
Fig. 2

(a) UV-vis absorption spectra, (b) PL emission spectra of ZnSe with varying ligands, and (c) ZnSe QDs under UV light according to ligands.

Fig. 3

Particle size distribution of ZnSe with varying ligands; (a) GSH, (b) TGA, (c) MPA and (d) no ligand.

Fig. 4

(a) UV-vis absorption spectra and (b) PL emission spectra of ZnSe with varying GSH contents. The inset in (b) shows ZnSe QDs in UV light with varying GSH contents.

Fig. 5

(a) UV-vis absorption spectra and (b) PL emission spectra of ZnSe with varying synthesis temperatures.

- 본 연구는 비카드뮴계 ZnSe 나노 입자에 GSH로 캡핑을 하여 수계 분위기에서 고 발광특성을 나타내는 친환경 ZnSe 나노입자를 합성하였다. 합성된 ZnSe는 흡수, 발광 스펙트럼 및 미세 입도 분석을 통해 특성평가 되어 다음 과 같은 결론이 도출되었다. GSH를 캡핑한 ZnSe는 강한 PL 강도와 400 nm 이하에서 발광 피크를 나타내며, 10 nm 이하 수준의 나노 입자가 합성된다. GSH 함량이 증가할 수록 intensity가 높아지나, 리간드 함량의 한계가 초과되 면 안정적인 화학 구조의 ZnSe 합성이 어려워진다. 따라 서 최적의 GSH 몰 수는 0.6 mmol 내외인 것으로 보인다. 합성 온도가 70°C 이상일 경우 Zn 이온의 용해가 활성화 되어 발광 특성이 향상된다. 한편, 저온의 경우에도 pH 값 을 증가시키면 높은 발광 특성을 나타낼 수 있는 ZnSe의 합성 공정이 가능함을 확인하였다. 이를 통해 OH-가 ZnSe의 화학 결합 메커니즘에 영향을 미치는 주요 요인으 로 작용하고 있음을 확인하였다. 무독성의 ZnSe 코어는 저온에서도 우수한 청색 발광으로 양자점 합성 공정의 기 반이 되어, 이후 코어/쉘 구조 양자점 개발에 기여할 것으 로 예상된다.
4. 결 론
-
Acknowledgements
- 이 논문은 2019년도 성신여자대학교 학술연구조성비 지 원에 의하여 연구되었으며, 이에 감사드립니다.
감사의 글
- 1. A. P. Alivisatos : Science, 271 (1996) 933. .Article
- 2. D. J. Norris, A. L. Efros and S. C. Erwin: Science, 319 (2008) 1776. .ArticlePubMed
- 3. A. Valizadeh, H. Mikaeili, M. Samiei, S. M. Farkhani, N. Zarghami, M. Kouhi, A. Akbarzadeh and S. Davaran: Nanoscale Res. Lett., 7 (2012) 480. .ArticlePubMedPMC
- 4. C. J. Barrelet, Y. Wu, D. C. Bell and C. M. Lieber: J. Am. Chem. Soc., 125 (2003) 11498. .ArticlePubMed
- 5. K. S. Leschkies, R. Divakar, J. Basu, E. Enache-Pommer, J. E. Boercher, C. B. Carter, U. R. Korshagen, D. J. Norris and E. S. Aydil: Nano Letters, 7 (2007) 1793. .ArticlePubMed
- 6. D. J. Norris and M. G. Bawendi: Phys. Rev. B, 53 (1996) 16338. .ArticlePubMed
- 7. L. W. Wang and A. Zunger: Phys. Rev. B, 53 (1996) 9579. .ArticlePubMed
- 8. C. Wang, Q. Wang, Z. Zhou, W. Wu, Z. Chai, Y. Gao and D. Kong: J. Lumin., 225 (2020) 117354. .Article
- 9. L. Langof, L. Fradkin, E. Ehrenfreund, E. Lifshitz, O. I. Micic and A. J. Nozik: Chem. Phys., 297 (2004) 93. .Article
- 10. F. Ángel-Huerta, M. P. González-Araoz, J. F. Sánchez- Ramírez, J. Díaz-Reyes, J. L. Herrera-Pérez, J. S. Arias- Cerón and J. G. Mendoza-Álvarez: J. Lumin., 197 (2018) 277. .Article
- 11. P. Reiss: New J. Chem., 31 (2007) 1843. .Article
- 12. K. Saikia, P. Deba and E. Kalita: Curr. Appl. Phys., 13 (2013) 925. .Article
- 13. G. Y. Lan, Y. W. Lin, Y. F. Huang and H. T. Chang: J. Mater. Chem., 17 (2007) 2661. .Article
- 14. Z. Deng, F. L. Lie, S. Shen, I. Ghosh M. Mansuripur and A. J. Muscat: Langmuir, 25 (2009) 434. .ArticlePubMed
- 15. A. Shavel, N. Gaponik and A. Eychmülle: J. Phys. Chem. B, 108 (2004) 5905. .Article
- 16. L. C. He, Y. A. Zhang, S. L. Zhang, X. T. Zhou, Z. Lin and T. L. Guo: Mater. Technol., 33 (2017) 205. .Article
- 17. H. Hong and M. Kim: Korean J. Mater. Res., 27 (2017) 459. .Article
- 18. H. Hong, M. Kim, E. Byun and Y. Lee: J. Crystal Growth., 535 (2020) 125523. .Article
- 19. C. Lee, U. Lee and H. Che: Vac. Magazine, 6 (2017) 29. .
- 20. F. O. Silva, M. S. Carvalho, R. Mendonça, W. A. Macedo, K. Balzuweit, P. Reiss and M. A. Schiavon: Nanoscale Res. Lett., 7 (2012) 1. .ArticlePubMedPMC
- 21. F. Jiang and A. J. Muscat: Langmuir, 28 (2012) 12931. .ArticlePubMed
- 22. S. Ramanathan, S. Patibandla, S. Bandyopadhyay, J. Anderson and J. D. Edwards: Nanotechnology, 19 (2008) 195601. .ArticlePubMed
- 23. P. Wu, Zh. Fang, X. Zhong and Y. J. Yang: Colloids and Surfaces A: Physicochem. Eng. Aspects, 375 (2011) 109. .Article
- 24. F. Jiang and A. J. Muscat: Langmuir, 28 (2012) 12931. .ArticlePubMed
- 25. L. Sun, F. Gong, Ch. Zhou, H. Wang, and Sh. Yao: Mater. Express, 5 (2015) 219. .Article
Figure & Data
References
Citations
Citations to this article as recorded by 

- Green synthesis and luminescence characteristics of ZnSe-ZnS core-shell quantum dots
Geum Ji Back, Ha Yeon Song, Min Seo Lee, Jaesik Yoon, Hyun Seon Hong
Journal of Crystal Growth.2024; 626: 127475. CrossRef - Effect of UV Irradiation on Optical Properties of Water-Based Synthetic Zinc Selenide Quantum Dots
Geum Ji Back, Yu Jin Kang, I Ju Kang, Jeong Hyeon Lim, Hyun Seon Hong
Korean Journal of Metals and Materials.2022; 60(2): 160. CrossRef
Effects of Synthesis Conditions on Luminescence Characteristics of Glutathione Capped ZnSe Nano particles
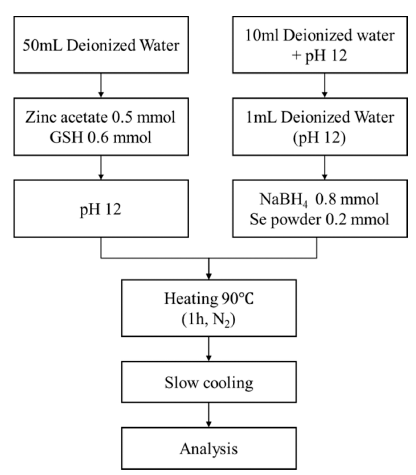
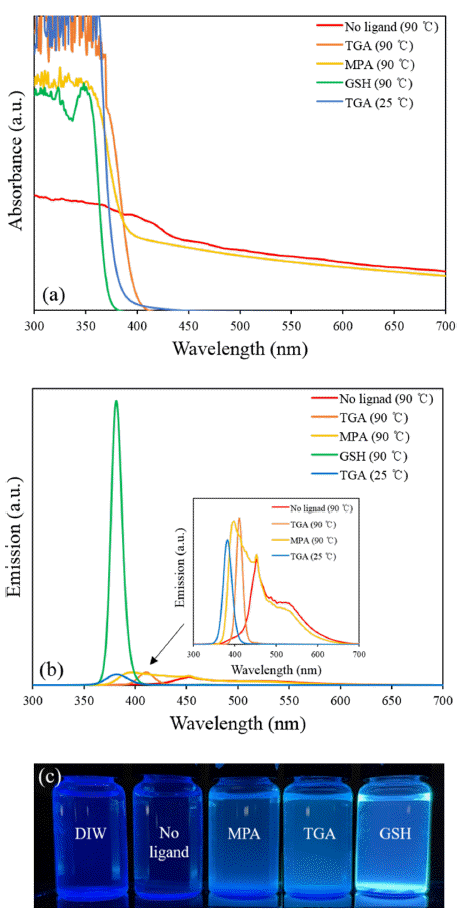

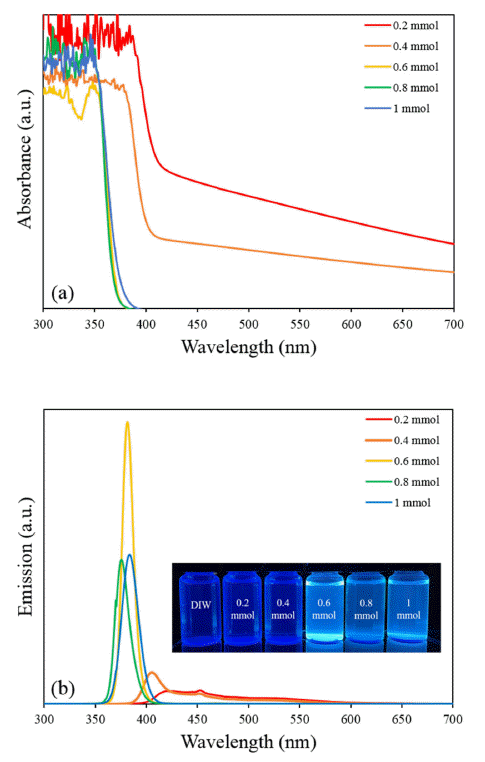

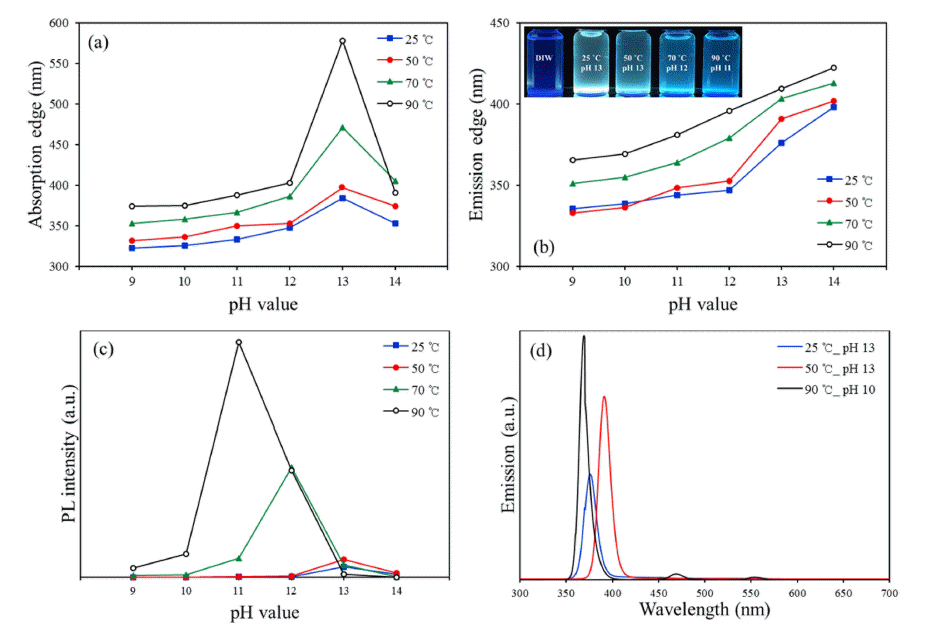
Fig. 1
Experimental flow chart for ZnSe synthesis.
Fig. 2
(a) UV-vis absorption spectra, (b) PL emission spectra of ZnSe with varying ligands, and (c) ZnSe QDs under UV light according to ligands.
Fig. 3
Particle size distribution of ZnSe with varying ligands; (a) GSH, (b) TGA, (c) MPA and (d) no ligand.
Fig. 4
(a) UV-vis absorption spectra and (b) PL emission spectra of ZnSe with varying GSH contents. The inset in (b) shows ZnSe QDs in UV light with varying GSH contents.
Fig. 5
(a) UV-vis absorption spectra and (b) PL emission spectra of ZnSe with varying synthesis temperatures.
Fig. 6
(a) Absorption edge (b) Emission edge, inset in (b) shows ZnSe QDs in UV light (c) Highest PL intensity with varying pH value and (d) PL emission spectra of 25°C (pH 13), 50°C (pH 13) and 90°C (pH 10), inset in (d) shows ZnSe QDs in UV light.
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Effects of Synthesis Conditions on Luminescence Characteristics of Glutathione Capped ZnSe Nano particles
TOP
 KPMI
KPMI



 ePub Link
ePub Link Cite this Article
Cite this Article