Articles
- Page Path
- HOME > J Powder Mater > Volume 30(5); 2023 > Article
-
Article
Sol-Gel법에 의한 Li1.5Al0.5Ti1.5(PO4)3 고체전해질 제조 및 chelating agent의 영향 - 류성준†, 최슬기†, 원종호*, 양민호*
- Effect of Chelating Agent on Li1.5Al0.5Ti1.5(PO4)3 Particles by Sol-gel Method and Densification
- SungJoon Ryu†, Seul Ki Choi†, Jong Ho Won*, MinHo Yang*
-
Journal of Korean Powder Metallurgy Institute 2023;30(5):394-401.
DOI: https://doi.org/10.4150/KPMI.2023.30.5.394
Published online: September 30, 2023
단국대학교 에너지공학과
Department of Energy Engineering, Dankook University, Cheonan 31116, Republic of Korea
-
* Corresponding Author: Jong Ho Won, TEL: +82-41-550-3687, FAX: +82-41-550-3687, E-mail: jhwon23@dankook.ac.kr
MinHo Yang, TEL: +82-41-550-3685, FAX: +82-41-559-7914, E-mail: mhyang@dankook.ac.kr -
- 류성준·최슬기: 학생, 원종호·양민호: 교수
†These authors contributed equally to this work.
• Received: August 21, 2023 • Revised: October 6, 2023 • Accepted: October 8, 2023
© The Korean Powder Metallurgy Institute. All rights reserved.
- 2,133 Views
- 55 Download
- 1 Crossref
Abstract
- Li1.5Al0.5Ti1.5(PO4)3 (LATP) is considered to be one of the promising solid-state electrolytes owing to its excellent chemical and thermal stability, wide potential range (~5.0 V), and high ionic conductivity (~10-4 S/cm). LATP powders are typically prepared via the sol-gel method by adding and mixing nitrate or alkoxide precursors with chelating agents. Here, the thermal properties, crystallinity, density, particle size, and distribution of LATP powders based on chelating agents (citric acid, acetylacetone, EDTA) are compared to find the optimal conditions for densely sintered LATP with high purity. In addition, the three types of LATP powders are utilized to prepare sintered solid electrolytes and observe the microstructure changes during the sintering process. The pyrolysis onset temperature and crystallization temperature of the powder samples are in the order AC-LATP > CA-LATP > ED-LATP, and the LATP powder utilizing citric acid exhibits the highest purity, as no secondary phase other than LiTi2PO4 phase is observed. LATP with citric acid and acetylacetone has a value close to the theoretical density (2.8 g/cm3) after sintering. In comparison, LATP with EDTA has a low sintered density (2.2 g/cm3) because of the generation of many pores after sintering.
- 최근 전세계적인 친환경정책에 따라 전기자동차 시장이 급격히 성장하고 있다. 리튬 이온전지는 전기자동차의 주 동력공급장치로 사용되며, 1회 충전 시 500 km 주행이 가 능한 고에너지 밀도 특성이 요구된다[1-3]. 리튬 이온전지 는 양극, 음극, 전해액으로 구성되어 있고 분리막을 통해 양∙음극간 직접적인 접촉을 막아 단락을 방지한다. 전해액 은 lithium hexafluorophosphate (LiPF6), lithium perchlorate (LiClO4), lithium bis(trifluoromethanesulfonyl) imide(LiTFSI) 와 같은 리튬염을 유기 용매에 녹여 사용하기 때문에 상 온 이온전도도가 10-2 S/cm 수준으로 높은 반면, 유기 용 매의 가연성으로 인한 화재와 폭발의 위험성이 있다[4-6]. 따라서 액체 전해액의 고온 안정성 문제를 해결할 수 있 는 불연성 고체 전해질의 개발이 요구되고 있다.
- 고체전해질은 크게 고분자, 황화물계, 산화물계 고체전 해질로 구분할 수 있다. 고분자 고체전해질은 제조비용과 공정 측면에서 우수하지만 큰 계면저항으로 인해 리튬 이 온전도도(~10-7 S/cm@25ºC)가 낮으며 65~80ºC의 높은 온 도 범위에서만 구동이 가능하다는 단점이 있다[7]. 황화물 계 고체전해질은 황의 낮은 전기음성도로 인해 황과 리튬 사이의 결합 강도가 상대적으로 낮아 리튬이온 이동이 원 활하여 높은 리튬 이온전도도(~10-3 S/cm@25ºC)를 갖는 장점이 있다[8]. 하지만 대기 중에서 수분과 반응하여 유 독성이 강한 H2S 가스를 방출하기 때문에 취급에 제약이 따른다[8, 9]. 산화물계 고체전해질은 공기 중에서 안정하 며, 5 V 이상의 넓은 전위창을 가져 고전압을 갖는 새로운 양극 소재를 적용할 수 있고 상온에서 10-4 S/cm 수준의 준수한 리튬 이온전도도를 나타내기 때문에 IoT 및 소형 전자기기 등의 전력원으로 이용되고 있다[10, 11].
- 대표적인 산화물계 고체전해질로는 lithium lanthanum titanate(LLTO), lithium lanthanum zirconium oxide(LLZO), lithium aluminum titanium phosphate(LATP), lithium aluminum germanium phosphate(LAGP) 등이 있고, 특히, LATP 는 우수한 화학적∙열적 안정성을 갖고 있어 유망한 고체전 해질 중 하나로 여겨진다[12, 13]. LATP는 용융-담금질법 (melt-quenching), 졸-겔법(sol-gel method), 공침법(co-precipitation) 등을 통해 합성이 가능하다[13]. 이 중 졸-겔법 은 균일하고 순도 높은 고밀도의 분말을 얻을 수 있고 비 교적 낮은 온도에서 합성이 가능하며 입자 크기와 구조를 제어하기에 용이한 장점을 가지고 있어 LATP 합성을 위 해 폭넓게 사용되고 있다[14, 15, 17]. 졸-겔법을 통해 합성 된 LATP의 이온전도도는 전구체의 화학양론비, chelating agent의 화학적 구조, 후속 열처리 조건 등의 인자에 영향 을 받는다. 그동안 전구체의 화학양론비, 열처리 온도 및 시간 등의 변화가 LATP의 전기적 특성에 미치는 영향에 관한 연구는 많이 이루어졌으나 chelating agent에 따른 LATP의 특성 변화에 대한 연구는 미비한 상황이다.
- Chelating agent는 금속 양이온과 배위 결합하여 다른 구 조와 낮은 반응성을 갖는 중간체를 형성하고 단일상 형성 을 가능하게 하며 졸-겔 합성에서 균일한 졸을 형성하는 데 중요한 역할을 한다[16]. LATP 합성 시 chelating agent 는 titanium 전구체의 산화를 방지해 부반응을 억제하고 이를 통해 titanium dioxide(TiO2), Aluminum phosphate (AlPO4) 등과 같은 이차상 생성을 억제하는데 큰 역할을 한다[13]. 졸-겔법에 사용되는 chelating agent는 citric acid, tartaric acid, acetylacetone, nitriloacetic acid, ethylenediaminetetraacetic acid(EDTA), glycolic acid 등이 있으며, chelating agent의 구조에 따라 전구체와의 결합 특성이 다르 기 때문에 chelating agent에 따른 LATP의 구조적, 열적, 전기적 특성 차이를 연구할 필요가 있다[18-20]. 본 연구 에서는 citric acid, acetylacetone, EDTA 세 종류의 chelating agent를 사용하여 LATP 분말을 합성하였고 각각 CALATP, AC-LATP, ED-LATP라고 명명하였다. 세 종류의 LATP 분말의 열적 특성, 결정화도, 입자 크기 및 분포도 에 chelating agent가 미치는 영향을 분석하였다. 또한, 소 결을 통해 소결체 형태의 LATP 고체전해질을 제조하고 chelating agent에 따른 고체전해질의 미세구조 및 결정성 의 차이를 관찰하였다.
1. Introduction
- 세 종류의 chelating agent를 사용하여 졸-겔법으로 LATP 분말을 합성하였다. 40ºC, 300 rpm 조건으로 교반 중인 탈이온수 350ml에 Titanium isopropoxide(Ti(OC3O7)4, 97%, S igma A ldrich) 56 g을 12 mL/min의 속도로 떨어뜨 려 백색의 침전물을 얻는다. 침전물을 여과하여 탈이온수 로 수차례 세척한 후 탈이온수 150 ml에 넣어 분산시킨다. 이 후, Nitric acid(HNO3, 70% Sigma Aldrich) 35 ml를 떨 어뜨린 후 용액이 투명해질 때까지 교반하고 chelating agent 로 citric acid(C6H8O7, 98%, Sigma Aldrich), acetylacetone (C5H8O2, 99%, DAEJUNG), EDTA(C10H16N2O8, 99.4 – 100.6% Sigma Aldrich)를 각각 0.45 mol씩 사용하여 세 가 지 Ti 전구체 용액을 제조한다. Lithium nitrate(LiNO3, 98%, DAEJUNG) 13.585 g, Aluminum nitrate(Al(NO3)3∙ 9H2O, 98%, Sigma Aldrich) 24.635 g를 Ti 전구체 용액에 넣고 용액에 완전히 용해될 때까지 교반한다. 마지막으로 Ammonium phosphate(NH4H2PO4, 98%, Sigma Aldrich) 45.33 g을 상기 용액에 넣어 sol 상태를 만든다. 수 초 혹 은 수 분 이내에 자발적으로 생성된 gel을 80ºC에서 24시 간 건조한 후 전기로에서 700ºC의 온도로 4시간 하소하여 유기물과 불순물을 제거한다. 하소 후 생성된 분말을 잘게 부순 후 LATP 분말을 공전/자전형 믹서를 사용해 지르코 니아 용기에 지르코니아 볼 : LATP : 에탄올 = 10 : 1 : 0.5 의 비율로 넣어 450 rpm의 속도로 15분 밀링, 15분 휴지 를 48회 반복한다. 밀링이 종료된 후 sieve를 이용해 지르 코니아 볼과 LATP 분말을 분리하고 분리한 분말 0.353 g 을 16 mm 성형 몰드에 넣어 2.5 ton/cm3의 압력으로 일축 가압성형하여 소결체를 만든다. 만들어진 소결체를 성형 체와 조성이 동일한 분말을 덮어주고 5ºC/min의 승온 속 도로 1000ºC까지 승온 후 10시간 동안 유지하여 LATP 고 체전해질을 제조한다.
- 각 chelating agent에 따른 LATP gel의 열적 특성을 확 인하기 위해 열중량 분석(Thermalgravimetric analyzer, TGA, TG_209_F1_Libra, NETZSCH)를 수행하였다. LATP 파우 더의 순도 및 결정성 확인을 위해 Cu-Kα 선을 사용하였 고, 40 kV, 15 mA와 2θ = 10° ~ 90°의 범위에서 5°/min의 스캔 속도로 X-선 회절 분석(X-ray diffraction; XRD, MiniFlex600, Rigaku)을 수행하였다. 하소 후 LATP 분말 입자 크기 및 분포도 확인을 위해 동적광산란 분석 (Dynamic Light Scattering; DLS, NanoPlus)을 수행하였다. 또한, LATP 분말 입자 크기 및 형태와 소결체의 미세구조 확인을 위해 전계 주사 현미경(Field Emission-Scanning Electron Microscopy; FE-SEM, S-4700, Hitachi)을 사용하 였다. 성형체의 bulk density는 저울(Satorius YDK03, Satorius) 을 사용하여 성형체의 무게와 부피를 측정하여 계산 하였고, 세 번 측정한 값의 평균을 기입하였다. 소결체의 apparent density는 Archimedes 밀도 측정법을 통해 측정 하였다.
2. Experimental
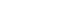
- Fig. 1은 chelating agent에 따른 LATP gel을 이용하여 N2 분위기 하에서 10ºC/min의 승온 속도로 30ºC에서 1000ºC 까지의 열중량 분석을 실시한 TGA 곡선을 나타낸 것이다. TGA 결과로부터 LATP gel의 열분해 거동은 chelating agent에 따라 다르게 나타나지만 크게 두 단계로 나누어져 일어나고 있음을 알 수 있다. 우선 I 단계는 중 량감소가 크게 일어나는 영역으로 용매로 사용한 수분 증 발과 질산의 열분해로 인한 중량 감소가 나타난다[21]. II 단계는 결정수 및 유기물 증발과 동시에 결합된 금속이온 과 chelating agent와의 분해반응으로 인한 중량 감소가 일 어난다[22, 23]. CA-LATP gel과 ED-LATP gel은 비슷한 형태의 TGA곡선을 보이며, I 단계에서 CA-LATP gel은 68.4%, ED-LATP gel은 53.5%의 중량 손실이 일어났다. AC-LATP gel은 두 시료와 달리 좁은 온도 영역에서의 급 격한 중량감소가 나타나지 않으며, I 단계에서 35.8%, II 단계에서 24.9%의 중량 감소를 보인다. 또한, 270ºC 이상 에서 중량 감소가 거의 나타나지 않는다. 이는 acetylacetone의 비점(AC 140ºC; CA 310ºC; ED 614ºC)이 상대적 으로 낮아 270ºC 부근에서 유기물들이 완전히 분해되고 금속산화물의 형태로 존재하는 것으로 판단할 수 있다. 하 지만, CA-LATP gel은 160ºC에서 700ºC까지의 영역인 II 단계에서 12.6%의 중량 감소를 보이며, ED-LATP gel은 125ºC에서 400ºC의 영역까지 20.2%, 400ºC 이상 영역에서 8%의 중량 감소를 나타낸다. 특히, II 단계 영역에서 일어나 는 결합된 금속이온과 chelating agent와의 열분해 시작 온도 는 AC-LATP > CA-LATP > ED-LATP 순으로 높게 나타났 다. 이는 chelating agent 내의 산소 원자와 금속이온과의 결 합 세기 차이에 의한 것으로 생각할 수 있다. 다시 말하면, EDTA가 금속 양이온과 결합 세기가 가장 약하여 상대적으 로 낮은 온도에서 금속이온으로부터 이탈되기 시작하여 낮 은 온도에서도 결정화가 진행될 수 있음을 의미한다[24].
- TGA curves of LATP gel synthesized by sol-gel process (30ºC ~ 900ºC). (a) CA-LATP (b) AC-LATP (c) EDLATP.
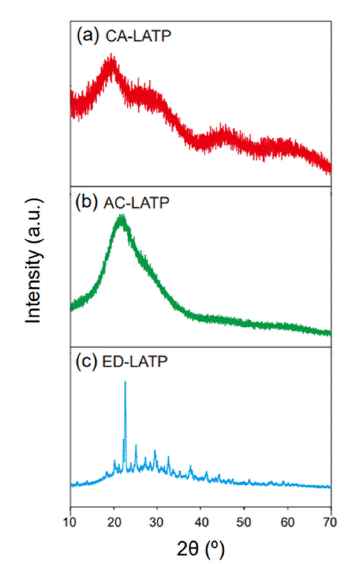
- 하소 전 CA-LATP, AC-LATP, ED-LATP 분말에 대한 결 정화도 및 순도를 확인하기 위해 XRD 분석을 수행하였고 그 결과를 Fig. 2에 나타내었다. Fig. 2a에 보인 바와 같이 하소 전의 CA-LATP와 AC-LATP는 비정질 피크가 관찰 되었다. 반면 ED-LATP는 결정질 피크와 비정질 피크가 모두 관찰되었다. 이는 EDTA를 사용하였을 때 80ºC의 건 조온도에서 결정화가 시작되었음을 알 수 있으며 위에 언 급한 것과 같이 EDTA와 금속이온과의 낮은 결합세기로 인해 건조 중에 결정화가 진행된 것으로 생각할 수 있다. 하지만, 결정화를 이루는데 충분한 온도에 도달하지 않았 기 때문에 합성에 사용된 잔여 산과 유기물이 남아있어 LiTi2(PO4)3(ICDD #35-0754)상 이외의 피크들이 다수 존 재하는 것을 관찰할 수 있다.
- Fig. 3는 하소 후 세 LATP 분말 시료의 XRD 분석 결과 를 나타낸 것이다. 700ºC로 하소한 후 세 시료 모두 결정 질의 NASICON 상이 관찰되었다. CA-LATP는 LiTi2(PO4)3 이외의 이차상 피크가 관찰되지 않아 LATP의 순도가 가 장 높은 것을 확인하였다. 반면 AC-LATP와 ED-LATP는 이차상 피크가 관찰되었는데 특히 acetylacetone을 사용한 LATP는 LiPO3, AlPO4, TiO2 등 다수의 이차상이 존재함 을 확인하였다[25, 26].
- XRD patterns of (a) CA-LATP, (b) AC-LATP, and (c) ED-LATP powder after calcination at 700°C (
 TiO2,
TiO2,  LiPO3,
LiPO3,  AlPO4, and
AlPO4, and  unknown).
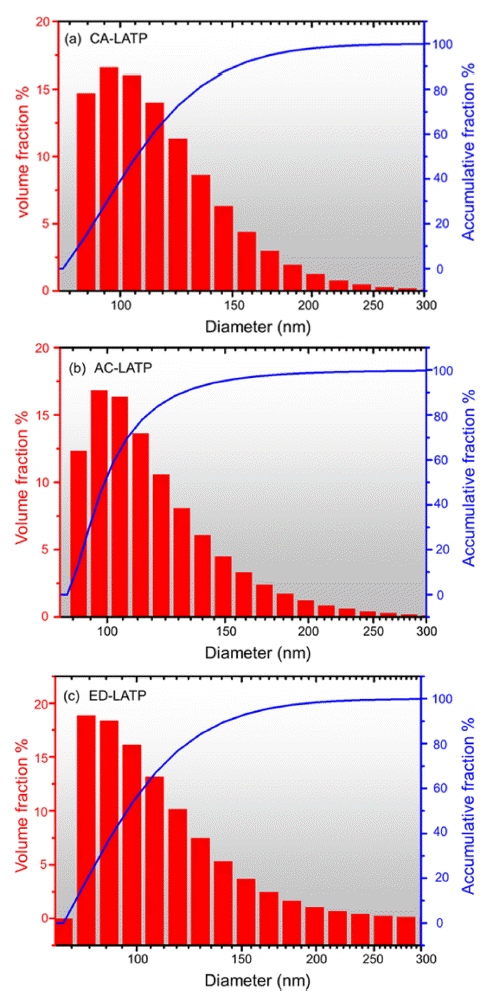
unknown). - 하소한 CA-LATP, AC-LATP, ED-LATP 분말 시료의 입 자 크기 및 분포를 확인하기 위해 산란광의 시간 상관 함 수 형태의 데이터를 입자 확산 상수 분포의 누적 값을 포 함한 DLS 분석을 수행하였고 그 결과를 Fig. 4에 나타내 었다. 기본에 사용되었던 선형 최소 제곱 분석법을 대신하 여 수식이 복잡함에도 불구하고 더욱 정확한 데이터를 얻 을 수 있다고 알려진 비선형적인 누적 분포분석을 통해 CA-LATP, AC-LATP, ED-LATP의 평균 누적 입도는 각각 555.3 nm, 559.6 nm, 359.7 nm 크기의 나노분말이 제조되 었음을 확인하였다[27]. 평균 누적 입도는 ED-LATP가 CA-LATP와 AC-LATP에 비해 더 작은 입자 크기를 확인 할 수 있었다. 더 자세한 분석을 위해 입도가 가장 작은 입자들부터 시작하여 누적 중량이 n%에 도달했을 때의 입도(dn)를 측정했고 d10, d50, d90 분포를 확인한 결과를 Table 1에 정리하였다.
- Size distribution of as-synthesized CA-LATP, AC-LATP and ED-LATP
- Fig. 5는 하소 후 CA-LATP, AC-LATP, ED-LATP 분말 입자의 FE-SEM으로 분석한 결과이다. Fig. 5a와 5b에서 보는 바와 같이 citric acid와 acetylacetone을 chelating agent로 사용하는 경우 크기와 형상이 불균일한 입자가 형 성되는 것을 확인할 수 있다. 반면, EDTA를 사용하는 경 우 단일 입자의 크기가 작고 균일한 입자가 형성되는 것 을 확인할 수 있다. 이는 TGA 분석 결과에서 볼 수 있는 것과 같이 열분해 온도가 가장 낮기 때문에 하소 중 많은 핵이 형성되어 많고 작은 결정립이 생성되었기 때문이라 고 추측된다[24]. 성형체 분말 입자의 크기와 분포는 소결 후 소결체의 밀도에 상당한 영향을 미치는 것으로 보고되 고 있다[28, 29]. 이에 근거한 성형체와 소결체의 밀도를 Table 2에 정리하였다. 성형체의 밀도는 AC-LATP > CALATP > ED-LATP 순으로 높게 나타났고 소결체의 밀도는 CA-LATP > AC-LATP > ED-LATP 순으로 나타났다. 이는 불균일한 입도 분포를 갖는 입자를 사용하면 밀도가 높은 소결체의 제조가 가능한 것으로 판단할 수 있다.
- Density of CA-LATP, AC-LATP, ED-LATP
- Fig. 6은 세 종류의 LATP 분말 시료를 1,000ºC로 소결 한 LATP 소결체의 표면과 파단면의 미세구조를 FE-SEM 으로 분석한 결과이다. Fig. 6(a), (b), (c)에 나타낸 것처럼 CA-LATP, AC-LATP, ED-LATP 모두 직사각형 모양을 갖 는 결정립들이 치밀화가 잘 이루어진 소결체를 관찰할 수 있다. 그 중 AC-LATP는 최대 10 μm 이상의 가장 큰 입 자들을 확인할 수 있고, 치밀화 과정에서 기공 형성이 관 찰되지 않았다. 반면 CA-LATP와 ED-LATP는 비슷한 크 기의 결정립들로 이루어져 있고 작은 기공들이 관찰되었 다. 특히, ED-LATP는 상대적으로 더 균일한 결정립 크기 를 갖지만 크기가 큰 기공들이 발견되었고 이는 소결과정 중 충분한 결정립 성장이 일어나지 않아 치밀화가 상대적 으로 약하게 이루어졌다고 판단된다. 이러한 기공 특성은 파단면에서 더 명확하게 관찰할 수 있다(Fig. 6(d), (e), (f)). CA-LATP와 AC-LATP의 파단면에서는 결정립들이 기공 없이 치밀화되어 있는 모습을 볼 수 있다. 반면 EDLATP는 크기가 큰 닫힌 기공들이 다수 관찰되었고 이로 인해 Table 2에서 나타낸 것처럼 소결밀도가 가장 낮아졌 다고 사료된다.
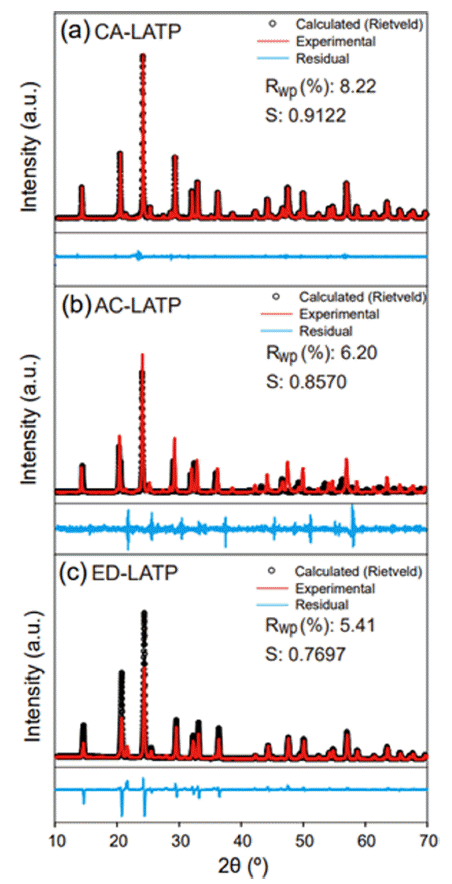
- Fig. 7 소결 후 소결체 형태의 LATP 시료의 XRD 분석 결과로써, TiPO3, AlPO4, TiP2O7 등의 이차상이 존재하지 않고 순수한 LiTi2(PO4)3 상을 나타내는 것을 확인하였다. 특히, CA-LATP에서 (300)와 (410) 면에서 높은 결정질 피 크가 관찰되었다. 이는 CA-LATP가 가장 높은 결정화도를 갖는다는 것을 의미한다. 또한, 분말 회절 패턴으로 결정 구조를 분석하는 일반적인 방법으로 리트벨트 정련법 (Rietveld refinement)을 사용하는데 이를 위해 결정구조의 초기 모델로부터 계산된 패턴을 구하여 측정된 회절 패턴 과 비교했다. 측정된 회절 패턴과 계산된 모델 간의 차이 를 줄이는 과정은 최소제곱법(least-square method)을 통해 반복했다. 최소제곱법은 측정값과 계산값 차이의 제곱의 합 또는 평균을 최소화하도록 매개 변수를 탐색하는 방법 이며 식 (1)를 이용하여 계산할 수 있다. 또한 두 시료 선 폭 평균 결정립자 크기 L을 관련시키는 공식을 다음 식 Scherrer equation (2)을 이용하여 계산하였다. 이때, 적층 결함(stacking fault)에 의한 미세 변형(microstrain)과 같은 효과는 무시하였다[31].
- CA-LATP는 두번의 cycle로 신뢰성 높은 x 값을 얻을 수 있었는데 반해 AC-LATP와 ED-LATP의 경우 18 cycle 과정을 거쳐야만 1에 가까운 x 값을 얻을 수 있었다.
- R-factor of CA-LATP, AC-LATP and ED-LATP
- Rietveld refinement 후, 측정 모델의 결과가 나타낸 신뢰 성 수치를 토대로 CA-LATP, AC-LATP 그리고 ED-LATP 의 unit volume 차이를 Table 4와 같이 나타내었다. 문헌 에 보고되었던 Li1.5Al0.5Ti1.5(PO4)3의 lattice parameter 와 비교해봤을 때, CA-LATP의 경우 소결 후 lattice volume 이 약 3% 줄어들고 ED-LATP는 거의 동일한 수치를 확인 할 수 있었다. 이에 반해 AC-LATP의 경우 약 7%가 늘어 났는데, 이는 상기 내용에서 언급한 바와 같이 높은 소결 온도에서 기공의 채널이 조기에 닫혀 결정립 성장과 기공 의 성장이 동시에 일어나 치밀화가 늦어진 결과로 추측된 다. 따라서 결정립의 성장이 밀도에 영향을 미치는 것을 확인할 수 있다.
3. Results and Discussion
Fig. 1
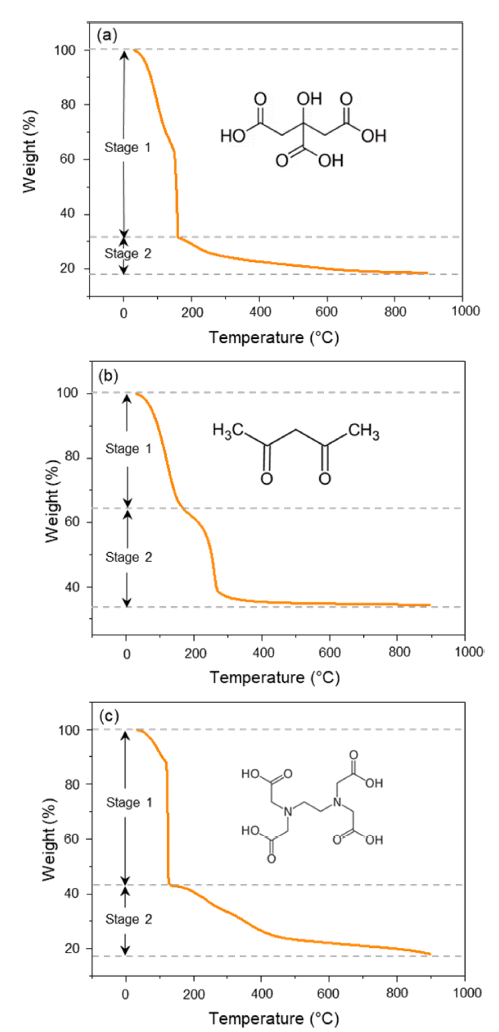

Fig. 3
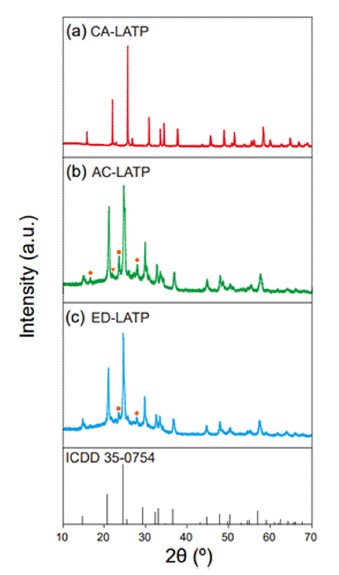

Table 1
| d10 (nm) | d50 (nm) | d90 (nm) | |
|---|---|---|---|
|
|
|||
| CA-LATP | 87.8 | 107.2 | 154.8 |
| AC-LATP | 89.4 | 106.9 | 154 |
| ED-LATP | 78.9 | 96.4 | 141.4 |
Table 2
| Green Body Density (g/cm³) | Sintered Density (g/cm³) | |
|---|---|---|
|
|
||
| CA-LATP | 1.9 ± 0.1 | 2.8 ± 0.1 |
| AC-LATP | 2.1 ± 0.1 | 2.7 ± 0.1 |
| ED-LATP | 1.5 ± 0.1 | 2.2 ± 0.1 |
Table 3
| R-factor | CA-LATP | AC-LATP | ED-LATP |
|---|---|---|---|
|
|
|||
| Rp (%) | 6.61 | 11.99 | 6.66 |
| Rwp (%) | 8.60 | 15.07 | 8.77 |
| χ2 | 1.5745 | 3.9485 | 1.7163 |
- 본 연구에서는 세 종류의 chelating agent(citric acid, acetylacetone, EDTA)를 사용하여 LATP 고체전해질을 제 조한 후 LATP 분말의 열적 특성 및 미세구조, LATP 소결 체의 미세구조 특성을 비교하였다. 금속이온과 chelating agent와의 열분해 시작 온도는 AC-LATP > CA-LATP > ED-LATP 순으로 높았다. 열분해 온도가 낮을수록 금속 이온과 chelating agent 사이의 결합 세기가 약하며 결정화 온도가 낮기 때문에 열분해 온도가 가장 낮은 ED-LATP 는 하소 중 많은 핵이 형성되어 다량의 작은 결정립 생성 으로 인해 작고 균일한 입자가 형성되었다. 반면 CALATP와 AC-LATP는 크기가 큰 결정립이 생성되었고 불 균일한 입도 분포를 나타냈다. 이러한 특성을 갖는 CALATP와 AC-LATP는 소결 후 각각 2.8 g/cm3, 2.7 g/cm3의 높은 소결 밀도를 가진 반면 ED-LATP의 경우 crosssection에서 다수의 닫힌 기공이 발견되었고 이로 인해 2.2 g/cm3의 가장 낮은 소결 밀도를 가졌다. 따라서 열분해 온 도가 높은 chelating agent를 사용할수록 입자의 크기가 크 고 불균일한 입도 분포를 나타내며, 상대적으로 치밀한 LATP 고체 전해질을 제조할 수 있는 것으로 판단된다.
4. Conclusion
-
Acknowledgements
- 이 성과는 정부(과학기술정보통신부)의 재원으로 한국 연구재단의 지원을 받아 수행된 연구임(No. 2022R1C1C 100653612 and RS-2023-00221237).
Acknowledgement
- 1. R. Shah, B. Gashi, S. Gonzalez-Poggini, M. Colet-Lagrille and A. Rosenkranz: Adv. Mech. Eng., 13 (2021) 1687..Article
- 2. G. G. Eshetu, H. Zhang, X. Judez, H. Adenusi, M. Armand, S. Passerini, E. Figgemeier: Nat. Commun., 12 (2021) 5459..ArticlePubMedPMC
- 3. M. Fichtner: Batter. Supercaps., 5 (2022) 2566..Article
- 4. J. Lau, R. H. DeBlock, D. M. Butts, D. S. Ashby, C.-S. Choi and B. S. Dunn: Adv. Energy Mater., 8 (2018) 1800933..Article
- 5. M. Qin, Z. Zeng, S. Cheng and J. Xie: Interdiscip Mater., 2 (2023) 308..Article
- 6. A. Sohib, J. Karunawan, C. Deliana D. Sundari, O. Floweri and F. Iskandar: J. Phys.: Conf. Ser., 2243 (2022) 012044..Article
- 7. J. Feng, L. Wang, Y. Chen P. Wang, H. Zhang and X. He: Nano Convergence, 8 (2021) 2..ArticlePubMedPMC
- 8. S. Chen, D. Xie, G. Liu, P.-M. Jean, Q. Zhang, Y. Zhao, X. Xu and X. Yao: Energy Stor. Mater., 14 (2018) 58..Article
- 9. K. Kerman, A. Luntz, V. Viswanathan, Y.-M. Chiang and Z. Chen: J. Electrochem. Soc., 164 (2017) 1731..Article
- 10. M. V. Reddy, C. M. Julien, A. Mauger and K. Zaghib, K: Nanomaterials, 10 (2020) 1606..ArticlePubMedPMC
- 11. F. Ichilhara, S. Miyoshi and T. Masuda: Phys. Chem. Chem. Phys., 24 (2022) 25878..ArticlePubMed
- 12. H. Raj, T. Fabre, M. Lachal, A. Neveu, J. Jean, M.-C. Steil, R. Bouchet and V. Pralong: ACS Appl. Energy Mater., 6 (2023) 1197..Article
- 13. R. DeWees and H. Wang: ChemSusChem., 12 (2019) 3713..ArticlePubMed
- 14. C.-J. Park, S.-M. Na, H.-G. Park and K.-J. Park: ACS Appl. Mater. Interfaces., 15 (2023) 26985..ArticlePubMed
- 15. Q. Ma, Q. Xu, C.-L. Tsai, F. Tietz and O. Guillon: J. Am. Ceram. Soc., 99 (2016) 410..Article
- 16. A. Wibowo, R. F. Indrawan, L. A. Tresna Wulan Asri, S. S. Rahardi and B. S. Purwasasmita: Conf. Ser.: Mater. Sci. Eng., 509 (2019) 012021..Article
- 17. R. Wei, S. Chen, T. Gao and W. Liu: Nano Select., 2 (2021) 2256..Article
- 18. K. Sinwinska-Stefanska, J. Zdarta, D. Paukszta and T. Jesionowski: J. Sol-Gel. Technol., 75 (2015) 264..Article
- 19. B. J. Hwang, R. Santhanam and D. G. Liu: J. Power Sources., 97 (2001) 443..Article
- 20. M. S. Mastuli, N. Kamarulzaman, M. A. Nawawi, A. M. Mahat, R. Rusdi and N. Kamarudin: Nanoscale Res Lett., 9 (2014) 134..ArticlePubMedPMC
- 21. N. Osman, A. A. Samat, A. N Che Mat, N. I. Abd Malek and J. Andas: Ceram. Int., 48 (2022) 2289..Article
- 22. Y.-S. Ho, C.-H. Wu, Y.-S. Chen and C.-K. Liu: Int. J. Appl. Ceram. Technol., 12 (2015) E53..Article
- 23. N. A. Abdullah, N. Osman, S. Hasan and O. H. Hassan: Int. J. Electrochem. Sci., 7 (2012) 9401..Article
- 24. M. R. Ghaani, A. M. Mohtasebi, R. Tajeri and P. Marashi: Batteries., 6 (2020) 48..Article
- 25. D. Chen, Y. Liu, F. Luo, J. Tang and Y. Zhou: J. Mater Sci: Mater. Electron., 31 (2020) 13724.
- 26. X. Hu, Y. Chen, Z. Hu, Y. Li and Z. Ling: J. Electrochem. Soc., 165 (2018) 1269..Article
- 27. S. Duluard, A. Paillassa, L. Puech, P. Vinatier, V. Turq, P. Rozier, P. Lenormand, P.-L. Taberna, P. Simon and F. Ansart: J. Eur. Ceram. Soc., 33 (2013) 1145..Article
- 28. G. Zhang, J. Li and Y. Wu: Ceram. Int., 48 (2022) 25120..Article
- 29. Y. Zhang, H. Wu, B. Jia, D. Zhang, Y. Wang, Z. Zhang, X. Qu and M. Qin: Ceram. Int., 48 (2022) 18165..Article
- 30. P. Liang, Z. Pan, L. Tang, G. Zhang, D. Yang, S. He and H. Yan: Batteries, 15 (2022) 2232..ArticlePubMedPMC
Figure & Data
References
Citations
Citations to this article as recorded by 

- Uniform lithium deposition using Cu teepee structures for anode-free lithium metal batteries
Seo Yun Jung, Jaehun Han, Seul Ki Choi, Se Youn Cho, Jong Ho Won, Jaewon Choi, Minho Yang
Chemical Engineering Journal.2025; 522: 167302. CrossRef
Effect of Chelating Agent on Li1.5Al0.5Ti1.5(PO4)3 Particles by Sol-gel Method and Densification
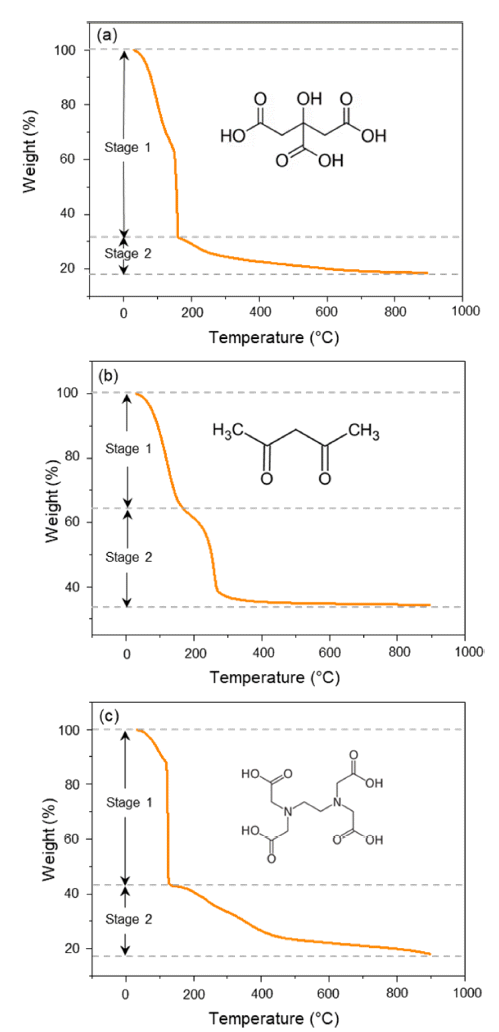

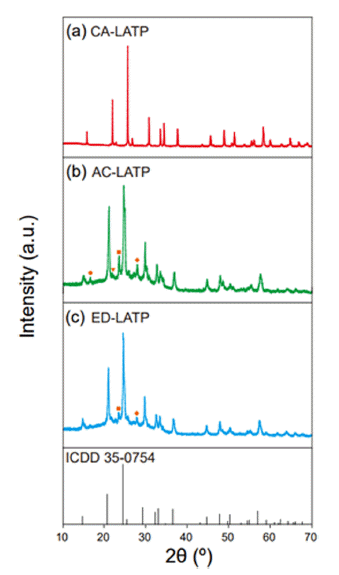
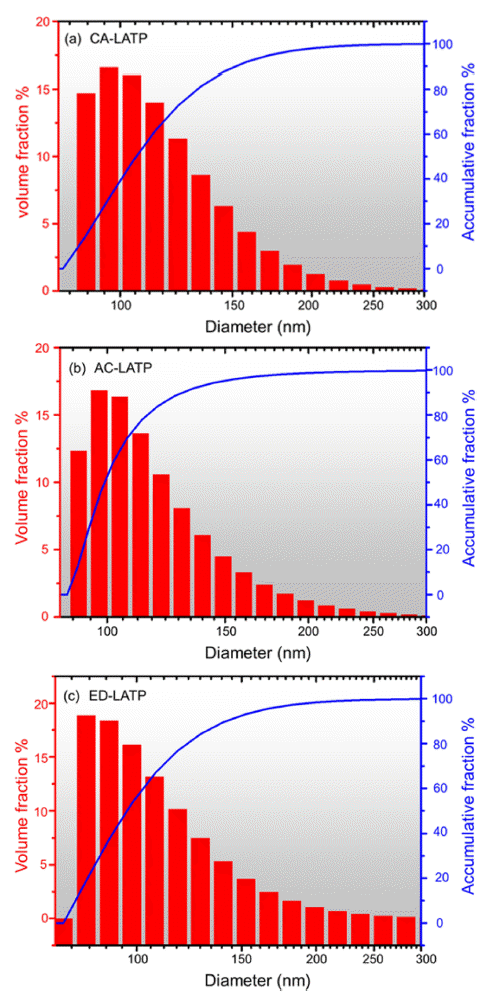



Fig. 1
TGA curves of LATP gel synthesized by sol-gel process (30ºC ~ 900ºC). (a) CA-LATP (b) AC-LATP (c) EDLATP.
Fig. 2
XRD patterns of (a) CA-LATP, (b) AC-LATP, and (c) ED-LATP powder before calcination.
Fig. 3
XRD patterns of (a) CA-LATP, (b) AC-LATP, and (c) ED-LATP powder after calcination at 700°C ( TiO2, LiPO3, AlPO4, and unknown).
Fig. 4
Size distribution of synthesized (a) CA-LATP, (b) ACLATP and (c) ED-LATP.
Fig. 5
FE-SEM images of (a) CA-LATP, (b) AC-LATP, (c) ED-LATP powder after calcination.
Fig. 6
FE-SEM images for (a - c) surface and (d - f) cross-section of LATP pellet.
Fig. 7
XRD patterns of (a) CA-LATP, (b) AC-LATP, (c) EDLATP pellet sintered at 1,000ºC for 10 h.
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Fig. 7
Effect of Chelating Agent on Li1.5Al0.5Ti1.5(PO4)3 Particles by Sol-gel Method and Densification
| d10 (nm) | d50 (nm) | d90 (nm) | |
|---|---|---|---|
|
|
|||
| CA-LATP | 87.8 | 107.2 | 154.8 |
| AC-LATP | 89.4 | 106.9 | 154 |
| ED-LATP | 78.9 | 96.4 | 141.4 |
| Green Body Density (g/cm³) | Sintered Density (g/cm³) | |
|---|---|---|
|
|
||
| CA-LATP | 1.9 ± 0.1 | 2.8 ± 0.1 |
| AC-LATP | 2.1 ± 0.1 | 2.7 ± 0.1 |
| ED-LATP | 1.5 ± 0.1 | 2.2 ± 0.1 |
| R-factor | CA-LATP | AC-LATP | ED-LATP |
|---|---|---|---|
|
|
|||
| Rp (%) | 6.61 | 11.99 | 6.66 |
| Rwp (%) | 8.60 | 15.07 | 8.77 |
| χ2 | 1.5745 | 3.9485 | 1.7163 |
| lattice parameter (Å) | ||||
|---|---|---|---|---|
| a (Å) | b (Å) | c (Å) | lattice volume (Å) | |
|
|
||||
| Li1.5Al0.5Ti1.5(PO4)3 | 8.50 | 8.50 | 20.82 | 1302.71 |
| CA-LATP | 8.494 | 8.500 | 20.787 | 1262.801 |
| AC-LATP | 8.509 | 8.509 | 20.826 | 1399.899 |
| ED-LATP | 8.477 | 8.477 | 20.744 | 1301.275 |
Table 1
Size distribution of as-synthesized CA-LATP, AC-LATP and ED-LATP
Table 2
Density of CA-LATP, AC-LATP, ED-LATP
Table 3
R-factor of CA-LATP, AC-LATP and ED-LATP
Table 4
Lattice parameter of CA-LATP, AC-LATP and ED-LATP
Table 1
Table 2
Table 3
Table 4
TOP
 KPMI
KPMI



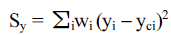
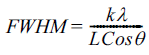
 Cite this Article
Cite this Article