Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 22(4); 2015 > Article
-
Article
새로운 용액환원법에 의한 구형 코발트 미세 분말의 제조 - 김대원, 김지훈, 최요한, 최희락a, 윤진호b,*
- Preparation of Spherical Cobalt Fine Powders by New Liquid Reduction Method
- Dae Weon Kim, Ji-Hoon Kim, Yo-Han Choi, Hee Lack Choia, Jin-Ho Yoonb,*
-
Journal of Korean Powder Metallurgy Institute 2015;22(4):260-265.
DOI: https://doi.org/10.4150/KPMI.2015.22.4.260
Published online: July 31, 2015
㈜미산
부경대학교 재료공학과
b 고등기술연구원 신소재공정센터
Misan Co. Ltd., Gyeongsangbukdo 730-030, Korea
a Dept. of Materials System Engineering, Pukyong National University, Busan 608-739, Korea
b Advanced Materials & Processing Center, Institute for Advanced Engineering, Gyeonggido 449-863, Korea
- * Corresponding Author: Jin-Ho Yoon, TEL: +82-31-330-7491, FAX: +82-31-330-7116, E-mail: yjh6373@iae.re.kr
© The Korean Powder Metallurgy Institute. All rights reserved.
- 932 Views
- 5 Download
Abstract
- Spherical fine cobalt powders were fabricated by new liquid reduction method. Commercial cobalt sufate heptahydrate was used as raw material. Also ethylene glycol was used as solvent and hydrazine-sodium hypophosphite mixture was used as reduction agent for the new liquid reduction method. A plate shaped cobalt powders with an approximately 300 nm were prepared by a traditional wet ruduction method using distilled water as solvent and hydrazine. Spherical fine cobalt powders with an average size of 1-3 μm were synthesized by a new liquid reduction method in 0.3M cobalt sulfate and 1.5M hydrazine-0.6M sodium hypophosphite mixture at 333K.
- 코발트 (Co) 는 주로 전지, 초내열합금, 공구강, 촉매 등 다양한 분야에 사용되고 있는 핵심금속 중 하나로서 최근 에는 우주항공산업과 국방소재 등으로 사용되는 전략물자 로서 취급하고 있다. 특히 초경재료의 경우 WC, TiC 등 의 입자의 결합제로서 사용되며 초경재료의 특성을 향상 시키기 위해서는 코발트 입자의 크기와 형태 제어가 매우 중요하다[1].
- 일반적으로 코발트 금속 분말을 합성하는 방법으로는 액상환원법[1-7], 폴리올법 (polyol method)[8-12], 수소환 원법[13-15], 전해정련법[16] 등이 있다. 수소환원법은 고 온 및 고압에서 수소가스를 넣어 수소에 의한 환원을 통 해 코발트 분말을 제조하는 방법으로 미세한 분말의 제조 가 가능하나 환원반응으로 인한 융합 및 응집으로 분쇄 및 분급과정이 필요하다는 단점이 있다. 또한, 많이 연구 되고 있는 방법 중 하나인 폴리올법은 핵생성으로부터 입 자성장제어가 가능하지만, 150°C이상의 고온 환경이 필요 하여 경제성 측면에서 액상환원법에 비해 불리하다.
- 액상환원법은 타 공정에 비하여 반응속도, 반응온도 등 비교적 쉽게 제어가 가능하고 공정이 간단하여 기술적 측 면뿐만 아니라 상용성 및 경제성 측면에서 매우 유리한 공정이다. 그러나 기존의 액상환원법은 코발트 분말의 입 자 형상제어 측면에서 있어서 어려움이 있다. 따라서 본 논문에서는 수 μm의 크기를 가지는 구형 코발트 금속 분 말을 얻기 새로운 용액환원법을 개발하여 실험을 실시하 였다.
1. 서 론
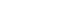
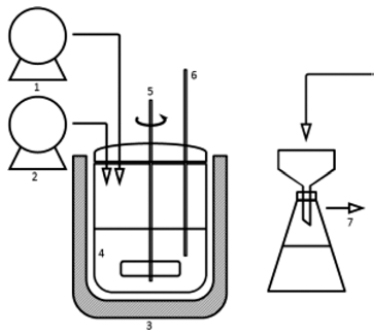
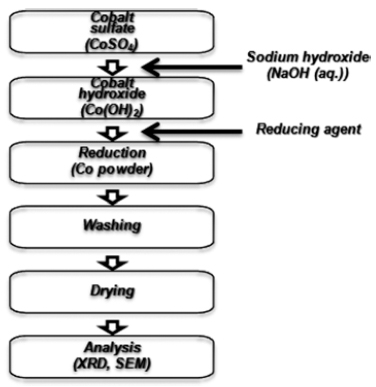
- 기존 액상환원법을 이용한 실험에 사용된 원료는 금속 코발트 분말의 상용화 및 경제성을 고려하여 국내에서 대 량 생산되고 있는 황산코발트 (CoSO4·7H2O, S.I.하이텍) 을 이용하였다. 용매로써 증류수 및 에틸렌글리콜(Ethylene glycol, 시약급, DaeJung) 을 사용하였으며, 환원제로 하이 드라진 (hydrazine, N2H4·H2O, J.Y. Chemical) 을 사용하 였다. 또한 환원제의 종류에 따른 영향을 관찰하고자 환원 제로 하이드라진 (hydrazine, N2H4·H2O, J.Y. Chemical) 에 차아인산나트륨 (sodium hypophosphte, NaH2PO2, 시약급, DaeJung), 및 수소화붕소나트륨 (sodium borohydride, NaBH4, 시약급, DaeJung) 을 각각 혼합하여 사용하였다. 새로이 개발하고자 하는 코발트 분말의 액상환원 공정을 위하여 코발트 전구체로써 증류수 및 에틸렌글리콜 용액에 고상 의 황산코발트를 혼합한 후 용해시켜 사용하였다. 그 후 기존 공정과 유사하게 50% 수산화나트륨 수용액을 혼합 하여 약 30분 정도 반응시켜 중간물질 생성 후 환원제로 하이드라진에 차아인산나트륨, 하이드라진에 수소화붕소 나트륨을 각각 혼합하여 사용하였다. 기본적인 실험공정 도는 그림 1과 같이 나타내었으며 표 1을 통해서 기존 공 정과 새로운 공정을 비교하였다. 반응에 사용한 반응기는 그림 2와 같은 5 L 용량의 유리반응기를 사용하여, 온도 60°C에서 300 rpm의 속도로 교반하였다. 온도 heating mantle을 이용하여 온도를 유지하였으며, pH meter를 사 용하여 pH의 변화를 확인하였다.
- 첨가하는 수산화나트륨의 양은 몰비로 [NaOH]/[Co]의 값이 6~12이 되도록 넣어주었고, pH는 11 이상이 되도록 조절하였다. 그리고 환원반응은 하이드라진 및 하이드라 진-차아인산나트륨 혼합액의 비율을 몰비로 [Reduction Agent]/[Co]=4~10을 천천히 투입하여 코발트 분말의 제조 하였다. 환원반응이 종료된 후 생성된 코발트 분말의 3회 정도 수세한 후 여과하여 70°C에서 12시간 이상 건조하여 하였다. 제조된 코발트 분말의 형상과 크기는 전자현미경 (FE-SEM, JSM6500F, JEOL) 으로 관찰하였으며, 결정상 은 X선회절장치 (XRD, X-Ray Diffractometer, X-Max12000, Rigaku) 를 이용하여 분석하였다.
2. 실험방법
Apparatus for fabrication of the Co powder; 1. CoSO4 solution, 2. NaOH solution, 3. heating mantle, 4. reactor, 5. stirrer, 6. thermometer, 7. vacuum.
Reagent for traditional process and new process
- 3.1. 기존 액상반응에 의한 실험
- 본 연구에서 실시한 새로운 액상환원법과 기존의 실험 결과를 비교하기 위하여 기존 연구에서 제시하였던 액상 환원 실험을 실시하였다[17]. 비교 실험에서는 논문에서 원료로 사용된 염화코발트를 대신하여 상용 황산코발트를 사용하였으며 CoSO4·7H2O:(8~10)NaOH:(2~8)N2H4의 몰 비율로 실험을 진행하였다. 반응온도 및 반응시간은 60°C, 1 hr로 고정하였으며, 환원반응 후 코발트의 입자 형상은 그림 3에 나타내었다. Won[17]의 실험 결과에서는 수지상 (dendrite) 구조로 코발트가 형성되었지만 황산코발트를 이 용한 비교 실험에서는 수 nm 폭과 300 nm 이상의 크기를 가지는 판상의 코발트가 관찰되었다. 이는 한국지질자원 연구소에서 제시한 특허[18]에서도 확인이 가능하였는데 염화코발트를 증류수에 녹인 후 수산화나트륨으로 수산화 코발트를 제조하고 하이드라진으로 환원하였을 때 수지상 의 코발트 입자를 제시하였으며, 이는 고체와 액체 사이의 계면에서 원자를 끌어당기는 속도의 영향으로 인하여 특 정의 방향으로 입자가 성장하기 때문이다.
- 염화코발트 및 황산코발트를 원료로 하여 환원반응 과 정은 다음과 같다.
- 상기 반응식에서 수산화나트륨은 중간물질인 수산화코 발트를 형성하고, 하이드라진의 환원에 필요한 OH− 이온 을 제공해 주는 역할을 한다. 코발트 분말을 제조하기 위 하여 필요한 양은 수산화코발트를 형성하는데 2M이 필요 하며, 코발트 금속으로 환원하기 위하여 2M이 필요하여 이론적으로 총 4M의 농도가 필요하다. 그러나 실제 환원 반응에서는 수산화코발트가 금속 코발트로 환원되기 위해 서 이론양의 약 2배 이상의 수산화나트륨이 필요하기 때 문에 본 연구에서는 수산화나트륨 양을 8M 이상의 농도 로 설정하여 사용하였다.
- 그림 4는 코발트 대비 수산화나트륨양을 6배 및 10배, 하이드라진의 양을 8배로 하여 환원하였을 때의 XRD 결 과를 나타낸 것이다. 코발트 대비 수산화나트륨 첨가량이 6배 일 때, 수산화코발트 피크가 나타난 것으로 보아 환원 이 완전히 이루어지지 않았음을 알 수 있으며, 수산화나트 륨 첨가량을 10배로 하였을 때는 수산화코발트의 피크가 사라진 것으로 보아 모든 수산화 코발트가 코발트 분말로 환원된 것으로 보인다.
- 또한, 환원제의 종류에 따른 코발트 형상을 살펴보기 위 하여 앞서 실험과는 달리 환원제로 하이드라진과 수소화 붕소나트륨 및 하이드라진과 차아인산나트륨 혼합액을 각 각 사용하여 환원실험을 실시하였고 그 결과를 그림 5에 나타내었다. 그림 5의 (a)는 황산코발트 수용액에 수산화 나트륨으로 수산화코발트를 제조한 후 하이드라진과 수소 화붕소나트륨 혼합액을 이용하여 환원하여 얻은 코발트 분말로서 하이드라진만 사용하였을 경우와 비교하여 보면 판상의 구조에서 부정형의 구조로 변화하는 현상이 보이 며 심하게 응집되어 있음을 확인할 수 있다. 그림 5의 (b) 는 액상환원 시 하이드라진과 차아인산나트륨 혼합액을 이용하여 얻은 분말로 (a)와 유사한 결과를 보이고 있다. 이는 용매가 증류수인 경우, 생성된 입자 표면이 산화되면 서 부정형의 형태를 가지게 하였거나 환원력이 약하여 입 자 생성보다 입자 성장에 의한 영향으로 방향성을 가지 고 성장하여 환원되어 가는 과정에서 응집된 것이라 추 측된다.
- 3.2. 새로운 액상반응에 의한 실험
- 새로운 액상환원반응을 연구하기 위한 본 실험에서는 용매로서 증류수가 아닌 에틸렌글리콜을 선택하여 실험을 실시하였다. 기존 폴리올 공정에서는 200°C이상의 높은 온도에서 환원공정이 이루어 졌지만 본 실험에서는 60°C 의 낮은 온도에서 합성을 실시하였으며, 또한 하이드라진 등의 환원제를 추가로 첨가하여서 수산화 코발트의 환원 력을 향상시키고자 하였다.
- 우선 에틸렌글리콜 600 ml에 황산코발트 0.3M를 넣어 황산코발트용액을 제조한 후 50% 수산화나트륨 용액을 300 rpm의 속도로 회전시키면서 코발트 전구체를 제조하 였으며, 이때의 온도는 60°C로 하였다. 약 30분 정도 반응 이 완료된 후 하이드라진 및 하이드라진-차아인산나트륨 혼합액을 천천히 투입시키면서 환원반응을 실시하여 코발 트 분말을 합성하였다. 새로운 폴리올 공정을 통해서 합성 된 코발트 분말을 그림 6과 그림 7에 나타내었으며 코발 트의 생성 여부를 확인하기 위하여 XRD 측정 결과를 그림 8에 나타내었다.
- 황산코발트의 용해를 위한 용매로서 에틸렌글리콜을 이 용한 경우 하이드라진만을 환원제로 사용하였 때 그림 6 과 같이 수 μm의 판상의 형태가 응집되어 있는 형상을 가 졌으며, 하이드라진-차아인산나트륨 혼합액을 환원제로 사용하였을 경우에는 그림 7과 같이 대략 1~3 μm의 원형 의 코발트 미세분말이 얻을 수 있었다. 이는 에틸렌글리콜 의 경우, 온도에 따라 그 환원력이 다르지만, 에틸렌글리 콜 자체로도 환원력을 가지고 있어 일반 환원제만을 사용 하였을 경우보다 강한 환원력을 통해 입자가 특정 방향으 로 성장하기 전에 입자 생성이 훨씬 많이 되어 1~3 μm크 기의 비교적 작은 분말 크기를 갖으면서 구형인 분말이 형성된 것으로 추측된다. 그림 8에 XRD 결과를 보면 [NaOH]/[Co]=8, [N2H4]/[Co]=4, [NaH2PO2]/[Co]=1.6의 조 건에서 코발트 결정의 피크가 확인되었고 그 밖의 피크는 확인되지 않았다. 이를 통하여 코발트가 합성되었음을 알 수 있다. 또한 피크를 보면 FCC구조의 코발트와 HCP 구 조를 갖는 코발트가 혼재 되어 있음을 확인 할 수 있는데 이는 FCC 코발트와 HCP 코발트는 동소체로 이들 구조 사이의 에너지 차이가 적고 구조 전이가 느리기 때문이다.
- 본 연구에서 사용한 에틸렌글리콜 공정의 반응식은 다 음과 같다.
- (1) 과정은 에틸렌글리콜의 탈수(dehydration) 반응으로 우선 아세트알데히드(Acetaldehyde, C2H4O)가 생성되고, (2) 과정에서 생성된 아세트알데히드는 코발트염과의 반 응을 통하여 디아세틸(Diacetyl, C2H3O)이 되면서 H+와 e− 를 발생시키며, 발생된 e-는 코발트 이온을 환원시켜 금속 코발트를 생성시킨다. 이러한 에틸렌글리콜의 초기 환원 반응으로 핵을 생성시켜, 추후에 첨가되는 환원제에 의해 핵 주위에서 성장함으로서 구형의 모양이 형성되는 것으 로 보인다. 따라서 기존의 폴리올 공정보다 100°C이상 낮 은 온도에서 환원제를 추가로 첨가하면 구형의 코발트 분 말이 형성되는 것이 확인되었으며 이렇게 합성된 코발트 분말은 초경공구, 3D프린터용 분말의 원료로 사용가능할 것으로 예상된다.
3. 실험결과 및 고찰
SEM images of Cobalt powders; (a) [NaOH]/[Co]=8, [N2H4]/[Co]=8 and (b) [NaOH]/[Co =12, [N2H4]/[Co]=4.

SEM images of Cobalt powders; (a) [N2H4]/[Co]=6, [NaBH4]/[Co]=1 and (b) [N2H4]/[Co]=6, [NaH2PO2]/[Co]=1.

- 본 연구에서는 기존의 액상환원법 및 폴리올법과는 달 리 두 공정의 장점을 이용하여 원형의 코발트 미세 분말 의 제조하였으며, 그 결론은 다음과 같다.
원형의 코발트 미세 분말의 상용화를 위하여 코발트 의 원료로서 시약급이 아닌 국내에서 생산되는 황산코발 트를 원료로 사용하였다.
용매가 증류수인 경우 하이드라진만으로 환원하였을 때 약 300 nm급의 판상의 코발트를 얻을 수 있었다.
하이드라진과 수소화붕소나트륨, 하이드라진과 차아 인산나트륨 혼합 용액을 각각 환원제로 사용하였을 경우, 부정형의 응집된 코발트 분말이 만들어졌다.
새로운 용액환원법으로 용매로서 에틸렌글리콜을 사 용하여 60°C에서 하이드라진으로 환원하였을 경우, 수 μm 급의 판상의 입자가 응집된 입자 모양이 관찰되었으며, 하 이드라진-차아인산나트륨 혼합액을 환원제로 사용하였을 경우, 1~3 μm의 원형 코발트 미세분말을 제조할 수 있었다.
4. 결 론
-
Acknowledgements
- 본 논문의 산업통상자원부 소재원천기술개발사업의 지 원으로 수행된 연구입니다(과제번호:10050938).
감사의 글
- 1. H. S. Hong, H. C. Jung, G. H. Kim, L. S. Kang and H. G. Suk: J. Korean Powder Metall. Inst., 20 (2013) 191 (Korean). .Article
- 2. S. A. Salman, T. Usami, K. Kuroda and M. Okido: J. of Nanotechnology, 2014 (2014) 1. .Article
- 3. J. P. Chen, K. M. Lee and C. M. Sorenen: J. Appl. Phys., 75 (1994) 5876. .Article
- 4. H. S. Hong, Y. D. Ko, L. S. Kang, G. H. Kim and H. C. Jung: J. Korean Powder Metall. Inst., 18 (2011) 244 (Korean). .Article
- 5. L. P. Zhu, W. D. Zhang, H. M. Xiao, Y. Yang and S. Y. Fu: J. Phys. Chem. C, 112 (2008) 10073. .Article
- 6. S. Ohara, H. Ditaka, J. Zhang, M. Umetsu. T. Naka and T. Adschiri: J. Jpn. Soc. Powd. Powd. Met., 54 (2007) 635. .Article
- 7. J. Z. Gao, Y. C. Zhao, J. N. Tian, W. Yang, F. Guan, Y. J. Ma, J. G. Hou and J. W. Kang: Chinese Chemical Letters, 12 (2001), 555. .
- 8. S. H. An, S. H. Kim, J. H. Lee, H. S. Hong and Y. D. Kim: Kor. J. Mater. Res., 21 (2001) 327 (Korean). .
- 9. D. J. Kim, H. S. Chung, S. D. Woo, J. J. Lee and J. G. Ahn: J. of the Korean Crystal Growth and Crystal Technology, 12 (2002) 73 (Korean). .
- 10. D. J. Kim, H. S. Chung, S. D. Woo and J. J. Lee: J. of the Korean Association of Crystal Growth, 11 (2001) 290 (Korean). .
- 11. M. G. Montiel, P. S. Jacinto, J. A. I. D. Gongora, E. Reguera and G. R. Gattorno: Nano Micro Lett, 3 (2011) 12. .Article
- 12. H. Yang, C. Shen, N. Song, Y. Wang, T. Yang, H. Gao and Z. Cheng: Nanotechnology, 21 (2010) 1. .ArticlePubMed
- 13. J. P. Kim: Trans. of the Korean Hydrogen and New Energy Society, 22 (2011) 35 (Korean). .
- 14. Y. Li, C. Lin and R. Cao: Int. J. of Refractory Metals & Hard Materials, 20 (2010) 270. .Article
- 15. D. J. Kim, H. S. Chung and K. Yu: Material Research Bullentin, 37 (2002) 2067. .Article
- 16. J. H. Huang, C. Kargl-Simard, M. Oliazadeh and A. M. Alfantazi: Hydrometallurgy, 75 (2004) 77. .Article
- 17. H. I. Won, H. H. Nersisyan and C. W. Won: Materials Chemistry and Physics, 133 (2012) 225. .Article
- 18. KIGAM: Korea, KR 10-2011-0122796 (2011)..
Figure & Data
References
Citations

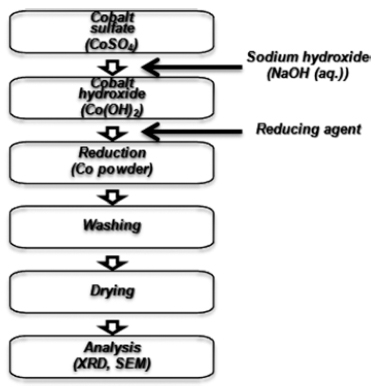
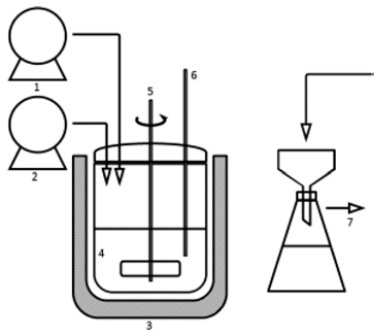

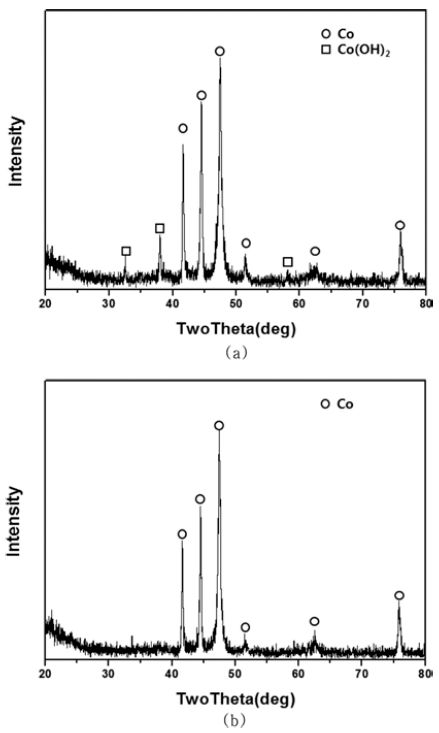




Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Fig. 7
Fig. 8
| Traditional process | New process | |
|---|---|---|
|
|
||
| Raw material | Distilled water, Commercial CoSO4·7H2O powder | Ethylene glycol, Commercial CoSO4·7H2O powder |
| Additives | 50% NaOH solution | 50% NaOH solution |
| Reductant | N2H4·H2O, NaH2PO2, NaBH4 | N2H4·H2O, NaH2PO2 |
Table 1
TOP
 KPMI
KPMI





 Cite this Article
Cite this Article