Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 23(4); 2016 > Article
-
Article
전구체 공침 온도가 LiNi1/3Co1/3Mn1/3O2 분말의 특성에 미치는 영향 - 최웅희, 강찬형*
- Effects of Precursor Co-Precipitation Temperature on the Properties of LiNi1/3Co1/3Mn1/3O2 Powders
- Woonghee Choi, Chan Hyoung Kang*
-
Journal of Korean Powder Metallurgy Institute 2016;23(4):287-296.
DOI: https://doi.org/10.4150/KPMI.2016.23.4.287
Published online: July 31, 2016
한국산업기술대학교 신소재공학과
Department of Advanced Materials Engineering, Korea Polytechnic University, 237 Sangidaehak-ro, Siheung-Si, Kyonggi-Do, 15073, Korea
- * Corresponding Author: Chan Hyoung Kang, TEL: +82-31-8041-0587, FAX: +82-31-8041-0599, E-mail: chkang@kpu.ac.kr
• Received: July 21, 2016 • Revised: August 9, 2016 • Accepted: August 11, 2016
© The Korean Powder Metallurgy Institute. All rights reserved.
- 2,368 Views
- 36 Download
- 1 Crossref
Abstract
- Ni1/3Co1/3Mn1/3(OH)2 powders have been synthesized in a continuously stirred tank reactor via a co-precipitation reaction between aqueous metal sulfates and NaOH using NH4OH as a chelating agent. The co-precipitation temperature is varied in the range of 30-80°C. Calcination of the prepared precursors with Li2CO3 for 8 h at 1000°C in air results in Li Ni1/3Co1/3Mn1/3O2 powders. Two kinds of obtained powders have been characterized by X-ray diffraction (XRD), scanning electron microscopy, particle size analyzer, and tap density measurements. The co-precipitation temperature does not differentiate the XRD patterns of precursors as well as their final powders. Precursor powders are spherical and dense, consisting of numerous acicular or flaky primary particles. The precursors obtained at 70 and 80°C possess bigger primary particles having more irregular shapes than those at lower temperatures. This is related to the lower tap density measured for the former. The final powders show a similar tendency in terms of primary particle shape and tap density. Electrochemical characterization shows that the initial charge/discharge capacities and cycle life of final powders from the precursors obtained at 70 and 80°C are inferior to those at 50°C. It is concluded that the optimum co-precipitation temperature is around 50°C.
- 리튬이온전지는 납축전지, Ni-Cd 전지와 같이 충·방전 이 가능한 2차전지 중의 하나로, 높은 무게당 및 부피당 에너지 밀도, 높은 작동전압, 비교적 긴 수명 등으로 많은 영역에서 활용되고 있다. 특히 최근에는 전기자동차와 에 너지저장시스템에서 효율적인 에너지 활용 가능성으로 리 튬이온전지가 각광을 받고 있다. 가장 먼저 상용화된 양극 소재인 LiCoO2은 구조적으로 안정한 3차원 결정구조를 가진 LiMn2O4나 LiFePO4이 개발되었음에도 불구하고 높 은 이온전도도와 작동전압 등 다양한 측면에서 유리한 특 성을 가지고 있기 때문에 가장 많이 사용되고 있다.
- 코발트의 한정적인 채굴 지역과 비싼 원료 가격 때문에 LiCoO2에서 Co 일부를 Ni과 Mn 등으로 치환한 삼성분계 양극소재가 개발됐다. 삼성분계 양극소재는 고상법[1,2], 분무건조법[2], 분무열분해법[3], 졸겔법[4], 연소법[5] 등 다양한 제조 방법이 제안되었으나, 결정 내 금속 원소의 고른 배치나 생산방식의 용이성으로 공침법[6]을 이용한 전구체(precursor) 제조법이 가장 많이 사용되고 있다. 탄 산염(carbonate) 전구체[7,8]가 제안되기도 했으나 수산염 (hydroxide) 전구체[6,9-11] 공침법이 더 효율적인 기술로 알려져 현재 공업적으로 적용되고 있다. 수산염 전구체는 Li 원소를 포함하는 Li2CO3나 LiOH와 혼합하여 열처리함 으로써 양극소재가 제조된다.
- 수산염 공침법은 보통 Ni, Mn, Co가 결합된 황산염들을 용해시킨 수용액에 염기로서 NaOH, 착화제로서 NH4OH 를 투입하여 공침 반응을 유도한다. 공침법으로 전구체를 합성하는 과정은 크게 3 단계로 나눌 수 있다. 먼저, 핵의 생성과 단결정의 비등방적 성장이 일어나 침상 또는 편상 의 1차 입자가 형성된다(1단계). 이러한 1차 입자들이 서 로 얽히게 된다(2단계). 이렇게 얽힌 1차 입자들은 다시 서로 뭉치는 동시에 다른 1차 입자들이 달라 붙으면서 구 상의 2차 입자가 성장한다(3단계)[12]. 전구체가 합성되는 과정에서 용액의 농도, pH, 교반 속도, 온도 등 다양한 변 수들에 의해 전구체 입자의 형태나 밀도, 1차 입자의 형태 등의 특성이 변하게 된다. 전구체의 크기, 표면 형상 등은 최종 양극소재의 특성을 좌우하므로 공침 공정의 제어를 통해 전구체 분말의 특성을 조절하는 것이 중요하다 [10,11]. 전구체의 형상 및 특성 제어를 위해 반응 용액의 pH, 교반 속도, NH4OH 농도 등의 영향에 대한 연구가 보 고되고 있다[9-13].
- 그러나 공침 반응온도를 변수로 전구체나 최종 양극소 재의 특성을 연구한 보고는 흔하지 않다. 초창기에는 반응 온도에 대한 언급 없이 아마도 상온에서 합성했으나[6], 그 후 반응온도를 50°C[13,14], 또는 60°C[9-12]로 설정하고 있다. 최근에 45, 50, 55°C로 공침 온도를 변화시켜 Ni0.8Co0.1Mn0.1(OH)2 전구체와 양극소재 분말을 합성한 연구가 보고된 바 있다[15]. 본 연구에서는 Ni1/3Co1/3Mn1/3(OH)2 전 구체 분말을 공침법으로 합성하는 공정 중의 여러 변수 중 에서 용액의 온도에 변화를 부여하여 공침 실험을 진행하 였다. 30~80°C의 범위에서 전구체의 공침 합성을 진행하 고, 공침 과정으로 얻은 전구체들을 Li2CO3과 혼합하여 1,000°C에서 8 h 동안 열처리함으로써 양극소재 LiNi1/3Co1/3Mn1/3O2를 합성했다. 이런 과정에서 얻은 전구체와 양극소 재 분말의 결정구조, 표면 형상, 입도, 탭 밀도, 전기화학 적 특성 등을 측정하여 서로 비교하여, 최적의 공침 온도 를 탐구하였다.
1. 서 론
- 전구체의 합성은 5 리터(L) 용량의 연속교반탱크반응기 (Continuously Stirred Tank Reactor; CSTR)에서 이루어졌다. 반응기의 구조와 공침 공정에 대해서는 이전 논문[14]에 언 급되어 있다. NiSO4·6H2O(대정화금, 98.5%), CoSO4·7H2O (대정화금, 98.0%), MnSO4·H2O(대정화금, 98.0%)의 세가지 전이금속황산염을 1:1:1의 몰 비로 초순수에 용해시켜 2.4M의 금속용액을 만들고, 4.8M의 NaOH(대정화금, 97.0%)와 7.2 M의 NH4OH(대정화금, 25~28%) 용액을 초 순수에 용해시켜 준비하였다. NaOH는 pH가 10.5가 되도 록 센서와 연결된 펌프로 투입량을 자동적으로 조절했으 며, 금속용액은 4 mL/min, NH4OH 용액은 0.4 mL/min의 속도로 반응탱크로 투입했다. 원료 투입 전에 반응기에 초 순수를 부은 후 1 h 동안 질소를 불어(purge) 넣고, 원료 투입 도중에는 40~50 sccm의 질소를 투입하였다. 반응용 액의 교반 속도는 900 rpm을 유지하였다. 반응 온도는 외 부의 순환기(circulator)를 이용해 탱크 외부의 재킷(jacket) 으로 온수를 순환시켜 조절했다. 온도는 30, 50, 60, 70, 80°C로 변화시켰다.
- 공침 공정이 진행되는 동안, 일정 시간 간격으로 반응탱 크의 배출구로 흘러 넘치는 전구체를 포함하는 용액을 채 취(sampling)하였다. 이러한 과정을 통해 채취된 전구체 용액은 거름종이로 여과한 후 건조했는데, 효율적인 여과 과정을 진행하기 위해 흡인기(aspirator)를 사용했다. 그리 고 전구체에 남아있을 수 있는 Na2SO4나 암모니아 등의 불순물을 씻어내기 위해 초순수를 40~50°C로 데워 여과과 정 중에 전구체에 수 차례 붓는 방식으로 세척과정을 진행했 다. 여과, 세척, 건조 과정을 거친 전구체는 Li2CO3(Sigma Aldrich, 99.0%)와 혼합하여 열처리했다. 열처리 과정 중의 리튬 손실량 보충과 리튬이 전구체로 충분하게 확산되도록 하기 위해 Li2CO3의 비율을 약간 높인 전구체: Li2CO3= 2:1.05의 비율로 혼합한 다음, 튜브로(tube furnace)에 넣어 공기 분위기에서 열처리 공정을 진행했다. 승온 속도는 2°C/min로 설정했으며, 1,000°C에서 8 h 동안 열처리를 진행 하였다.
- 전구체와 양극소재를 분석하기 위해 X선 회절(X-Ray Diffraction; XRD), 주사 전자 현미경(Scanning Electron Microscopy; SEM), 탭 밀도 측정, 입도 분석, 충·방전 평 가를 진행했다. 먼저 XRD는 Cu-Kα(λ = 1.54Å)로 분당 5°/min의 스캔 속도로 10~80°의 범위를 분석하여 전구체 와 양극소재의 결정구조에 대한 정보를 얻었다. 그리고 양 극소재는 XRD 분석을 통해 얻은 정보를 이용하여 격자상 수를 계산하였다. SEM은 전구체와 양극소재의 표면 관찰 을 위해 사용했으며, 1차 입자와 2차 입자의 형상을 관찰 함으로써 공침 반응 온도에 따른 입자 형상의 차이를 살 펴봤다. 또한 분말의 탭 밀도를 측정함으로써 입자의 유동 성을 평가했고, 입도분석기(Particle Size Analyzer)를 이용 해 입도 분포를 측정했다.
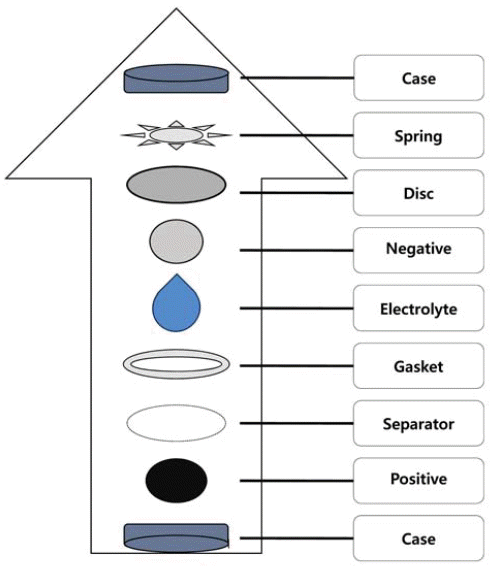
- 제조된 양극소재의 전기화학적 성능을 평가하기 위해 전 극을 제조했다. 양극소재와 바인더(Polyvinylidene Difluoride; PVDF), 도전재(super-p)가 90:5:5의 비율로 NMP(N-Methyl- 2-Pyrrolidone)에 용해되어 혼합된 슬러리(slurry)를 제조하여 Al 포일 위에 도포한 뒤, micrometer applicator를 이용하여 일정한 두께로 Al 포일 위에 슬러리가 도포되도록 했다. 그 리고 건조된 슬러리가 도포된 Al 포일을 롤 프레스(roll press)로 압착하여 NMP가 증발된 뒤에 남은 전극 물질들 간의 공극을 줄였다. 이러한 과정을 통해 제작된 전극은 펀치를 이용해 원형의 전극으로 만든 다음, Ar 분위기의 글러브 박스 내에서 그림 1과 같은 구조와 순서로 코인 셀 (coin cell)을 조립하였다. 음극으로 Li 금속 포일을 사용하 고, 전해액은 LiPF6를 EC(Ethylene Carbonate):EMC(Ethyl Methyl Carbonate) = 1:1(v/o) 유기용매에 1 M의 농도로 용 해하여 사용했다. 분리막은 Celgard 2400을 사용했다. 완성 된 셀은 Wonatech 사의 충·방전 측정기를 이용해 3.0~4.3 V vs. Li/Li+의 전압 범위에서 초기 충·방전 특성과 30 사이 클 수명 평가를 실시하였다.
2. 실험방법
- 3.1. XRD 분석
- 그림 2는 각 공침 반응 온도에서 48 h 동안 합성된 전구 체 분말의 XRD 결과이다. 전구체가 저온인 30°C~80°C의 범위에서 합성되어 각 피크의 세기가 작고 일부 피크는 현저하게 감소되어 희미하게 관찰되고 있다. 그림 2의 XRD 패턴은 다른 연구팀의 보고[9-13]와 유사한 것으로 학계에서는 이 패턴을 Ni1/3Co1/3Mn1/3(OH)2 물질로 동정 (identification)하고 있다. Ni(OH)2와 Ni1/2Mn1/2(OH)2 물질 도 동일한 XRD 패턴을 나타낸다고 보고되고 있다[11]. 그 림 2에서 38° 부근에 작은 피크가 관찰되는데, 이를 Co(OH)2 와 연관시키는 보고[16,17]가 있다. 그림 2에서 보면 대체 적으로 공침 반응 온도가 증가할수록 각 피크의 강도가 증가함을 알 수 있다.
- 그림 3은 각 공침 반응 온도에서 48 h 동안 합성된 전구 체 분말을 각각 Li2CO3와 혼합한 후 1,000°C에서 8 h 열 처리한 양극소재 분말의 XRD 결과이다. 그림 2의 전구체 XRD 결과와는 달리 그림 3의 양극소재 분말의 경우 공침 반응 온도에 따라 XRD 패턴에 유의한 차이가 관찰되지 않는다. 그림 3의 패턴은 다른 연구[9-17]에서 보고된 것 과 일치하는 것으로 층상구조인 R3m에 해당하는 LiNi1/3Co1/3Mn1/3O2로 동정된다. 그림 2의 전구체 상태에서 일부 피크가 약하게 관찰된 분말도 그림 3의 고온에서 Li과 합 성 열처리된 양극소재 분말의 XRD 패턴에서는 모두 잘 발달된 피크들을 보이고 있다. 그림 2에서 38° 부근에 여 분의 피크가 관찰된 전구체 분말도 그림 3에 보이듯이 최 종 양극소재 분말의 XRD 패턴에 어떠한 영향도 끼치지 않고 있다. 이는 불순한 상이 관찰되는 상용 전구체 분말 을 구입하여, 열처리하여 얻은 양극소재 분말에서도 동일 한 결과를 보고한 연구[16,17]와도 일치한다. 고온 열처리 과정에서 완전한 양극소재인 LiNi1/3Co1/3Mn1/3O2 결정이 형성된다고 볼 수 있다.
- 그림 3과 같은 XRD 패턴에서 (006)/(012)과 (018)/(110) 이중피크(doublet peak)가 뚜렷하게 분리될수록 재료의 결 정성이 우수하다고 평가되고 있다[18,19]. 그림 3에서 각 공침 반응 온도 조건의 양극소재 분말에서 두 조의 이중 피크가 잘 분리되어 있는 것으로 보아 불순물 상이 없는 우수한 분말이 합성된 것으로 볼 수 있다. 한편 그림 3의 XRD 데이터에 대하여 Rietveld 분석을 실시하여 얻은 격 자상수 a와 c, 그리고 c/a의 비율을 표 1에 나타내었다. 격 자상수의 비 c/a가 전구체 합성 온도에 상관없이 최종 양 극소재 분말 모두 다 4.9779 이상으로서 그 차이가 크지 않고, 다른 연구[19,20]에서 보고된 값과 유사하다. 일반적 으로 c/a 값이 4.9 이상이면 층상구조가 잘 형성된 것으로 간주되고 있다[19,20].
- 한편 그림 3에서 (003)과 (104) 피크 크기의 비율인 I003/I104 값을 각 전구체 합성 온도 별로 표 1에 나타내었다. I003/I104 값은 이른바 양이온 혼합(cation mixing) 정도와 연 관된다고 알려져 있다[6,7,19,21]. 양이온 혼합이란 Ni2+ 이 온의 크기(0.69Å)와 Li+ 이온의 크기(0.76Å)가 비슷하여 두 이온의 위치가 일부 바뀌는 현상을 말한다. 즉 전이금속 층 에 존재해야 할 Ni 원자 일부가 Li 원자 층에 들어와 있는 현상이다. I003/I104 값이 1.25일 때 양이온 혼합 양이 약 2% 이고, 1.5일 때 약 1%로 보고 있다[7]. 표 1에 의하면 각 조 건의 양극소재 분말의 I003/I104 값이 1.2680~1.4929 사이에 있어 양이온 혼합 양은 1~2%로 추정된다.
- 3.2. 분말의 형상과 입도
- 그림 4는 각 전구체 합성 온도 별로 일정 시간 간격(12, 24, 36, 48 h)으로 채취한 전구체 분말의 SEM 사진이고, 그림 5는 각 온도에서 48 h 동안 합성 후 채취한 전구체 분말의 고배율 SEM 사진이다. 반응 초기에 침상의 1차 입자가 서로 실타래처럼 얽혀 2차 입자가 형성된 것을 SEM 사진을 통해 볼 수 있으며, 같은 온도에서 공정 시 간이 경과됨에 따라 2차 입자의 크기가 증가하고 표면이 점점 더 매끄러워지는(smooth) 것을 알 수 있다. 그러나 같은 반응 시간에서 반응 온도 별로 2차 입자의 평균 크 기가 눈에 띄게 차이 나는 점은 발견할 수 없었다.
- 초기에 반응 탱크에 용액이 투입되면 공침반응이 일어 나 Ni1/3Co1/3Mn1/3(OH)2 또는 이와 유사한 금속수산화물의 핵이 생성된 후 시간이 지남에 따라 침상(needle) 혹은 편 상(flake)의 1차 입자가 형성된다. 이런 와중에 1차 입자들 끼리 응집(agglomeration)이 일어나고 교차된 침상 입자들 사이의 간극을 메우기 위한 재용해(dissolution)와 재결정 화(re-crystallization)가 일어나면서 구형의 2차 입자로 성 장하게 된다. 아울러 구형의 2차 입자의 표면에 있는 1차 입자들 사이의 간극에서도 재용해와 재결정이 일어나면서 구 표면이 더욱 매끄럽게 된다. 이때 재용해와 재결정화의 구동력은 1차 입자 표면의 곡률에 따른 용해도의 차이에 서 나온다. 고체 입자의 표면에서의 용해도는 Thomson- Freundlich 식으로 표시되는데 이를 근사식으로 나타내면 다음과 같다[22].
- 여기서 Cr은 곡률반경 r인 표면에서 용질 원자의 용해도 이고 C∞는 평면에서 원자의 평형 용해도이다. 또 σ는 고 체 입자와 용액 간의 계면에너지, M은 입자의 분자량, ρ 는 입자의 밀도, R은 기체상수, T는 절대온도이다. 이 식 에 의하면, 용액에 대한 용질 원자의 용해도는 고체 입자 표면의 곡률반경에 반비례한다. 즉, 침상 1차 입자의 모서 리 지역에서는 곡률 반경이 작기 때문에 금속 원자들이 용액으로 재용해되고, 1차 입자의 평평한 지역에서는 석 출이 일어나게 된다. 이로써 공침 반응 시간이 경과함에 따라 1차 입자 사이의 간극이 메워지고 2차 입자의 표면 이 매끄러워지는 것으로 해석할 수 있다.
- 어느 정도의 공침 반응 시간이 지나면 구형의 2차 입자들 은 입도분포를 가지고 있는 다분산계를 유지하게 된다. 이 후에는 입자의 크기에 따른 용해도의 차이에 의해서 작은 입자에서 큰 입자로 물질 이동이 난다. 큰 입자는 계속 커 지고, 작은 입자는 계속 작아져서 결국 소멸하게 된다. 이 현상을 일명 Ostwald Ripening이라고 한다. Lifshitz와 Slyozov[23], Wagner[24]는 오래 전에 이런 계에서의 입자 성장 속도론을 수학적으로 정리하였는데 이를 LSW 이론이 라고 부른다. 이 이론에 따르면, 만약 용액 내에서 용질 원 자들의 확산이 입자 성장 전체의 속도를 결정한다면, 시간 t 경과 후의 입자의 평균 반경 rt는 다음과 같이 표시된다.
- 여기서 r0는 정상상태(steady state)가 유지되기 시작하는 초기에 입자의 평균 반경이고, k는 속도상수(rate constant) 이다. 속도상수 k는 여러 가지 변수를 포함하고 있지만 [25], 온도에 관해서는 Arrhenius 식으로 의존관계를 표시 할 수 있다.
- 여기서 k0는 최대 성장속도, Q는 활성화에너지(activation energy)이다. 즉 반응 온도가 높을수록 속도상수가 커지고 따라서 시간이 경과함에 따라 평균 입자 크기가 증가하게 된다.
- 그림 4에 의하면 같은 공침 반응 온도에서 시간이 지날 수록 2차 입자의 크기가 증가하는 것은 확연하게 관찰할 수 있지만, 같은 공침 시간에서 온도에 따른 2차 입자 크 기의 차이는 확실하게 구분할 수 없다. 이는 CSTR에서 이 용하고 있는 교반의 효과라고 생각된다. 1차 입자는 성장 과정 중에 900 rpm으로 회전하는 교반기(impeller)에 의해 힘을 받아 깨지거나 깎이게 된다. 교반기는 또한 용액 내 의 용질원자의 분포를 계속 교란시켜 정상상태에서 멀어 지게 만든다. 또한 CSTR에서는 물질이 닫힌 계가 아니라 외부에서 새로운 반응물이 연속적으로 공급되고 있다.
- 그림 4에 의하면 공침 온도가 높아질수록 반응 초기에 1차 입자 덩어리가 큰 것을 볼 수 있는데, 이는 온도가 높 아짐에 따라 1차 입자끼리 뭉쳐지는 것과 뭉쳐진 1차 입 자가 2차 입자에 붙는 것이 용이해지기 때문이라고 판단 된다. 모든 온도 조건에서, 반응 시간이 경과함에 따라 점 점 1차 입자 사이가 메워지고 치밀하게 뭉쳐 매끄러운 2 차 입자를 이루는 것을 볼 수 있다. 그림 5에서 70°C와 80°C에서 48 h 동안 합성된 전구체 분말의 표면을 보면 다 른 온도에서의 전구체보다 1차 입자 덩어리의 크기가 불 균일한 것을 볼 수 있다.
- 그림 6은 각 공침 반응 온도에서 합성된 전구체 분말과 리튬을 포함하는 물질과 혼합하여 고온 열처리하여 제조 한 양극소재 분말의 SEM 사진으로 아래 열의 사진들은 위 열의 사진들을 확대한 것이다. 양극소재의 1차 입자들 의 크기가 30, 50, 60°C에 비해 70°C와 80°C에서 덜 균일 한 것을 볼 수 있다. 이는 열처리 과정에서 리튬이 전구체 로 확산되면서 앞에서 논의한 70°C와 80°C의 불균일한 크 기의 전구체 1차 입자의 형상이 그대로 유지되었기 때문 으로 보인다.
- 각 공침 반응 온도에서 48 h 동안 합성된 전구체 분말의 입도 분포를 입도분석기(Particle Size Analyzer)로 분석한 결과를 표 2에 나타내었다. 전구체의 반응 온도에 따른 전 구체 입도분포 변화의 경향성은 쉽게 파악되지 않는다. 각 공침 반응 온도의 전구체 분말과 그것들로부터 고온 열처 리를 통해 얻은 양극소재 분말의 탭 밀도를 측정한 결과 를 표 3에 나타내었다. 50°C에서 합성된 전구체와 양극소 재 분말이 가장 높은 탭 밀도를 보이고, 60°C 이상에서는 거의 일정한 탭 밀도를 유지함을 알 수 있다. 또한 표 3에 서 전구체와 양극소재의 탭 밀도를 비교하면, 열처리에 의 해 탭 밀도가 증가됨을 볼 수 있다. 30°C와 50°C에서 합 성한 전구체는 열처리 후 탭 밀도가 약 0.3 g/cc 증가한 반 면에 그 이상의 온도에서는 공침 반응 온도가 높아짐에 따라 탭 밀도의 증가 폭이 작아졌다. 이는 70°C와 80°C에 서 합성된 전구체로부터 얻은 양극소재 분말 표면의 1차 입자가 불균일한 형상으로 인해 분말의 유동 시 공간 충 전(filling)에 제한을 주기 때문이라고 판단된다.
- 3.3. 전기화학적 분석
- 그림 7은 3.0~4.3V vs Li/Li+의 범위에서 0.1 C-rate로 충· 방전하여 초기 충·방전 특성을 평가하여 얻은 그래프이 다. 그리고 표 4에 초기 충전용량과 초기 방전용량, 초기 충·방전 효율을 정리하였다. 전구체의 합성 온도와 최종 양극소재 분말의 용량 및 초기 충·방전 효율과의 상관관 계를 찾기가 쉽지 않아 보인다. 다만 표 4에서 60°C에서 합 성한 전구체로 만든 양극소재의 충·방전 효율 값이 가장 작은 것과 표 1에서 그 시료가 I003/I104 값이 가장 작은 것 과 연관성이 있어 보인다. 앞에서 I003/I104값이 낮을수록 양 이온 혼합(cation mixing) 현상이 많이 발생한다는 것을 언 급한 바 있다. 양극소재에서 양이온 혼합이 많이 일어나면 Ni 원자가 Li 원자 층에 혼입되어 있어 충·방전 시에 Li 이온의 이탈과 삽입을 방해하게 되어 용량과 효율을 저하 한다고 볼 수 있다. 한편, 70°C와 80°C에서의 I003/I104 값이 50°C에서의 값보다 높게 측정됐지만 초기 충·방전 효율 은 반대로 작게 측정됐다. 이것은 그림 4와 그림 5에서 관 찰되었던 전구체의 1차 입자의 불균일한 형상이 그림 6의 양극소재에서도 그대로 불균일하게 유지된 것으로 보아 70°C와 80°C에서 합성한 전구체로 제조한 양극소재에서 충·방전 시에 Li 이온의 확산이 균일한 1차 입자를 갖는 경우에 비하여 용이하지 않기 때문으로 해석된다.
- 0.1 C-rate로 충·방전하여 전극을 활성화한 후, 1.0 Crate로 30회 충·방전하여 수명 특성을 평가한 결과를 그 림 8과 표 5에 나타냈다. 표 5를 보면, 30 사이클 충·방전 후에 30, 50, 60°C에서 97% 이상의 용량이 유지된 반면에 70°C와 80°C에서는 94% 정도의 용량이 유지됐다. 충·방 전 횟수가 적기 때문에 양극과 전해액 사이의 부반응의 영 향이 크지 않을 것이라고 생각하면, 70°C와 80°C에서 합성 된 전구체를 이용해 제조된 양극소재는 반복적인 리튬 이 온의 삽입과 탈리에 대한 내구성이 낮은 것으로 판단된다. 이 또한 앞에서 언급한 불균일한 크기의 1차 입자 때문으 로 반복적인 리튬 이온의 출입 시 확산속도가 저하되고 양 극소재의 손상으로 이어졌을 것으로 판단할 수 있다. 양극 소재 분말의 비표면적과 전기화학적 특성과의 연관성에 대 한 추가적인 해석을 위하여 차후에 BET 측정 등을 통한 표면 분석에 관한 연구가 필요하다고 본다.
3. 결과 및 고찰
Fig. 2
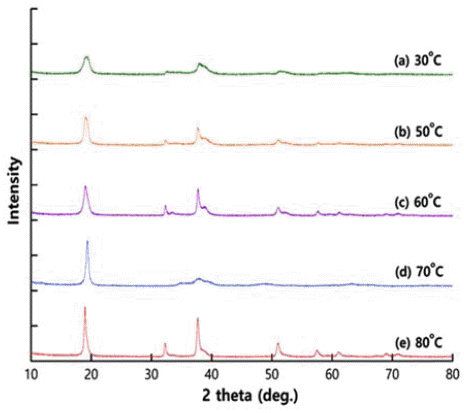
XRD patterns of precursor powders with different coprecipitation temperatures. (Intensity: arbitrary unit.)

Fig. 3
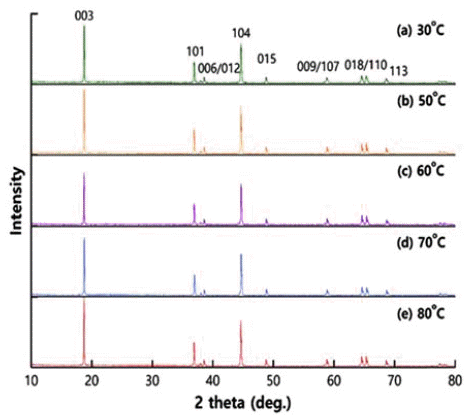
XRD patterns of positive electrode materials from precursors with different co-precipitation temperatures. (Intensity: arbitrary unit.)

Table 1
Calculated lattice parameters and I003/I104 values of positive electrode materials from the precursors prepared at different co-precipitation temperatures.
| Temperature (°C) | a (Å) | c (Å) | c/a | I003/I104 |
|---|---|---|---|---|
|
|
||||
| 30 | 2.8567 | 14.225 | 4.9795 | 1.4580 |
| 50 | 2.8548 | 14.211 | 4.9779 | 1.3162 |
| 60 | 2.8509 | 14.198 | 4.9802 | 1.2680 |
| 70 | 2.8524 | 14.205 | 4.9800 | 1.3867 |
| 80 | 2.8540 | 14.210 | 4.9790 | 1.4929 |
Fig. 4
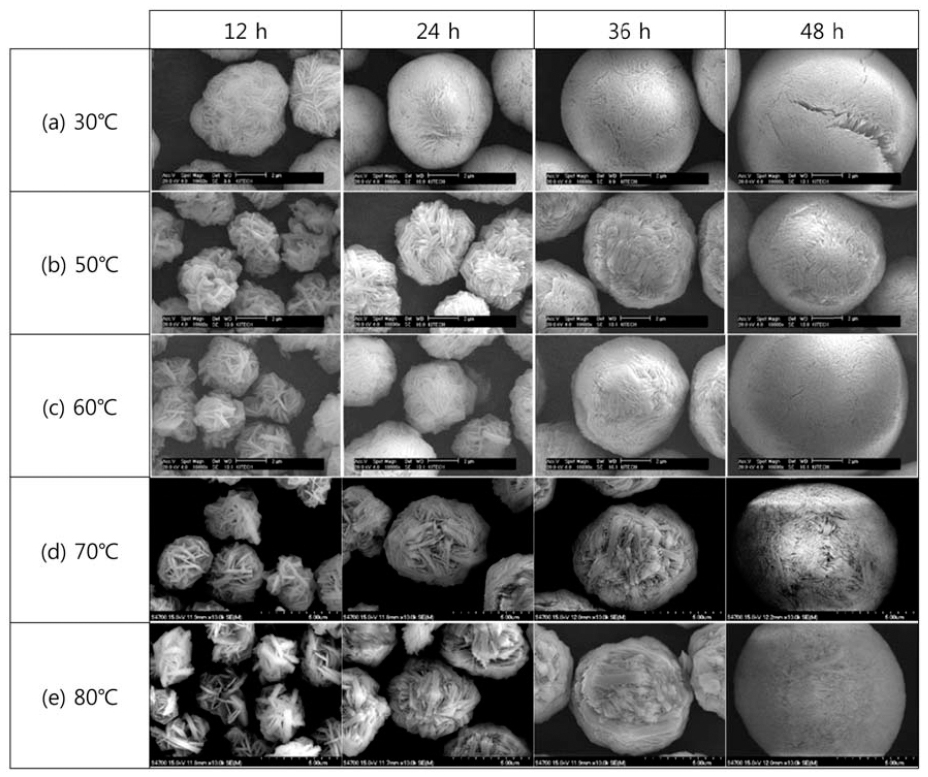
SEM images of the precursor powders prepared for various times at different co-precipitation temperatures.

Fig. 5

Magnified SEM images of the precursor particles prepared for 48 h at different co-precipitation temperatures.

Fig. 6

SEM images of positive electrode materials from precursors with different co-precipitation temperatures.

Table 2
Particle size analysis data of precursors with different co-precipitation temperatures.
Table 3
Tap density of precursor and positive electrode powders with different co-precipitation temperatures.
| Temperature (°C) | precursor powder (A) (g/cc) | positive electrode powder (B) (g/cc) | Difference (B-A) |
|---|---|---|---|
|
|
|||
| 30 | 1.47 | 1.77 | 0.30 |
| 50 | 1.94 | 2.23 | 0.29 |
| 60 | 1.78 | 2.02 | 0.24 |
| 70 | 1.81 | 2.00 | 0.19 |
| 80 | 1.78 | 1.82 | 0.16 |
Fig. 7
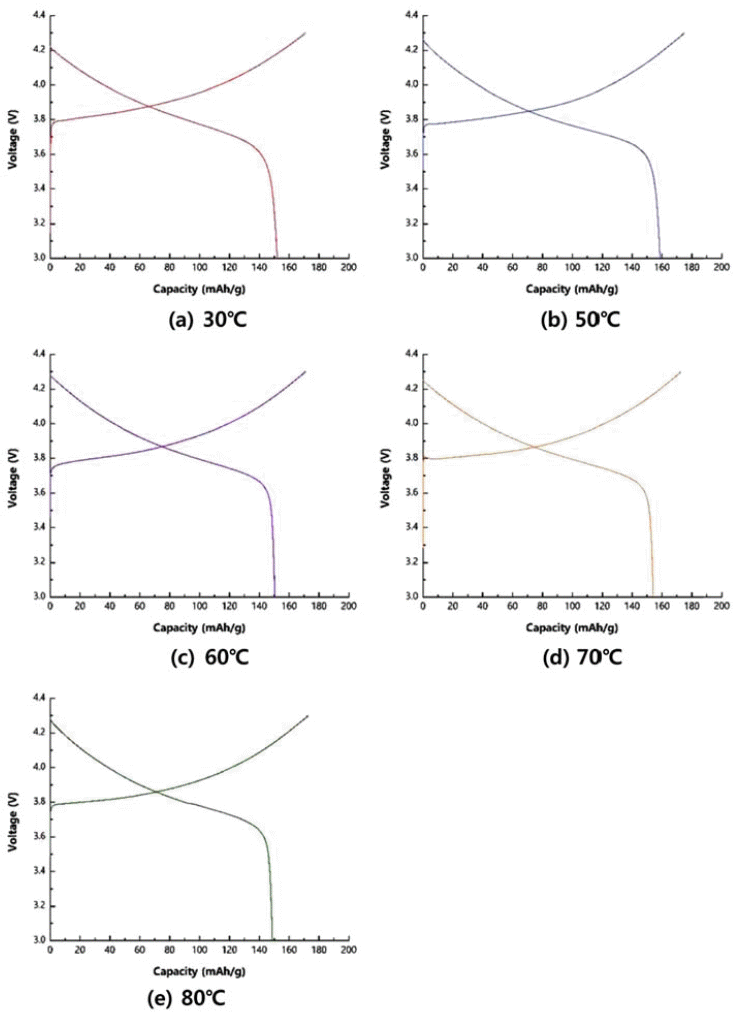
Initial charge/discharge curves of positive electrode materials from precursors with different co-precipitation temperatures.

Table 4
Initial charge/discharge capacity and efficiency of positive electrode materials from precursors with different co-precipitation temperatures.
Fig. 8

Cycling performance of positive electrode materials from precursors with different co-precipitation temperatures.

Table 5
Capacity retention (%) vs number of cycles for positive electrode materials from precursors with different co-precipitation temperatures.
- 리튬이온전지의 양극소재 LiNi1/3Co1/3Mn1/3O2의 전구체 인 Ni1/3Co1/3Mn1/3(OH)2 분말을 반응 온도를 30~80°C 범 위에서 달리하여 공침 방법으로 합성하고 각 조건의 전구 체와 양극소재의 특성을 분석하여 다음과 같은 결론을 얻 었다. 저온에서 합성되는 전구체 분말은 결정화가 완전하 게 이루어지지 않아 XRD 상의 피크가 희미하게 관찰되는 경우가 있지만, 전구체에 1,000°C의 고온에서 Li을 확산시 킨 양극소재는 완전한 층상구조를 갖고 있고 공침 온도에 따라 XRD 패턴에 유의한 차이가 관찰되지 않았다. 전구 체는 침상 또는 편상의 1차 입자가 뭉쳐서 구상의 2차 입 자로 형성되어 있으며, 공침 온도가 높을수록 1차 입자의 형상이 불균일하고 복잡한 배치로 뭉쳐 2차 입자를 이루 고 있었다. 전구체의 1차 입자의 형상과 배치는 최종 양극 소재까지 유지되었다. 이로 인해 높은 결정성을 가진 양극 소재가 합성되어도 충·방전 시에 Li 이온의 확산에 어려 움이 생겨 낮은 전기화학적 성능을 보였다. 실제로 70°C 와 80°C에서 합성한 전구체로 제조된 양극소재의 초기 용 량, 초기 충·방전 효율, 30 사이클 이후 용량 유지율이 50°C에서 합성한 전구체의 경우보다 낮았다. 50°C에서 합 성한 전구체와 그로부터의 양극소재의 탭 밀도가 가장 높 았다. 공침 온도가 높을수록, 전구체와 양극소재의 탭 밀 도의 차이가 작았으며, 양극소재의 탭 밀도가 낮았다. 이 는 복잡하게 뭉친 1차 입자로 인해 분말의 유동 시 충전 (filling)이 잘 일어나지 않기 때문으로 사료된다. 결론적으 로 실험한 조건 중에서 50°C가 Ni1/3Co1/3Mn1/3(OH)2 분말 의 최적 공침 온도라고 판단된다.
4. 결 론
- 1. D.-C. Li, T. Muta, L.-Q. Zhang, M. Yoshio and H. Noguchi: J. Power Sources, 132 (2004) 150. .Article
- 2. D. Li, Y. Sasaki, M. Kageyama, K. Kobayakawa and Y. Sato: J. Power Sources, 148 (2005) 85. .Article
- 3. S. H. Park, C. S. Yoon, S. G. Kang, H.-S. Kim, S.-I. Moon and Y.-K. Sun: Electrochim. Acta, 49 (2004) 557. .Article
- 4. C. J. Han, J. H. Yoon, W. I. Cho and Ho Jang: J. Power Sources, 136 (2004) 132. .Article
- 5. S. Patoux and M. M. Doeff: Electrochem. Comm., 6 (2004) 767. .Article
- 6. S. Jouanneau, K. W. Eberman, L. J. Krause and J. R. Dahn: J. Electrochem. Soc., 150 (2003) A1637. .Article
- 7. S.-H. Park, S.-H. Kang, I. Belharouak, Y.-K. Sun and K. Amine: J. Power Sources, 177 (2008) 177. .Article
- 8. D. Wang, I. Belharouak, G. M. Koenig, Jr., G. Zhou and K. Amine: J. Mater. Chem., 21 (2011) 9290. .Article
- 9. M.-H. Lee, Y.-J. Kang, S.-T. Myung and Y.-K. Sun: Electrochim. Acta, 50 (2004) 939. .Article
- 10. A. van Bommel and J. R. Dahn: J. Electrochem. Soc., 156 (2009) A362. .Article
- 11. A. van Bommel and J. R. Dahn: Chem. Mater., 21 (2009) 1500. .Article
- 12. Y. Yang, S. Xu, M, Xie, Y. He, G. Huang and Y. Yang: J. Alloys and Compounds, 619 (2015) 846. .Article
- 13. D. Kang, N. Arailym, J. E. Chae and S.-S. Kim: J. Korean Electrochem. Soc., 16 (2013) 191. .Article
- 14. W. Choi, S.-R. Park and C. H. Kang: J. Korean Powder Metall. Inst., 23 (2016) 136 (Korean). .Article
- 15. D.-L. Vu and J.-W. Lee: Korean J. Chem. Eng., 33 (2016) 514. .Article
- 16. K. Wu, F. Wang, L. Gao, M.-R. Li, L. Xiao, L. Zhao, S. Hu, X, Wang, Z. Xu and Q. Wu: Electrochim. Acta, 75 (2012) 393. .Article
- 17. Z. Xu, L. Xiao, F. Wang, K. Wu, L. Zhao, M.-R. Li, H.-L. Zhang, Q. Wu and J. Wang: J. Power Sources, 248 (2014) 180. .Article
- 18. A. Rougier, P. Gravereau and C. Delmas: J. Electrochem. Soc., 143 (1996) 1168. .Article
- 19. S. W. Oh, S. H. Park, C.-W. Park and Y.-K. Sun: Solid State Ionics, 171 (2004) 167. .Article
- 20. D. D. MacNeil, Z. Lu and J. R. Dahn: J. Electrochem. Soc., 149 (2002) A1332. .Article
- 21. T. Ohzuku, A. Ueda and M. Nagayama: J. Electrochem. Soc., 140 (1993) 1862. .Article
- 22. R. W. Balluffi, S. M. Allen and W. C. Carter: Kinetics of Materials, Wiley-Interscience, Hoboken, New Jersey (2005) 365. .Article
- 23. I. M. Lifshitz and V. V. Slyozov: J. Phys. Chem. Solids, 19 (1961) 35. .Article
- 24. C. Wagner: Z. Elektrochem., 65 (1961) 581. .Article
- 25. C. H. Kang and D. N. Yoon: Metall. Trans. A, 12 (1981) 65..Article
Figure & Data
References
Citations
Citations to this article as recorded by 

- A kinetic descriptor to optimize Co-precipitation of Nickel-rich cathode precursors for Lithium-ion batteries
Seon Hwa Lee, Ki Young Kwon, Byeong Kil Choi, Hyun Deog Yoo
Journal of Electroanalytical Chemistry.2022; 924: 116828. CrossRef
Effects of Precursor Co-Precipitation Temperature on the Properties of LiNi1/3Co1/3Mn1/3O2 Powders
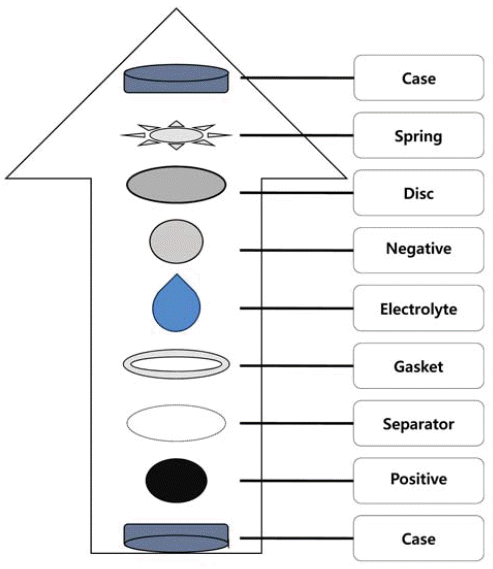
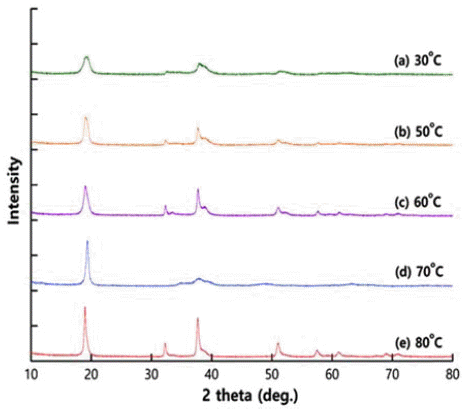
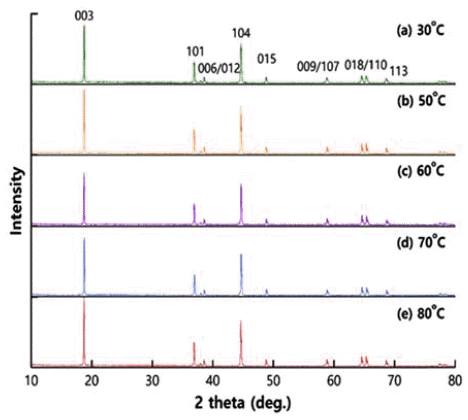
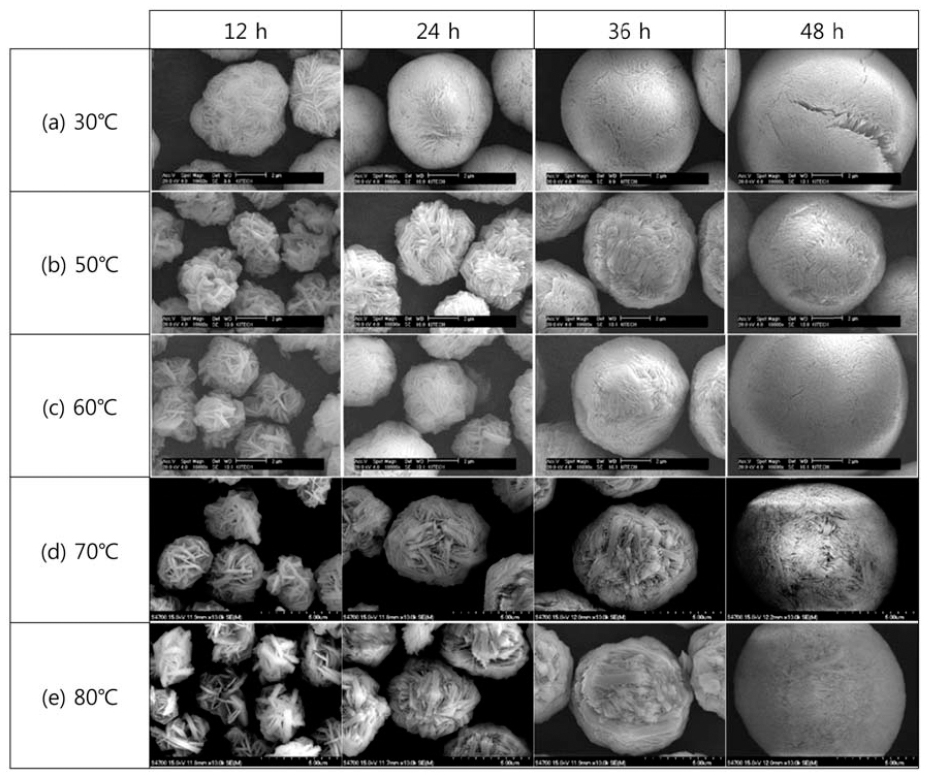


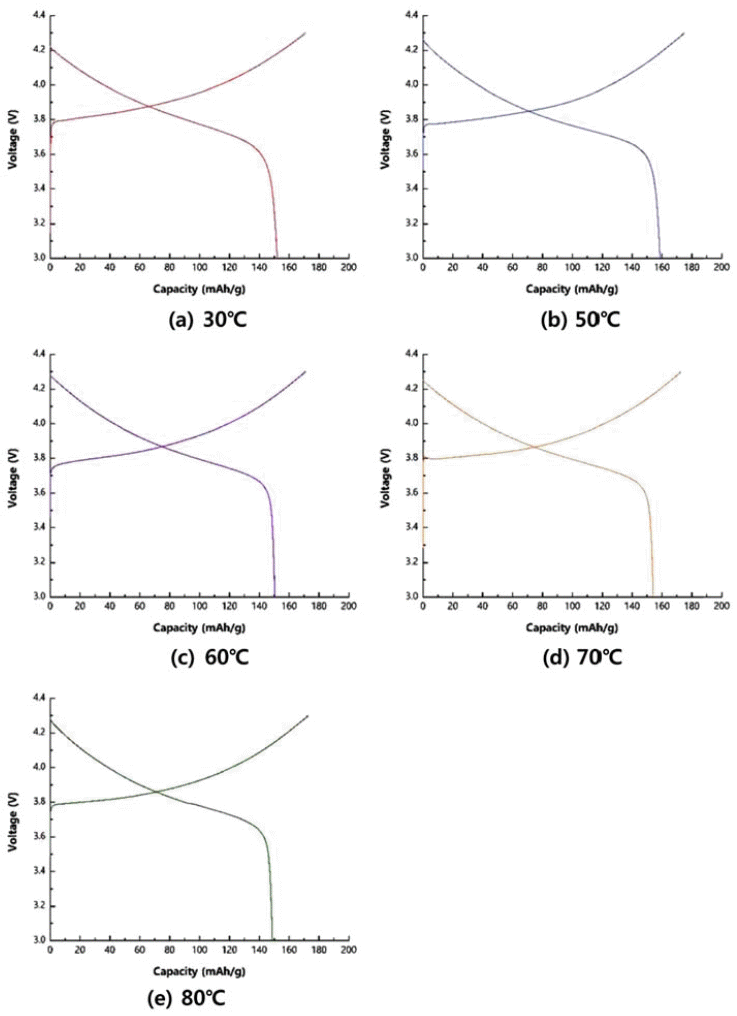
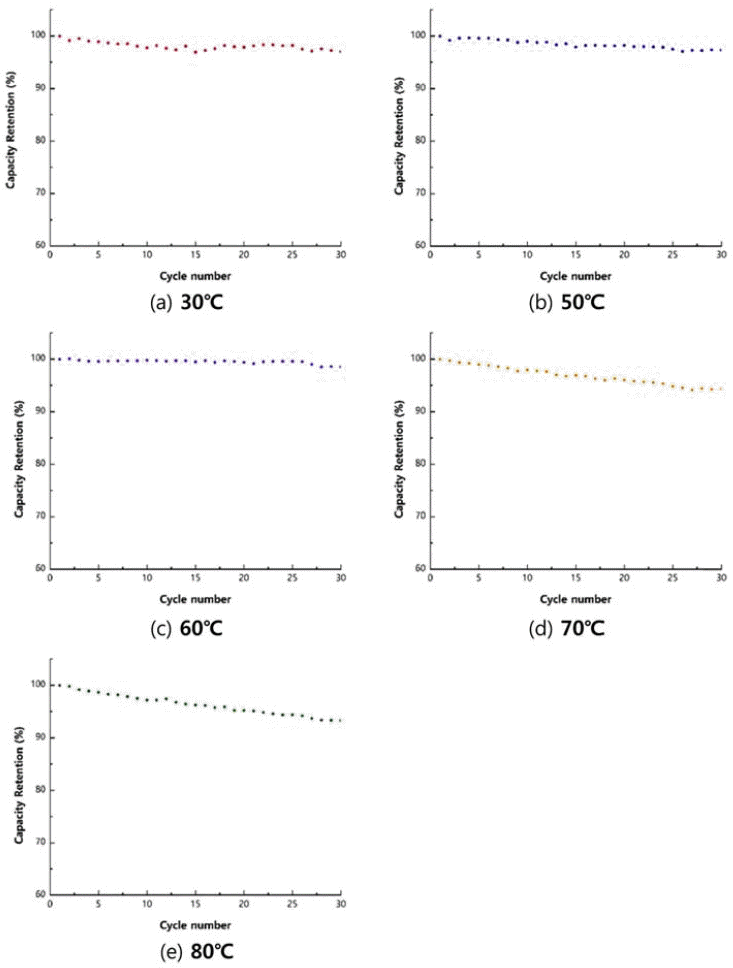
Fig. 1
Configuration and assembly sequence of coin cell.
Fig. 2
XRD patterns of precursor powders with different coprecipitation temperatures. (Intensity: arbitrary unit.)
Fig. 3
XRD patterns of positive electrode materials from precursors with different co-precipitation temperatures. (Intensity: arbitrary unit.)
Fig. 4
SEM images of the precursor powders prepared for various times at different co-precipitation temperatures.
Fig. 5
Magnified SEM images of the precursor particles prepared for 48 h at different co-precipitation temperatures.
Fig. 6
SEM images of positive electrode materials from precursors with different co-precipitation temperatures.
Fig. 7
Initial charge/discharge curves of positive electrode materials from precursors with different co-precipitation temperatures.
Fig. 8
Cycling performance of positive electrode materials from precursors with different co-precipitation temperatures.
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
Fig. 7
Fig. 8
Effects of Precursor Co-Precipitation Temperature on the Properties of LiNi1/3Co1/3Mn1/3O2 Powders
| Temperature (°C) | a (Å) | c (Å) | c/a | I003/I104 |
|---|---|---|---|---|
|
|
||||
| 30 | 2.8567 | 14.225 | 4.9795 | 1.4580 |
| 50 | 2.8548 | 14.211 | 4.9779 | 1.3162 |
| 60 | 2.8509 | 14.198 | 4.9802 | 1.2680 |
| 70 | 2.8524 | 14.205 | 4.9800 | 1.3867 |
| 80 | 2.8540 | 14.210 | 4.9790 | 1.4929 |
| 30°C | 50°C | 60°C | 70°C | 80°C | |||||
|---|---|---|---|---|---|---|---|---|---|
|
|
|||||||||
| D10 | 11.30 µm | D10 | 9.23 µm | D10 | 11.18 µm | D10 | 9.36 µm | D10 | 7.42 µm |
| D50 | 12.38 µm | D50 | 11.22 µm | D50 | 12.28 µm | D50 | 10.53 µm | D50 | 10.67 µm |
| D90 | 14.12 µm | D90 | 14.59 µm | D90 | 13.96 µm | D90 | 12.42 µm | D90 | 14.12 µm |
| Temperature (°C) | precursor powder (A) (g/cc) | positive electrode powder (B) (g/cc) | Difference (B-A) |
|---|---|---|---|
|
|
|||
| 30 | 1.47 | 1.77 | 0.30 |
| 50 | 1.94 | 2.23 | 0.29 |
| 60 | 1.78 | 2.02 | 0.24 |
| 70 | 1.81 | 2.00 | 0.19 |
| 80 | 1.78 | 1.82 | 0.16 |
| Temperature (°C) | Charge capacity (A) (mAh/g) | Discharge capacity (B) (mAh/g) | Efficiency (B/A) (%) |
|---|---|---|---|
|
|
|||
| 30 | 179.54 | 159.03 | 88.6 |
| 50 | 175.04 | 158.65 | 90.6 |
| 60 | 170.98 | 150.44 | 88.0 |
| 70 | 172.85 | 154.22 | 89.2 |
| 80 | 172.94 | 148.80 | 86.0 |
| No. of cycles | 30°C | 50°C | 60°C | 70°C | 80°C |
|---|---|---|---|---|---|
|
|
|||||
| 1 | 100 | 100 | 100 | 100 | 100 |
| 5 | 99.0 | 99.6 | 99.6 | 99.0 | 98.7 |
| 10 | 98.0 | 99.1 | 99.9 | 98.0 | 97.2 |
| 15 | 97.2 | 98.1 | 99.6 | 96.9 | 96.2 |
| 20 | 98.1 | 98.4 | 99.5 | 96.0 | 95.2 |
| 25 | 98.4 | 97.7 | 99.7 | 94.8 | 94.4 |
| 30 | 97.4 | 97.6 | 98.7 | 94.3 | 93.3 |
Table 1
Calculated lattice parameters and I003/I104 values of positive electrode materials from the precursors prepared at different
co-precipitation temperatures.
Table 2
Particle size analysis data of precursors with different co-precipitation temperatures.
Table 3
Tap density of precursor and positive electrode powders with different co-precipitation temperatures.
Table 4
Initial charge/discharge capacity and efficiency of positive electrode materials from precursors with different co-precipitation temperatures.
Table 5
Capacity retention (%) vs number of cycles for positive electrode materials from precursors with different co-precipitation temperatures.
Table 1
Table 2
Table 3
Table 4
Table 5
TOP
 KPMI
KPMI

 Cite this Article
Cite this Article