Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 23(4); 2016 > Article
-
Article
마이크로 주입장치를 이용한 용매치환결정화에 의한 중공상 수산화니켈 분말의 제조 - 김세기*, 박경수a, 정광일a
- Preparation of Ni(OH)2 Hollow Spheres by Solvent Displacement Crystallization Using Micro-Injection Device
- Seiki Kim*, Kyungsoo Parka, Kwang-Il Junga
-
Journal of Korean Powder Metallurgy Institute 2016;23(4):311-316.
DOI: https://doi.org/10.4150/KPMI.2016.23.4.311
Published online: July 31, 2016
한국세라믹기술원 이천분원 엔지니어링세라믹팀
㈜비츠로셀 연구소
Engineering Ceramic Center, Korea Institute of Ceramic Engineering and Technology, Icheon, Gyeonggi-do 17303, Korea
a VITZRO CELL Co. Ltd., Chusa-ro 235-35 Sinam-myun, Yesan-gun, Chungcheongnam-do 32417, Korea
- * Corresponding Author: Seiki Kim, TEL: +82-31-645-1469, FAX: +82-31-645-1492, E-mail: kimseiki@kicet.re.kr
© The Korean Powder Metallurgy Institute. All rights reserved.
- 1,317 Views
- 9 Download
- 1 Crossref
Abstract
- Ni(OH)2 hollow spheres have been prepared by solvent displacement crystallization using a micro-injection device, and the effect of process parameters such as concentration and the relative ratio of the injection speed of the precursor solution, which is an aqueous solution of NiSO4·6H2O, to isopropyl alcohol of displacement solvent have been investigated. The crystal phases after NaOH treatment are in the β-phase for all process parameters. A higher concentration of NiSO4·6H2O aqueous solution is injected by a micro-injection device and bigger Ni(OH)2 hollow spheres with a narrower particle size distribution are formed. The crystallinity and hardness of the as-obtained powder are so poor that hydrothermal treatment of the as-obtained Ni(OH)2 at 120°C for 24 h in distilled water is performed in order to greatly improve the crystallinity. It is thought that a relative ratio of the injection speed of NiSO4·6H2O to that of isopropyl alcohol of at least more than 1 is preferable to synthesize Ni(OH)2 hollow spheres. It is confirmed that this solution- based process is very effective in synthesizing ceramic hollow spheres by simple adjustment of the process parameters such as the concentration and the injection speed.
- 용매치환결정화(Solvent displacement crystallization) 는 구리의 정련과정에서 불순물인 니켈의 회수 공정으로 사 용되는 증발결정화(evaporative crystallization) 공정에 대 한 에너지 절감형 공정 대안으로 제안된 방법[1]으로서, 물과 혼합되는 낮은 비등점을 가진 유기용매를 회수 목적 인 무기질 이온을 함유하는 수용액에 첨가하면 극성 유기 용매와 무기질 이온 간의 친화성 경합이 일어나고 유사한 수소결합을 나타내는 극성 유기용매의 물에 대한 친화성 으로 인하여 물에 대한 무기질 이온의 용해도 저하를 초 래하는 현상[2,3]에 근거한 방법이다. 이러한 용매치환결 정화법은 증발결정화에 소요되는 막대한 에너지를 절감할 수 있으며, 액상 공정을 통하여 무기 물질의 고순도화를 동시에 구현할 수 있어서 화학 및 제약 공정에 널리 채택 되고 있는 공정이다[4,5].
- 중공(hollow sphere)상 세라믹 입자는 그 특이한 형상으 로 인한 높은 비표면적, 낮은 밀도 등의 기능 발현으로 인 하여 나노 또는 마이크로 스케일의 입자의 경우, 촉매 담 체[6-7], 경량소재[8-9] 및 단열재[10], 흡착제[11-12] 및 약 물전달제어용 캡슐 용기[13-14] 등의 폭 넓은 분야에 활용 되고 있다. 이러한 중공(hollow sphere)상 세라믹 입자는 전통적으로 폴리스틸렌이나 라텍스 단분산 입자 등을 템 플레이트로 활용하는 방법[15-16], 분무열분해법[17-18] 등이 사용되어 왔으나, 제조 단가가 높거나 수율이 낮다는 단점이 있다[19].
- 수산화니켈(Ni(OH)2)은 Ni/Zn, Ni/MH 같은 이차전지의 양극 소재로 널리 활용[20-23]되고 있으며, 전지의 에너지 밀도의 향상을 위하여 충진성이 좋은 구상(spherical) 의 분 말 형상을 사용하여 에너지밀도 향상을 구현하고 있다[24]. 그러나 전지의 중량 에너지밀도의 관점에서 볼 때, 전지의 경량화도 중요한 요소이다.
- 본 연구에서는 수산화니켈(Ni(OH)2) 전극 활물질 소재 의 구상화와 아울러 중공화에 의한 경량화를 목적으로 마 이크로 주입 장치를 통하여 원료용액인 황산니켈6수화물 (NiSO4·6H2O)을 주입하여 용매치환결정화에 있어서 원료 용액의 농도 및 원료용액과 치환용매의 주입 속도 비 등의 공정 인자 변화에 따른 중공상 의한 수산화니켈(Ni(OH)2) 분말의 결정상, 미세구조 및 분말 밀도와 비표면적 등을 분석하고 합성 공정 조건을 제시하고자 한다.
1. 서 론
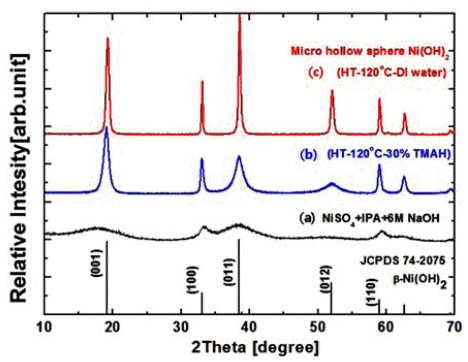
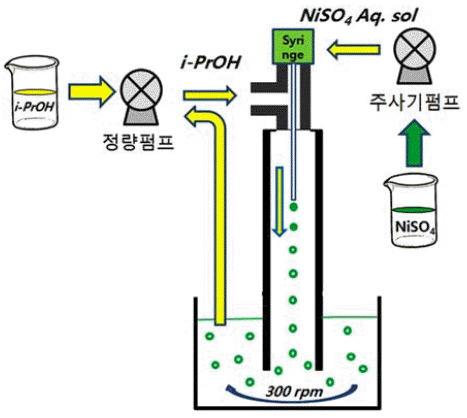
- 본 연구에서는 용매치환결정화에 의한 마이크로 스케일 의 중공(hollow sphere) 상의 수산화니켈(Ni(OH)2) 분말을 제조하기 위한 출발 원료로써 순도 98%의 황산니켈6수화 물(NiSO4·6H2O, Daejung Chemicals & Metals Co., Ltd., Korea) 과 치환용매로써 순도 99.5%의 이소프로필알콜(i- C3H7OH, Daejung Chemicals & Metals Co., Ltd., Korea), 제조된 중공상의 황산니켈을 수산화니켈로 처리하기 위하 여 순도 98%의 수산화나트륨(NaOH, Daejung Chemicals & Metals Co., Ltd., Korea)을 사용하였다. 또한 본 연구에 서 사용한 마이크로 주입 장치는 자체 제작한 것으로서 황산니켈6수화물을 증류수에 1~3M 농도로 용해시켜서 내 경 292 μm, 길이 90 mm의 SUS 제의 주사기 바늘을 가진 60 mL 용량의 정밀 주사기 펌프(TJ-3A, Longer Precision Pump Co., Ltd., China) 에 장착하고, 그림 1에 나타낸 바와 같이 정밀 정량펌프(PP-600DW, PoongLim Co., Ltd., Korea) 를 이용하여 치환 용매인 이소프로필알콜이 100~240 mL/ min의 흐름속도로 폐회로로 순환하고 있는 마이크로 주입 장치를 통하여 0.25~1mL/min의 주입 속도로 NiSO4·6H2O 수용액을 주입하였다. NiSO4·6H2O 수용액과 이소프로필 알콜(IPA)이 최초 혼합되어 용매치환결정화가 일어나는 부위는 내경 3 mm의 유리튜브로 구성하였다.
- 이와 같은 용매치환에 의해 중공상으로 결정화된 황산 니켈을 함유한 이소프로필알콜 용액을 여과하여 얻은 황 산니켈 결정을 250 rpm의 속도로 교반하는 6 M 농도의 수 산화나트륨 수용액에 투입하여 여과, 증류수 세정 및 80°C에서 16시간 건조를 통하여 중공(hollow sphere) 상의 수산화니켈(Ni(OH)2) 분말을 제조하였다. 또한 이렇게 하 여 제조한 수산화니켈 분말의 일부는 결정성 및 경도 향 상을 위하여 테플론 내장 내압 용기 내에서 증류수 및 30% TMAH(N(CH3)4OH, Tetramethylammonium Hydroxide, Alfa Aesar, USA)를 용매로 120°C에서 24시간 동안 수열처리를 행하였다.
- 제조 분말 시료의 결정상 분석은 X-선회절분석기(X-ray diffractometer, D/MAX-2500/PCP, Rigaku, Japan), 미세구 조는 주사전자현미경(Scanning Electron Microscope, JSM- 6390, JEOL, Japan), 분말의 진밀도는 헬륨(He) 가스를 사 용하여 피크노미터(Accupyc 1330, Micromeritics, USA), 분 말의 충진 겉보기 밀도는 탭(Tap) 밀도 측정기(TAP-2S, Logan Instruments, USA)를 이용하였고, 비표면적은 BET 비표면적 측정기(Micromeritics, Tristar II, USA)를 이용하 여 측정하였다.
2. 실험 방법
- 3.1. 중공(hollow sphere) 상 분말의 형성 기구
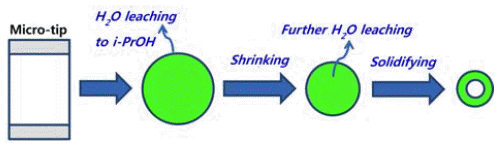
- 그림 2에 황산니켈과 같은 금속염의 수용액으로부터 중공 상 분말의 형성 과정을 나타내었다. 마이크로 주입 장치를 통하여 이소프로필알콜에 주입된 황산니켈 수용액 액적으로 부터 물 성분이 이소프로필알콜로 용출되어 액적은 수축이 일어나며, 물의 확산이 계속 진행됨에 따라서 NiSO4·6H2O (용해도 65 g/100 g H2O)의 이소프로필알콜에 대한 낮은 용 해도(0.12 g/100 g i- C3H7OH)로 인하여 결정화가 일어나 고 최종적으로 마지막 단계에서는 결정화가 일어나며 구 상으로 형성된 NiSO4·6H2O의 내부에서 물의 용출로 중공 상의 형상이 형성된다. 이 때 주입하는 원료 용액의 농도 와 원료용액/치환용매(이소프로필알콜)의 상대적인 주입 속도 비율에 따라서 형성되는 중공상 입자의 크기를 제어 할 수 있다.
- 3.2. 중공(hollow sphere) 상 수산화니켈(Ni(OH)2) 분말 의 결정상
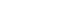
- 용매치환결정화에 의하여 상온에서 제조한 중공상 (hollow)의 구상 Ni(OH)2 분말의 결정상 분석 결과를 그림 3에 나타내었다. 1.0 M 농도의 NiSO4·6H2O 원료 용액과 이소프로필알콜의 주입속도는 각각 1 mL/min와 240 mL/ min의 속도로 마이크로 주입(IPA /Ni염 주입속도 비 ~0.97) 하였다. 그림 3(a)에 나타낸 바와 같이 합성 후의 Ni(OH)2 분말은 β 상의 Ni(OH)2가 생성되었음을 알 수 있으나, 결 정성은 매우 낮은 것으로 판명되었다. 많은 선진 연구자들 이 수산화니켈의 이차전지 양극소재로서의 가장 중요한 물성인 충방전 특성 향상과 결정성 및 결정립 크기의 반 비례 관계에 대하여 보고하였다[23,25,26]. 따라서 본 연 구에서도 결정성 및 결정립 크기의 제어를 위하여 후속 공정으로서 증류수 또는 TMAH(Tetra Methyl Ammonium Hydroxide)를 용매로 120°C의 온도에서 24 시간 수열처리 를 행한 결과, 그림 3(b), (c)에 나타낸 바와 같이 β 상의 결정성이 크게 향상됨을 확인할 수 있다. 특히 그림 3(b) 의 TMAH(Tetra Methyl Ammonium Hydroxide)를 용매로 수열합성을 행한 경우가 증류수를 용매로 한 경우에 비하 여 약한 피크 강도를 나타내는데, 이는 TMAH의 수열합 성 중에 유리된 암모늄 이온에 의하여 수산화니켈 분말이 일부 용해된 것에 기인하는 것으로 사료된다.
- 3.3. 합성 공정 인자에 따른 중공상 수산화니켈(Ni(OH)2) 분말의 미세 구조 변화
- NiSO4·6H2O 원료 용액의 농도에 따른 미세구조를 관찰 한 결과를 그림 4에 나타내었다. IPA 대 Ni염의 주입속도 비는 ~1.0 이며, 본 연구에서 채택한 NiSO4·6H2O 수용액 의 1.0~3.0 M 농도 영역에서는 모두 구상의 Ni(OH)2이 생 성된 것을 확인할 수 있으며, 1 M 농도의 NiSO4·6H2O 원 료 용액으로 제조된 수산화니켈은 2~30 μm, 2 M 농도의 경우 3~40 μm, 3 M 농도의 경우 5~50 μm로 농도가 높아 질수록 생성된 Ni(OH)2의 입자 크기와 입도분포가 커지는 것을 알 수 있다. 또한 그림 4(a)에 나타낸 바와 같이, 1 M 농도의 NiSO4·6H2O 원료 용액으로 제조된 Ni(OH)2 의 내 부 코어(core)에 형성된 중공(hollow sphere) 의 직경은 약 14~15 μm, 쉘(shell) 의 두께는 약 10 μm 정도 임을 알 수 있는데, 이러한 쉘(shell)의 두께는 투입하는 NiSO4·6H2O 원료 용액 속의 용매인 물이 용출되어 용해도 차이에 의 하여 분말이 생성되는 원리를 고려하면 원료용액의 농도 에 비례할 것으로 사료되며, 또한 원료용액의 농도가 높을 수록 용매치환에 따른 입자 석출 속도가 빠를 것이므로 입도분포가 평균화되지 않고 크게 나타나며 비 구상의 입 자 생성률이 높아지는 것으로 사료된다.
- 그림 5에 이소프로필알콜의 투입속도를 240 mL/min으로 고정하고 NiSO4·6H2O 원료 용액의 주입속도는 0.25~1 mL/ min(IPA/Ni염 주입속도 비 1.0~3.9)로 변화시킨 경우의 미세 구조를 관찰한 결과를 나타내었다. 본 제조 조건에서 모두 양호한 중공상의 입자가 생성됨을 확인할 수 있으며, 입자 크기와 입도분포가 본 주입속도 범위 내에서는 그다지 변 화되지 않음을 알 수 있다. 이는 이소프로필알콜의 주입 속도가 NiSO4·6H2O 원료 용액의 주입속도 보다 큰 영역 으로서 마이크로 주입된 NiSO4·6H2O 액적이 응집되지 않 고 적당히 분산되어 중공상으로 결정화될 수 있기 때문으 로 사료된다.
- 그림 6은 NiSO4·6H2O의 주입속도를 1 mL/min으로 고 정하고 이소프로필알콜의 주입속도를 100~240 mL/min으 로 변화시킨 즉, IPA/Ni염 주입속도 비가 0.4~1.0로서 1 보다 작은 조건에서 합성된 Ni(OH)2의 미세구조 관찰 결 과를 나타내었다. 모든 조건에서 중공상 분말이 합성되었 으나 IPA/Ni 염 주입속도 비가 낮을수록 생성된 분말의 응집 현상이 일어나는 것을 확인할 수 있다.
- 3.4. 합성 공정 인자에 따른 중공상 수산화니켈 (Ni(OH)2) 분말의 밀도
- 표 1에 합성 공정 인자에 따른 중공상 Ni(OH)2) 분말의 겉보기 밀도와 진밀도(피크노미터 밀도)를 정리하였다. 표 1에서 분말의 겉보기 밀도는 탭(Tap) 밀도 측정 결과를 진 밀도는 He 가스를 이용하여 피크노미터로 측정한 결과를 나타낸다. NiSO4·6H2O 원료 용액의 농도가 1~3 M로 높아 질수록 Ni(OH)2의 진밀도는 2.75 g/cm3에서 2.88 g/cm3로 높아진 반면, 겉보기(Tap) 밀도는 0.56 g/cm3에서 0.39 g/ cm3로 낮아졌다. 이는 농도가 높아질수록 생성된 입자의 크기와 입도분포가 증가하는 것에 기인하는 것으로 사료 된다. IPA/Ni염 주입속도 비가 1.0~3.9 영역에서는 생성 분말의 응집도 적고 입자 크기의 변화도 적은 이유로 겉 보기(Tap) 밀도의 변화가 0.63 g/cm3에서 0.56 g/cm3로 변화 폭이 적었다. 따라서 원료용액의 농도 및 마이크로 주입 속 도의 제어를 통하여 입자크기와 입도분포의 제어가 가능한 중공상 금속수산화물의 제어가 가능함을 알 수 있다. “2. 실험방법”에 또한 이러한 분말의 진밀도와 겉보기 밀도의 현격한 차이는 중공(hollow sphere) 이라는 특수한 구조에 기인하는 것으로서, 비표면적 측정 결과도 중공상의 형상 을 반영하였다. 즉, 전술한 제조공정에서 1 M-NiSO4를 1 mL/min의 속도로 투입하여 제조한 Ni(OH)2의 비표면적 은 201 m2/g, 이 분말을 이온교환수에서 120°C, 24시간 수 열처리한 결과 39 m2/g의 비표면적 값을 나타내었는데, 이 는 Ni(OH)2의 이론 밀도를 4.15 g/cm3로 계산한 반경 20 μm의 구상 분말의 비표면적이 0.1 m2/g 이하 임을 고려 하면 매우 높은 값으로서 이러한 중공상 분말의 높은 비표 면적을 이용한 다양한 용도로의 활용이 기대된다.
3. 결과 및 고찰
X-ray diffraction patterns of Ni(OH)2 hollow spheres (a) as-received, after hydrothermally-treated using (b) TMAH, and (c) distilled water as a solvent.
SEM image of Ni(OH)2 hollow spheres prepared from (a) 1M-NiSO4, (b) 2M-NiSO4 and (c) 3M-NiSO4 aquous solution.

SEM image of Ni(OH)2 hollow spheres with the injection speed ratio of NiSO4 aqua solution to isopropyl alcohol ; (a) 3.88, (b) 1.94, and (c) 0.97.

SEM image of Ni(OH)2 hollow spheres with the injection speed ratio of NiSO4 aqua solution to isopropyl alcohol ; (a) 0.41, (b) 0.61, and (c) 0.97.

Summary of preparation condition and the resultant powder density.
| No. | Composition | NiSO4 Input speed [mL/min] | IPA Input speed [mL/min] | Input speed ratio (IPA/Ni) | Apparent density [g/cm3]a | True density [g/cm3]b |
|---|---|---|---|---|---|---|
|
|
||||||
| N1-1 | 1 M NiSO | 0.56 | 2.75 | |||
| N1-2 | 2 M NiSO4 | 1 mL/min | 1 | 0.48 | 2.79 | |
| N1-3 | 3 M NiSO4 | 4 | 240 | 3.9 | 0.39 | 2.88 |
| N2-1 | 250 uL/min | 0.63 | 2.48 | |||
| N2-2 | 500 uL/min | 1.95 | 0.6 | 2.51 | ||
| N2-3 | 1 M NiSO4 | 1 mL/min | 1 | 0.56 | 2.75 | |
| N3-1 | 100 | 0.4 | - | - | ||
| N3-2 | 1 mL/min | 150 | 0.6 | - | - | |
| N3-3 | 240 | 1 | 0.56 | 2.75 | ||
- 본 연구에서는 중공(hollow sphere) 상의 수산화니켈 (Ni(OH)2) 분말을 이소프로필알콜을 치환용매로 NiSO4·6H2O 수용액을 마이크로 주입장치를 이용하여 용매치환결정화에 의하여 제조하였고, 출발원료 용액의 농도 및 원료용액/치 환용매(이소프로필알콜)의 합성 공정 인자를 변화시켜서 결과적인 합성 분말의 결정상, 미세구조 및 분말의 진밀도 와 겉보기밀도 변화를 고찰하였고 다음과 같은 결론을 도 출하였다.
NiSO4·6H2O의 주입 농도가 높을수록 합성입자의 크 기와 분포가 커지며, 치환용매인 이소프로필알콜의 주입 속도가 원료용액인 NiSO4·6H2O 수용액의 주입 속도 보다 클수록 응집이 적고 입자분포도 좁은 중공상의 입자를 얻 을 수 있다.
따라서 치환용매로써 이소프로필알콜의 주입속도가 원 료용액인 NiSO4·6H2O의 주입 속도 보다 빠른 조건에서 양 호한 중공상의 수산화니켈 (Ni(OH)2) 분말을 얻을 수 있다.
본 마이크로 주입 장치를 이용한 용매치환결정화 방 법으로 원료용액의 농도 및 마이크로 주입 속도의 제어를 통하여 입자 크기와 입도분포의 제어가 가능한 중공상 금 속수산화물의 제어가 가능함을 알 수 있다.
4. 결 론
-
Acknowledgements
- 본 연구는 산업통상자원부의 WC300사업의 연구비 지 원으로 수행되었으며 이에 감사드립니다.
감사의 글
- 1. J. M. Cohen: Separation Processes in Hydrometallurgy, G. A. Davis (Ed.), Ellis Horwood, London, (1987) 265. .
- 2. Z. B. alfassi: Separation Sci. and Technol., 14 (1979) 155. .Article
- 3. Z. B. alfassi and S. Mosser: AlChE Journal, 30 (1984) 874. .Article
- 4. T.G. Zijlema, H.Oosterhof, G. J. Witkamp and G. M. van Rosmalen: Separation and Purification by Crystallization, G.D. Botsaris and K. Tokoyura (Ed.), Washington, D.C.: ACS, (1997) 230. .Article
- 5. N. Sato, Y. Wei and M. Nanjo: Metallurgical Review of MMIJ, 15 (1998) 1. .
- 6. Sakamishi, H. Hasuo, M. Kishino, I. Mochida and O. Okuma: Energy Fuels, 10 (1996) 216. .Article
- 7. H. Huang and E. E. Remsen: J. Am. Chem. Soc., 121 (1999) 3805. .Article
- 8. M. Ohmori and E. Matijevic: J. Colloid Interface Sci., 150 (1992) 594. .Article
- 9. J.E.G.J. Wijhoven and W.L. Vos: Science, 281 (1998) 802. .ArticlePubMed
- 10. J.P.H. Ansermet and E. Baberiswyl: J. Mater. Sci., 29 (1994) 2841. .Article
- 11. D. Zhao: Science, 279 (1998) 548. .ArticlePubMed
- 12. A. Imhof and D.J. Pine: Nature, 389 (1997) 948. .Article
- 13. S. Kirsch, A. Doerk and E. Bartsch: Macromolecules, 32 (1999) 4508. .Article
- 14. H.K. Lee, J.H. Park and K.C. Kwon: J. Controlled Release, 44 (1997) 283. .Article
- 15. S.A. Jenekhe and X.L. Chen: Science, 279 (1998) 1903. .ArticlePubMed
- 16. B. T. Holland, C. F. Blanford and A. Stein: Science, 281 (1998) 538. .ArticlePubMed
- 17. V. Belov, I. Belov and L. Harel: J. Am. Ceram. Soc., 80 (1997) 982. .Article
- 18. T. Thorsen, R. W. Roberts, F. H. Arnold and S. R. Quake: Phys. Rev. Lett., 86 (2001) 4163. .ArticlePubMed
- 19. S. Che, O. Sakurai, K. Shinozaki and N. Mizutani: J. Aerosol Sci., 29 (1998) 271. .Article
- 20. G. Sakai, M. Miyazaki and T. Kijima: J. Electrochem. Soc., 157 (2010) A 480. .Article
- 21. D Linden: Handbook of Batteries, 3rd (Ed.), McGraw- Hill, New York (2002) 29.1. .
- 22. X. Han, X. Xie and C. Xu: Opt. Mater., 23 (2003) 465. .Article
- 23. K. Watanabe, T. Kikuoka and N. Kumagai: J. Appl. Electrochem., 25 (1995) 219. .Article
- 24. M. Oshitani, H. Yufu and K. Takashima: J. Electrochem. Soc., 136 (1989) 1590. .Article
- 25. A. Audemer, A. Delahaye, R. Farhi, N. Sac-Epée and J. M. Tarascon: J. Electrochem. Soc., 144 (1997) 2614. .Article
- 26. D. Louër, D. Weigel and J. I. Langford: J. Appl. Crystallogr., 5 (1972) 353..Article
Figure & Data
References
Citations

- The Effects of Hexamethylenetetramine Concentration on the Structural and Electrochemical Performances of Ni(OH)2 Powder for Pseudocapacitor Applications
Dong Yeon Kim, Young-Min Jeong, Seong-Ho Baek, Injoon Son
Journal of Korean Powder Metallurgy Institute.2019; 26(3): 231. CrossRef
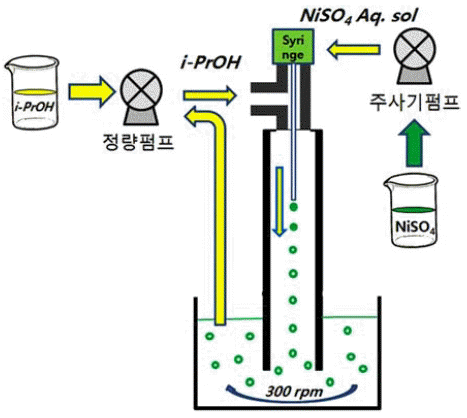
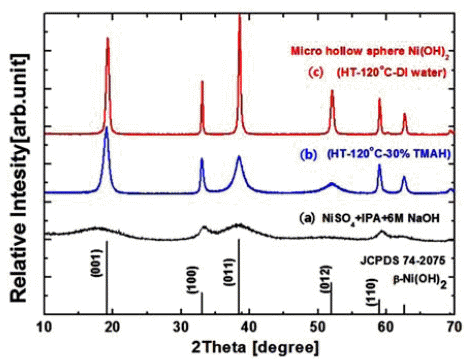



Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
| No. | Composition | NiSO4 Input speed [mL/min] | IPA Input speed [mL/min] | Input speed ratio (IPA/Ni) | Apparent density [g/cm3] |
True density [g/cm3] |
|---|---|---|---|---|---|---|
|
|
||||||
| N1-1 | 1 M NiSO | 0.56 | 2.75 | |||
| N1-2 | 2 M NiSO4 | 1 mL/min | 1 | 0.48 | 2.79 | |
| N1-3 | 3 M NiSO4 | 4 | 240 | 3.9 | 0.39 | 2.88 |
| N2-1 | 250 uL/min | 0.63 | 2.48 | |||
| N2-2 | 500 uL/min | 1.95 | 0.6 | 2.51 | ||
| N2-3 | 1 M NiSO4 | 1 mL/min | 1 | 0.56 | 2.75 | |
| N3-1 | 100 | 0.4 | - | - | ||
| N3-2 | 1 mL/min | 150 | 0.6 | - | - | |
| N3-3 | 240 | 1 | 0.56 | 2.75 | ||
※ a : 탭(Tap) 밀도 측정, b : He 가스 이용 피크노미터로 측정
Table 1
TOP
 KPMI
KPMI

 Cite this Article
Cite this Article