Articles
- Page Path
- HOME > J Korean Powder Metall Inst > Volume 21(2); 2014 > Article
-
ARTICLE
전기 방사법을 이용한 플레이크형 LiCoO2 나노 분말의 제조 - 구본율, 안건형, 안효진*
- Fabrication of Flake-like LiCoO2 Nanopowders using Electrospinning
- Bon-Ryul Koo, Geon-Hyoung An, Hyo-Jin Ahn*
-
Journal of Korean Powder Metallurgy Institute 2014;21(2):108-113.
DOI: https://doi.org/10.4150/KPMI.2014.21.2.108
Published online: March 31, 2014
서울과학기술대학교 신소재공학과
Department of Materials Science and Engineering, Seoul National University of Science and Technology, Seoul 139-743, Korea
- *Corresponding Author : Hyo-Jin Ahn, TEL: +82-2-970-6622, FAX: +82-2-973-6657, E-mail: hjahn@seoultech.ac.kr
• Received: February 12, 2014 • Revised: March 8, 2014 • Accepted: March 13, 2014
© Korean Powder Metallurgy Institute
- 903 Views
- 4 Download
- 2 Crossref
Abstract
- Flake-like LiCoO2 nanopowders were fabricated using electrospinning. To investigate their formation mechanism, field-emssion scanning electron microscopy, X-ray diffraction, and X-ray photoelectron spectroscopy were carried out. Among various parameters of electrospinning, we controlled the molar concentration of the precursor and the PVP polymer. When the molar concentration of lithium and cobalt was 0.45 M, the morphology of LiCoO2 nanopowders was irregular and round. For 1.27 M molar concentration, the LiCoO2 nanopowders formed with flake-like morphology. For the PVP polymer, the molar concentration was set to 0.011 mM, 0.026 mM, and 0.043 mM. Irregular LiCoO2 nanopowders were formed at low concentration (0.011 mM), while flake-like LiCoO2 were formed at high concentration (0.026 mM and 0.043 mM). Thus, optimized molar concentration of the precursor and the PVP polymer may be related to the successful formation of flake-like LiCoO2 nanopowders. As a results, the synthesized LiCoO2 nanopowder can be used as the electrode material of Li-ion batteries.
- 최근 휴대용 전자기기(예를 들면, 노트북, 휴대폰, 디지 털카메라, PDA) 등이 점점 더 발전함에 따라 리튬이온 배 터리의 사용이 더욱더 확대되고 있다. 이러한 리튬이온 배 터리는 산업적 관심뿐만 아니라 학문적으로도 현재 활발 한 연구가 진행되고 있다. 리튬이온 배터리는 양극, 음극, 전해질 및 분리막으로 주로 구성되어 있으며, 그 중 전극 물질인 양극 및 음극의 개발은 리튬이온 배터리에 에너지 밀도 및 용량과 같은 성능 향상을 위해서 반드시 필요한 요소이다. 더욱이 음극 물질에는 SnO2, SiO2 및 CNT등이 사용되고 있으며, 양극 물질에는 LiCoO2, LiMn2O4 및 V2O5등이 대표적으로 사용되고 있다. 특히 양극 물질 중 에서도 LiCoO2는 높은 에너지밀도(~140 mAh/g), 우수한 내구성, 높은 작동 전압(~4V) 및 낮은 자가방전 등의 특징 을 가지기 때문에 현재 가장 많은 관심을 받고 있다[1,2]. 이 러한 LiCoO2의 우수한 특성은 결정질 LiCoO2의 rhombohedral layered structure가 리튬 확산을 위해 이동 가능한 통로를 제공하기 때문이다[2]. 또한 최근에는 하이브리드 전기 자동차와 같은 중대형 전자기기를 위한 고출력 에너 지 저장 장치의 수요가 증가됨에 따라 LiCoO2의 고출력특 성을 향상시키는 연구도 다양하게 시도되고 있다. 일반적 으로 고출력 특성은 전극물질이 갖는 입자형태와 작은 입 자사이즈에 매우 의존적이기 때문에 형태제어와 작은 입 자크기를 갖는 LiCoO2의 합성이 요구된다. 이와 같은 입 자감소는 리튬 이온의 짧은 확산거리를 제공하기 때문에 빠른 리튬 이온의 이동을 가능하게 하여 고출력특성을 제 공하게 된다[3]. 예를 들어 Okudo 등은 차세대 고출력 응 용분야를 위한 양극 물질로써 17 nm 크기의 결정으로 이 루어진 LiCoO2의 향상된 고출력특성을 보고했다[4]. 또한 다양한 물질의 형태제어는 온도, 용매, 농도, 계면활성제 및 고분자 등의 조절을 통해 다양하게 시도되고 있지만 LiCoO2에 대한 형태제어의 연구결과는 아직도 미흡한 실 정이다[5, 6]. 따라서 현재까지 연구 그룹들은 LiCoO2을 졸겔법, 주형법, 수열합성법 및 공침법 등의 다양한 방법 으로 합성하고 있다[7-10]. 하지만 이런 방법들은 실험조 건이 어렵고 다량의 용매 및 유기물이 요구된다는 단점이 따르고 있다. 그에 비해 본 연구에서 활용한 전기 방사법 은 상대적으로 장비구조가 간단하고 재현성이 우수하며 제조비용이 저렴한 장점을 가지고 있다[11]. 특히 전기 방 사법은 용액의 농도, 집전체 종류, 첨가제의 종류, 바늘의 형태, 온도 및 습도 등과 같은 변수를 조절함으로써 단일, 복합, 이중, 중공 및 다공성과 같은 다양한 형태의 제조가 가능하다. 예를 들어 An 등은 TiO2에 도핑되는 Nb의 함 량을 조절하여 주름진 형태의 1 차원 나노선 제조에 성공 하였다[12]. 또한 C.L. Casper 등은 전기 방사시 습도 분 위기를 30-60 %로 조절하여 습도가 증가 할수록 합성된 폴리스티렌 섬유의 표면 기공도가 증가한다는 것을 증명 했다[13]. 이와 같이 전기 방사법은 1 차원 나노선을 제조 하는 일반적인 합성법으로 널리 알려져 있다. 하지만 우리 는 전기 방사법을 통해 현재까지 보고되지 않은 2 차원 플 레이크형 LiCoO2 나노 분말을 성공적으로 제조하였으며 그에 따른 구조적 특성 및 형성 메커니즘을 본 논문을 통 하여 연구하였다.
- 따라서, 본 연구에서는 리튬과 코발트 전구체 및 PVP 고분자의 몰 농도를 조절하여 최적화된 조건에서 2 차원 플레이크형 LiCoO2 나노 분말을 전기 방사법을 이용하여 성공적으로 합성하였으며 그들의 형태적, 구조적 및 화학 적 특성을 증명하였다.
서 론
- 본 연구에서는 용액의 몰 농도 제어를 통해 플레이크 형 태를 갖는 LiCoO2 나노 분말을 전기 방사법을 이용하여 제조하였다. 먼저 전기 방사법에 사용될 용액을 제조하기 위해 리튬과 코발트의 전구체인 lithium acetate dehydrate (CH3COOLi∙2H2O, Aldrich)와 cobalt(III) acetate tetrahydrate ((CH3COO)2Co∙4H2O, Aldrich)를 각각 서로 다른 용매에 서 2 시간 동안 용해 시켰으며, 리튬 전구체는 acetic acid (CH3CO2H, Aldrich)와 ethanol(CH3CH2OH, Aldrich)이 혼 합된 용액, 코발트 전구체는 N,N-dimethylformamide (HCON(CH3)2, Aldrich)를 각각 용매로 사용하였다. 균일 하게 용해된 리튬 용액과 코발트 용액을 하나로 3 시간 동안 충분히 혼합한 후 0.026 mM에 해당하는 polyvinylpyrrolidone (PVP, Mw=1,300,000 g/mol, Aldrich)를 첨가하여 점성을 갖는 전기 방사용 용액을 준비하였다. 이때 혼합물 내 리 튬과 코발트 전구체의 혼합비율은 1:1(molar ratio)로 고정 하고 전체 전구체의 몰 농도는 0.45 M, 0.87 M, 1.27 M 가 되도록 조절하였다. 다음으로 제조된 용액을 주사기에 옮겨 전기 방사법을 준비하였다. 이 때, 주사기에 장착된 스테인리스 바늘은 23 gauge이며, DC 고전압 발생기 (Powertron. Co., Ltd., Korea)를 이용하여 바늘 끝 과 포집 판 사이에 고전압을 인가한다. 전기 방사가 수행되는 동안 바늘과 포집판 사이의 거리는 17 cm를 유지하고, 인가 전 압 및 실린지 펌프의 공급유량은 13 kV 및 0.02 mL/h로 각각 고정하였다. 습도와 온도는 20%와 25℃로 유지하였 다. 이렇게 포집된 나노 섬유를 승온 속도를 1℃/min으로 하고 500℃에서 5 시간 동안 열처리하여 LiCoO2 나노 분 말을 얻었다. 여기서 열처리 후 최종적으로 얻은 LiCoO2 나노 분말을 0.45 M의 경우 sample A, 0.87 M의 경우 sample B, 1.27 M의 경우 sample C로 언급할 것이다. 또 한 플레이크형 LiCoO2 나노 분말의 형성 메커니즘을 규명 하기 위하여 1.27 M에 해당하는 용액에 첨가되는 PVP 고 분자 함량을 0.011 mM, 0.026 mM, 0.043 mM로 조절하 였다.
- LiCoO2 나노 분말의 형태를 확인 하기 위하여 주사 전 자 현미경(field-emission scanning electron microscopy, FESEM, Hitachi S-4800)을 사용하였다. 또한 각 sample의 결정구조 및 화학적 결합상태를 규명하기 위하여 X-선 회 절분석(X-ray diffraction, XRD, Rigaku Rint 2500)과 X-선 광전자 주사법(X-ray photoelectron spectroscopy, XPS, ESCALAB 250 equipped with an Al Ka X-ray source)을 수행하였다.
실험방법
- 본 연구에서는 플레이크형 LiCoO2 나노 분말을 제조하 기 위해서 전기 방사법을 사용하였으며 전기 방사법의 모 식도와 실험과정을 그림 1에서 간략하게 묘사하였다. 전 기 방사법의 장치는 전구체를 포함한 점성을 지닌 용액, 이를 일정하게 공급하는 실린지펌프, 나노 섬유를 방사하 기 위한 바늘, 나노 섬유를 포집하기 위한 포집판 및 바늘 과 하부기판 사이에 전압을 발생시킬 수 있는 DC 고전압 발생기로 이루어져 있다. 전기 방사법의 작동원리는 실린 지펌프를 이용하여 일정하게 용액이 공급되면서 바늘 끝 과 포집판 사이에 높은 전압을 걸어주게 되면 표면 장력 에 의한 반구 형태를 유지하던 용액이 불안정한 상태가 되고 용액의 표면 장력보다 더 높은 전압이 인가되면 바 늘 끝에서 방사가 발생하게 되어 1 차원 형태를 갖는 나 노 섬유가 연속적으로 형성된다[14, 15]. 또한 전기 방사법 은 전구체 농도, 고분자의 농도 및 종류, 전압, 습도, 온도 등을 조절하여 현재까지 다양한 나노 재료의 제조 및 형 태 제어에 관한 연구를 보고하고 있다[16, 17]. 따라서, 본 연구에서는 다양한 요인 중에서도 LiCoO2를 제조하기 위 해 전구체 및 PVP 고분자의 몰 농도를 조절하는 실험을 진행하였으며 결과적으로 최적화된 조건에서 2 차원 플레 이크형 LiCoO2 나노 분말을 성공적으로 제조하였다.
- 그림 2는 (a) 열처리 전의 나노 섬유, (b) sample A, (c) sample B, (d) sample C의 FESEM 이미지이다. 열처리 전 의 나노 섬유는 1차원 구조의 매끈한 표면을 갖는 나노선 형태이며 직경은 약 250~361 nm 범위 안에 놓여 있다. 일 반적으로 전기 방사법을 통해 1차원 나노선 형태를 얻기 위해서는 금속 전구체가 포함된 용액에 고분자 물질(PVP) 의 첨가가 이루어 진다. 그리고 나노 섬유에 포함된 PVP 고분자를 제거할 목적으로 공기 중에서 5 시간 동안 500℃에서 열처리를 진행 한다. 이때 1 차원 구조의 나노 선이 제조된다. 그러나 우리의 실험에서는 2 차원 구조를 갖는 sample A, sample B, sample C와 같은 형태의 나노 분말들이 제조되었다. 이는 500℃에서 열처리 시에 리튬 과 코발트 전구체가 결정 성장 및 나노 크기의 응집에 따 라 기존의 나노 섬유 형태를 유지 못한 결과로 판단된다. 더욱이 그림 2에서 보여지는 것처럼 sample A에서 sample C로 갈수록 나노 분말의 형태가 0 차원의 불규칙한 구형 에서 2 차원의 플레이크 형태로 변화 하였다. 그에 따라 sample A, sample B, sample C에 대한 직경이 각각 47~115 nm, 76~188 nm 및 278~496 nm로 나타난다. 이것은 증가 된 전구체의 몰 농도 변화가 입자 형태에 영향을 주는 것 으로 판단된다. 다시 말해서 증가된 몰 농도는 입자의 결 정 성장 속도의 증가와 형성된 결정들의 응집을 크게 유 발시키기 때문에 열처리 후에 LiCoO2 나노 분말이 합성된 다[18]. 따라서 제조된 LiCoO2 나노 분말들의 구조적 및 화학적 특성 변화를 자세히 확인 하기 위하여 XRD와 XPS 실험들을 수행하였다.
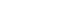
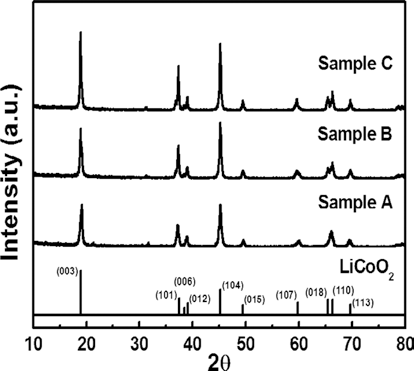
- 그림 3은 전기 방사법으로 제조된 sample A, sample B, sample C의 XRD 회절 피크들을 나타낸다. 모든 샘플들에 특정 회절 피크들은 공통적으로 18.9°, 37.4°, 39.0°, 45.2°, 49.4°, 59.6°, 66.3°, 69.7°에서 각각 나타난다. 이 결과는 rhombohedral layered structure(space group R3m[166])를 갖는 LiCoO2 의 (003), (101), (012), (104), (015), (107), (110), (113) 면들과 일치한다(JCPDS card No.50-0653). 또 한 리튬과 코발트 전구체의 농도가 증가할수록 (006), (012) 면과 (018), (110) 면의 분리가 발생하고 최우선 방향 인 (003) 면의 강도가 증가한다. 이러한 피크들의 분리는 700℃ 이상에서 열처리한 high temperature-LiCoO2(HTLiCoO2) 에서 얻을 수 있는 XRD 결과와 동일하며 뚜렷한 피크의 분리가 발생한 sample C의 경우 결정성이 가장 우 수하다는 것과 동시에 layered structure를 갖는 LiCoO2의 형성을 의미한다[19]. 따라서 전구체의 몰 농도의 증가가 LiCoO2 나노 분말이 가지는 결정성 및 입자 성장을 발생 시킨다[20]. 또한 LiCoO2 의 (003)과 (104) 피크의 강도 비 율은 양이온 무질서화와 밀접한 관계가 있다. 즉 (003)/ (104)의 강도 비율이 증가하면 LiCoO2을 이루는 격자 안 에 양이온들(Li+, Co3+)의 정돈된 배열이 증가하게 된다 [19]. 따라서 sample C의 경우 다른 샘플들과 비교해서 높 은 강도 비율을 보여준다(sample A: 0.94, sample B: 1.01, sample C: 1.05). 이로써 1.27 M의 전구체 농도에서 높은 결정성뿐만 아니라 향상된 rhombohedral layered structure 가지는 LiCoO2 나노 분말을 성공적으로 제조하였다.
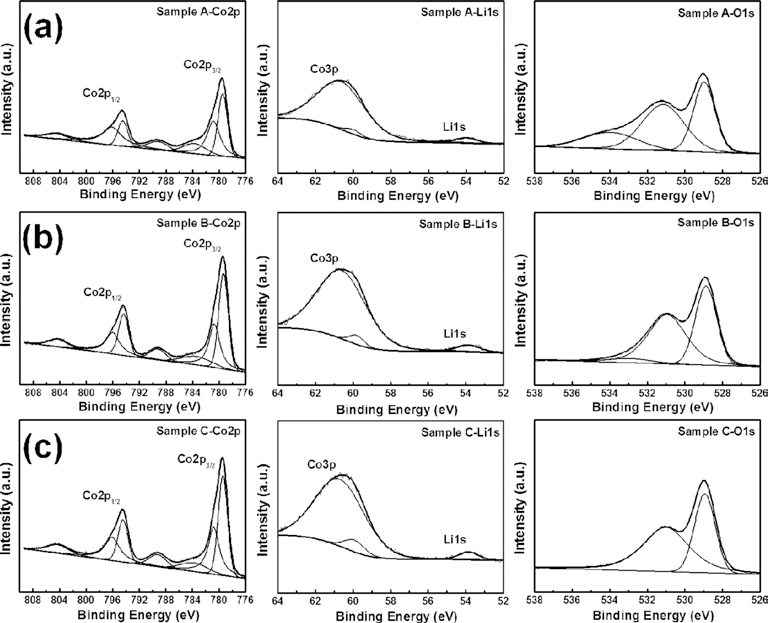
- 그림 4은 전구체의 몰 농도 조절을 통해 제조된 sample A, sample B, sample C를 구성하는 원소의 화학적 결합 상태에 대한 Co 2p core level, Li 1s core level, 및 O 1s core level의 XPS 스펙트럼을 보여준다. 모든 sample들의 피크들은 C 1s 의 284.5 eV를 이용하여 보정하였다. 그림 3(a), (b) 및 (c)에 Co 2p의 XPS 스펙트럼은 총 7 개의 피 크들로 나누어진다. 먼저 778.43 eV 및 794.48 eV에 해당 하는 피크들은 Co3+ 이온, 780.79 eV 및 796.09 eV에 해 당하는 피크들은 Co4+ 이온, 783.71 eV에 해당하는 피크 는 Co2+ 이온을 의미한다. 그리고 789.18 eV와 804.4 eV 에서 나타나는 피크들은 코발트 이온의 위성 피크들이며 이는 LiCoO2 격자의 동일한 환경에 코발트 이온이 존재함 을 의미한다[22]. Li 1s의 스펙트럼의 경우, 53.95 eV에서 대칭성 있는 피크들이 관찰되며 이는 산소 원자로 둘러 쌓인 팔면체 자리 안에 존재하는 리튬 원자를 가리킨다 [23]. 또한 모든 sample들에서 보여지는 60.69 eV의 피크 는 Co 3p에 해당하며 Co3+의 산화 상태를 확인시켜주는 요소로 모든 샘플들에서 LiCoO2 상의 존재를 확인할 수 있다. 뿐만 아니라 59.92 eV에서 미세한 피크가 존재하며 이는 흑연과 결합된 Li 피크를 의미한다[24]. O 1s피크들 에 경우 sample A 및 sample B에서는 총 3 개의 피크들 로 sample C에서는 총 2 개의 피크들로 나누어 진다. 모 든 샘플들에서 공통으로 확인되는 528.95 eV 및 531.19 eV의 피크들은 각각 결정구조에 안에 존재하는 Li-O 및 Co-O의 결합상태를 나타낸다[25]. 하지만 전구체의 농도 가 증가 할수록 532.34 eV에 해당하는 피크가 점차적으로 감소한다는 것을 볼 수 있다. 해당 피크는 LiCoO2내에 존 재하는 OH-의 존재를 의미하며 전구체의 몰농도가 증가 할수록 샘플내에 존재하는 LiOH 및 Co(OH)2 상의 감소 를 의미한다. 따라서 1.27 M의 전구체 농도에서LiCoO2 상의 성공적인 합성을 XPS 결과로부터 알 수 있다. 이로 서 SEM, XRD, XPS 결과를 토대로 1.27 M의 전구체 농 도에서 layered structure를 갖는 플레이크형 LiCoO2 나노 분말의 제조를 확인하였다.
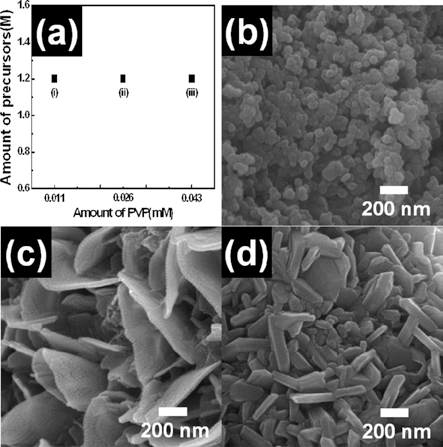
- 플레이크형 LiCoO2 나노 분말이 형성되는 메커니즘을 자세히 알아보기 위해 1.27 M의 전구체 몰 농도에 첨가되 는 PVP 고분자를 0.011 mM, 0.026 mM, 0.043 mM로 조 절하여 실험하였다(그림 5(a)). 그림 5(b)는 0.011 mM의 PVP 고분자를 첨가하였을 때를 나타내는 FESEM 이미지 이며, LiCoO2 나노 분말이 42~89 nm직경을 갖는 불규칙 적인 입자로 존재한다. 더욱이 기존의 0.026 mM보다(그림 5(c)) 증가한 0.043 mM의 PVP 고분자를 첨가할 경우에는 플레이크형 LiCoO2 나노 분말의 두께가 상대적으로 증가 하였다(그림 5(d)). 따라서 LiCoO2 나노 분말이 PVP 고분 자의 몰 농도에 의해 형태가 변화하는 것을 확인 할 수 있 었다. 본 연구에서의 PVP 고분자는 계면활성제로써 초기 입자의 특정면에 선택적으로 흡착되는 특성이 있다고 알 려져 있으며, 이러한 특징으로 인하여 합성되는 LiCoO2입 자의 불규칙적인 뭉침을 방지하고 자가조립을 촉진시킨다 [25]. 그러므로 많은 연구자들은 PVP 고분자를 이용하여 nanorods, nanoplates, nanoparticles과 같은 다양한 구조의 나노 입자를 합성하기 위해 널리 사용하였다. 본 연구에서 는 PVP 고분자를 이용하여 LiCoO2의 layered structure를 갖는 플레이크 형태를 성공적으로 합성하였다[3, 26, 27]. 따라서 전구체의 증가된 몰 농도에서 입자의 결정 성장 속도 증가와 결정들의 응집에 의해 LiCoO2 나노 분말이 형 성되었으며, 최적화된 PVP 고분자 몰 농도에 의한 자가조 립 현상에 의해 플레이크형 LiCoO2 나노 분말이 제조되었 음을 확인 하였다. 다시 말하면 플레이크형 LiCoO2 나노 분 말은 최적의 전구체 몰 농도(1.27 M) 와 PVP 고분자 몰 농 도(0.026 mM)에서 성공적으로 형성되었다. 이렇게 형태가 제어된 플레이크형 LiCoO2 나노 분말은 리튬이온 배터리에 자세히 알아보기 위해 1.27 M의 전구체 몰 농도에 첨가되 는 PVP 고분자를 0.011 mM, 0.026 mM, 0.043 mM로 조 절하여 실험하였다(그림 5(a)). 그림 5(b)는 0.011 mM의 PVP 고분자를 첨가하였을 때를 나타내는 FESEM 이미지 이며, LiCoO2 나노 분말이 42~89 nm직경을 갖는 불규칙 적인 입자로 존재한다. 더욱이 기존의 0.026 mM보다(그림 5(c)) 증가한 0.043 mM의 PVP 고분자를 첨가할 경우에는 플레이크형 LiCoO2 나노 분말의 두께가 상대적으로 증가 하였다(그림 5(d)). 따라서 LiCoO2 나노 분말이 PVP 고분 자의 몰 농도에 의해 형태가 변화하는 것을 확인 할 수 있 었다. 본 연구에서의 PVP 고분자는 계면활성제로써 초기 입자의 특정면에 선택적으로 흡착되는 특성이 있다고 알 려져 있으며, 이러한 특징으로 인하여 합성되는 LiCoO2입 자의 불규칙적인 뭉침을 방지하고 자가조립을 촉진시킨다 [25]. 그러므로 많은 연구자들은 PVP 고분자를 이용하여 nanorods, nanoplates, nanoparticles과 같은 다양한 구조의 나노 입자를 합성하기 위해 널리 사용하였다. 본 연구에서 는 PVP 고분자를 이용하여 LiCoO2의 layered structure를 갖는 플레이크 형태를 성공적으로 합성하였다[3, 26, 27]. 따라서 전구체의 증가된 몰 농도에서 입자의 결정 성장 속도 증가와 결정들의 응집에 의해 LiCoO2 나노 분말이 형 성되었으며, 최적화된 PVP 고분자 몰 농도에 의한 자가조 립 현상에 의해 플레이크형 LiCoO2 나노 분말이 제조되었 음을 확인 하였다. 다시 말하면 플레이크형 LiCoO2 나노 분 말은 최적의 전구체 몰 농도(1.27 M) 와 PVP 고분자 몰 농 도(0.026 mM)에서 성공적으로 형성되었다. 이렇게 형태가 제어된 플레이크형 LiCoO2 나노 분말은 리튬이온 배터리에 양극 전극물질로 응용될 수 있으며 성능 향상이 가능할 것 으로 기대된다. 이러한 성능 향상은 Cho 등의 논문을 통해 서 예측할 수 있다. 다시 말해 본 연구에서 전기 방사법을 이용하여 합성된 플레이크형 LiCoO2 나노 분말과 유사한 plate-LiCoO2로 이루어진 입자들이 일반적인 구형을 띄는 LiCoO2 입자보다 리튬이온 배터리에서 향상된 출력 및 용 량 특성을 보고하였다[28]. 따라서 본 연구에서 얻은 플레이 크형 LiCoO2 나노 분말은 리튬이온 배터리의 성능 향상에 긍정적인 영향을 끼칠 것으로 예상되며, 이와 관련된 실험 은 본 연구실에서 현재 진행 중에 있다.
결과 및 고찰
- 본 연구에서는 전구체 및 PVP 고분자의 몰 농도 변화를 통해 플레이크형 LiCoO2 나노 분말을 전기 방사법을 통해 성공적으로 제조하였다. 전구체의 몰농도는 sample A는 0.45 M, sample B는 0.87 M, sample C는 1.27 M으로 총 3 단 계로 조절하였다. 상대적으로 낮은 0.45 M에서는 LiCoO2 나 노 분말 입자형태가 전체적으로 구형에 가까우며 불균일한 입도분포가 확인되었다. 하지만 몰 농도가 0.87 M, 1.27 M 로 증가하는 경우 입자 형태가 점차 플레이크 형태로 변화 하였음을 알 수 있었다. 또한 이러한 형태 변화에 따른 구조 적 및 화학적 특성을 확인한 결과 증가된 몰 농도 조건에서 LiCoO2 나노 분말의 결정성 상승과 layered structure의 특성 을 확인하였다. 더 나아가 플레이크 형태를 갖는 LiCoO2 나 노 분말에 형성 메커니즘을 확인하기 위해 PVP 고분자의 몰 농도를 0.011 mM, 0.026 mM, 0.043 mM로 조절하였다. 그 결과 0.026 mM의 몰 농도에서 플레이크 형태의 LiCoO2 의 나노 분말이 형성 되었으며, 이는 특정면에 선택적인 흡 착에 의한 불규칙적인 응집 방지와 자가조립이 촉진되는 PVP 고분자의 특성 때문이라고 설명된다.
결 론
-
Acknowledgements
- This study was financially supported by the Research Program funded by the Seoul National University of Science and Technology.
감사의 글
Fig. 2.Top-view FESEM images (a-d) obtained from as-spun nanofibers, sample A, sample B, and sample C.


- 1. H. S Yang, J. H Pee and Y. J Kim, J. Kor. Powd. Met. Inst. (2011) 18 277.Article
- 2. H Xia and L Lu, Electrochim. Acta. (2007) 52 7014.Article
- 3. X Qian, X Cheng, Z Wang, X Huang, R Guo, D Mao, C Chang and W Song, Nanotechnology. (2009) 20 115608.Article
- 4. M Okubo, E Hosono, J D Kim, M Enomoto, N Kojima, T Kudo, H Zhou and I Honma, J. Am. Chem. Soc. (2007) 129 7444.Article
- 5. C Chen, E. M Kelder, P. J. J. M van der Put and J Schoonman, J. Mater. Chem. (1996) 6 765.Article
- 6. H. P Lin and C. Y Mou, Acc. Chem. Res. (2002) 35 927.Article
- 7. Z. S Peng, C. R Wan and C. Y Jiang, J. Power Sources. (1998) 72 215.Article
- 8. F Jiao, K. M Shaju and P. G Bruce, Angew. Chem. Int. Ed. (2005) 44 6550.Article
- 9. A Burukhin, O Brylev, P Hany and B. R Churagulov, Solid State Ionics. (2002) 151 259.Article
- 10. H Chen, X Qiu, W Zhu and P Hagenmuller, Electrochem. Commun. (2002) 4 488.Article
- 11. Y. I Lee and Y. H Choa, J. Kor. Powd. Met. Inst. (2012) 9 271.
- 12. H. L An and H Ahn, J. Mater. Lett. (2013) 93 88.Article
- 13. C. L Casper, J. S Stephens, N. G Tassi, D. B Chase and J. F Rabolt, Macromolecules. (2004) 37 573.ArticlePDF
- 14. H. T Kim, C. Y Hwang, H. B Song, K. J Lee, Y. J Joo, S. J Hong, N. K Kang, S. D Park, K. D Kim and Y. H Choa, J. Kor. Powd. Met. Inst. (2008) 15 114.Article
- 15. Z Wang, X Liu, M Lv, P Chai, Y Liu and J Meng, J. Phys. Chem. B. (2008) 112 11292.Article
- 16. S Megelski, J. S Stephens, D. B Chase and J. F Rabolt, Macromolecules. (2002) 35 8456.Article
- 17. K. H Lee, H. Y Kim, H. J Bang, Y. H Jung and S. G Lee, Polymer. (2003) 44 4029.Article
- 18. A. R Babar, S. S Shinde, A. V Moholkar, C. H Bhosale, J. H Kim and K. Y Rajpure, J. Alloys Compd. (2011) 509 3108.Article
- 19. J Fu, Y Bai, C Liu, H. J Yu and Y Mo, J. Mater. Chem. Phys. (2009) 115 105.Article
- 20. A. A Akl, Appl. Surf. Sci. (2006) 252 8745.Article
- 21. M Das, R Ranjith, C Bittencourt, S. B Krupanidhi, J. J Pireaux and S. A Shivashankar, Appl. Phys. A. (2009) 95 523.ArticlePDF
- 22. R Alcántara, G. F Ortiz, P Lavela, J. L Tirado, W Jaegermann and A Thißen, J. Electroanal. Chem. (2005) 584 147.
- 23. L Dahéron, R Dedryvère, H Martinez, M Ménétrier, C Denage, C Delmas and D Gonbeau, Chem. Mater. (2008) 20 583.Article
- 24. Y Aykut, B Pourdeyhimi and S. A Khan, J. Phys. Chem. Solids. (2013) 74 1538.Article
- 25. Y. J Zhang, Q Yao, Y Zhang, T. Y Cui, D Li, W Liu, W Lawrence and Z. D Zhang, Cryst. Growth Des. (2008) 8 3206.Article
- 26. T Watanabe, H Uono, S. W Song, K. S Han and M Yoshimura, J. Solid State Chem. (2001) 162 364.Article
- 27. Y Shao-Horn, S. A Hackney, A. J Kahaian and M. M Thackeray, J. Solid State Chem. (2002) 168 60.Article
- 28. M. K Jo, S. Y Jeong and J. P Cho, Electrochem. Commun. (2010) 12 992.Article
REFERENCES
Figure & Data
References
Citations
Citations to this article as recorded by 

- Electrochemical Behavior of Well-dispersed Catalysts on Ruthenium Oxide Nanofiber Supports
Geon-Hyoung An, Hyo-Jin Ahn
Journal of Korean Powder Metallurgy Institute.2017; 24(2): 96. CrossRef - Synthesis and Characterization of SnO2-CoO/carbon-coated CoO Core/shell Nanowire Composites
Yu-Jin Lee, Bon-Ryul Koo, Hyo-Jin Ahn
Journal of Korean Powder Metallurgy Institute.2014; 21(5): 360. CrossRef
Fabrication of Flake-like LiCoO2 Nanopowders using Electrospinning


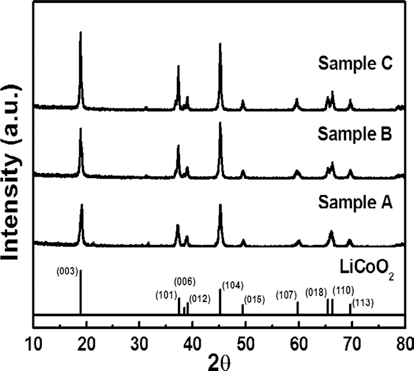
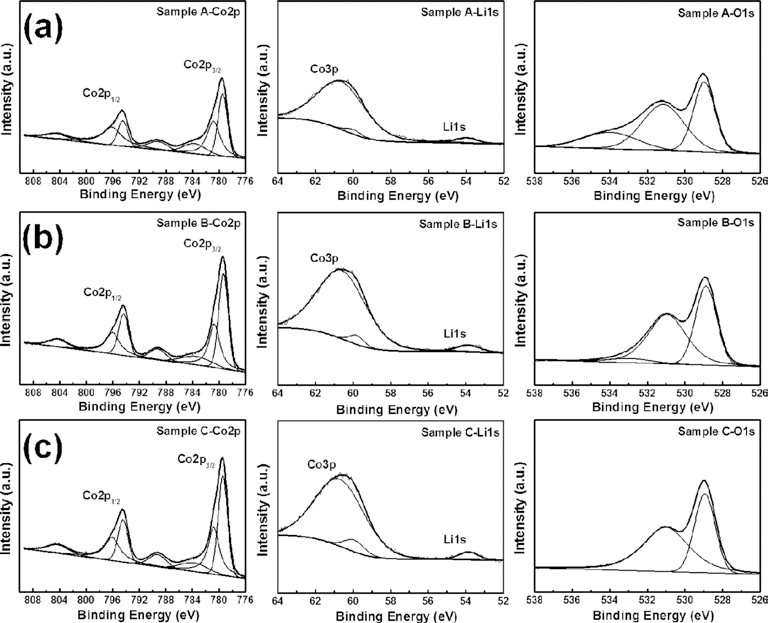
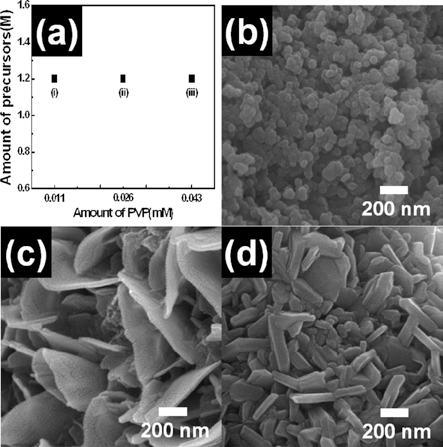
Fig. 1.
A schematic illustration of electrospinning apparatus and preparation procedure.
Fig. 2.
Top-view FESEM images (a-d) obtained from as-spun nanofibers, sample A, sample B, and sample C.
Fig. 3.
XRD plots obtained from sample A, sample B, and sample C.
Fig. 4.
XPS spectra of the Co 2p, Li 1s and O 1s core levels for sample A, sample B, and sample C.
Fig. 5.
The amount dependence of a PVP polymer for 1.2 M LiCoO2 nanopowders.
Fig. 1.
Fig. 2.
Fig. 3.
Fig. 4.
Fig. 5.
Fabrication of Flake-like LiCoO2 Nanopowders using Electrospinning
TOP
 KPMI
KPMI


 Cite this Article
Cite this Article