Articles
- Page Path
- HOME > J Powder Mater > Volume 29(5); 2022 > Article
-
Article
알칼라인 수전해 산소 발생 반응을 위한 NiCo2O4/Ni foam 전극 제조 및 특성 평가 - 권민솔a, 고재성b, 이예솔b, 이성민b, 유지수b, 이효원b, 송성호c,*, 이동주a,b,*
- Fabrication and Characterization of NiCo2O4/Ni Foam Electrode for Oxygen Evolution Reaction in Alkaline Water Splitting
- Minsol Kwona, Jaeseong Gob, Yesol Leeb, Sungmin Leeb, Jisu Yub, Hyowon Leeb, Sung Ho Songc,*, Dongju Leea,b,*
-
Journal of Korean Powder Metallurgy Institute 2022;29(5):411-417.
DOI: https://doi.org/10.4150/KPMI.2022.29.5.411
Published online: September 30, 2022
a 충북대학교 도시·에너지·환경 융합학부
b 충북대학교 신소재공학과
c 공주대학교 신소재공학부
a Department of Urban, Energy, and Environmental Engineering, Chungbuk National University, Chungdae-ro 1, Seowon-Gu, Cheongju, Chungbuk 28644, Republic of Korea
b Department of Advanced Materials Engineering, Chungbuk National University, Chungdae-ro 1, Seowon-Gu, Cheongju, Chungbuk 28644, Republic of Korea
c Division of Advanced Materials Engineering, Kongju National University, Chungnam 330-717, Cheonan-si, Republic of Korea
-
* Corresponding Authors: Dongju Lee, TEL: +82-43-261-2414, FAX: +82-43-271-3222, E-mail: dongjulee@chungbuk.ac.kr
Sung Ho Song, TEL: +82-41-521-9379, FAX: +82-41-568-5776, E-mail: shsong805@kongju.ac.kr - - 권민솔·고재성·이예솔·이성민·유지수·이효원: 학생, 송성호·이동주: 교수
© The Korean Powder Metallurgy Institute. All rights reserved.
- 1,169 Views
- 11 Download
Abstract
- Environmental issues such as global warming due to fossil fuel use are now major worldwide concerns, and interest in renewable and clean energy is growing. Of the various types of renewable energy, green hydrogen energy has recently attracted attention because of its eco-friendly and high-energy density. Electrochemical water splitting is considered a pollution-free means of producing clean hydrogen and oxygen and in large quantities. The development of non-noble electrocatalysts with low cost and high performance in water splitting has also attracted considerable attention. In this study, we successfully synthesized a NiCo2O4/NF electrode for an oxygen evolution reaction in alkaline water splitting using a hydrothermal method, which was followed by post-heat treatment. The effects of heat treatment on the electrochemical performance of the electrodes were evaluated under different heat-treatment conditions. The optimized NCO/NF-300 electrode showed an overpotential of 416 mV at a high current density of 50 mA/cm2 and a low Tafel slope (49.06 mV dec-1). It also showed excellent stability (due to the large surface area) and the lowest charge transfer resistance (12.59 Ω). The results suggested that our noble-metal free electrodes have great potential for use in developing alkaline electrolysis systems.
- 현재의 에너지 시스템은 화석 연료를 기반으로 하고 있 으나, 지구온난화 및 대기오염과 같은 환경 문제와 향후 자원 고갈 우려 문제로 인해 대체 에너지원의 필요성이 강조되고 있다. 이에 화석 연료를 대체할 수 있는 에너지 로 태양광, 풍력, 수소 에너지와 같은 신재생에너지에 관 한 연구가 활발하게 진행되고 있다[1-4]. 특히, 수소 에너 지는 친환경적이며, 에너지 밀도가 높고 기체, 액체, 화합 물과 같이 다양한 형태로의 에너지 저장 및 운송이 가능 하다는 장점이 있다[5]. 이러한 수소 에너지는 천연 가스 개질, 물의 열분해, 전기분해 및 광분해 공정과 바이오 매 스 등의 방법으로 생산되고 있다[6]. 현재는 주로 가격이 저렴한 천연 가스 개질 공정을 통해 수소를 생산하고 있 으나, 1 kg의 수소를 생산하는데 약 10 kg의 이산화탄소를 배출하여 환경 오염을 가속화한다는 치명적인 단점이 있 다. 이러한 생산방식의 단점을 극복하기 위해 최근 신재생 에너지 기반 수전해 기술이 대두되고 있다. 이는 신재생에 너지에서 얻은 전기로 물을 분해하여 수소를 생산하는 방 식이기 때문에 온실가스를 배출하지 않는 청정에너지 시 스템을 구축할 수 있는 장점이 있다[7].
- 수전해 기술의 종류로는 이동하는 이온의 종류에 따라 고체 산화물 수전해(solid oxide electrolysis), 양이온 교환 막 수전해(proton exchange membrane electrolysis), 알칼라 인 수전해(alkaline electrolysis) 등이 있다[8]. 이 중 알칼 라인 수전해 기술은 가장 일찍 상용화되어 가격이 저렴하 고 모듈 사이즈의 대형화가 가능해 장기/대용량 에너지 저 장에 적합하다[9]. 이론적으로는 알칼라인 수전해의 이론 분해 전압인 1.23 V를 전극에 가해주면, 양극에서 수소와 산소가 발생하나, 전극 표면의 저항, 전해질과 전극 사이 의 저항 등에 의해 실제로 1.23 V 보다 더 높은 전압이 필 요하게 되는데 이를 과전압(overpotential)이라 한다. 물의 전기분해는 cathode에서 수소 발생 반응(hydrogen evolution reaction), anode에서 산소 발생 반응(oxygen evolution reaction) 이 일어나는데[10], 수소 발생 반응은 2 개의 전자가 참여하는 반응인 반면, 산소 발생 반응은 4 개의 전자가 참 여하는 반응으로, 속도가 더 느려 보다 높은 과전압이 요구 된다. 때문에 산소 발생 반응에서 발생하는 전압 손실을 낮 춰 수전해 반응의 효율을 향상시키는 것이 중요하다[11, 12].
- 현재는 Ir, Pt와 같은 귀금속 또는 귀금속 산화물을 수전 해의 전극 재료로 사용하고있는데, 이러한 귀금속 물질은 내식성과 효율이 우수하지만, 가격이 매우 비싸고 희귀하 다는 한계점이 있어 상대적으로 저렴한 비귀금속 화합물 을 전극 촉매로 활용하는 연구들이 활발히 진행되고 있다 [13-15]. 그 중에서도 Ni은 알칼리 조건에서 높은 내식성 과 반응 활성을 보유하고 있으나[16], 산소 발생 반응에 대한 전기화학적 활성이 낮으며, 귀금속 대비 높은 과전압 으로 인해 성능이 떨어진다. 이를 극복하고자 Ni을 기반 으로 Fe, Co, Cu 등의 전이금속 물질과 혼합하여 화합물 을 합성하는 연구가 진행되고 있다[17]. 특히 Ni-Co 산화 물은 비교적 높은 전기 전도도를 가지기 때문에 과전압을 낮출 수 있으며[18], 우수한 산소 발생 반응 활성을 나타 내므로 이를 활용하면 알칼라인 수전해의 산소 발생 효율 향상에 기여할 수 있을 것으로 기대된다[19].
- 본 연구에서는 알칼라인 수전해 반응 효율을 향상시키 기 위해 산소 발생 반응의 과전압을 낮추고 활성 표면적 향상을 위해 수열 합성법(hydrothermal method)을 통해 다 공성 니켈 폼(nickel foam, NF) 위에 침상 형태의 니켈 코 발트 산화물(NiCo2O4) 어레이(array)를 합성해 전극을 제 조하고, 후열처리(post heat treatment) 공정 변수에 따른 전극 소재들의 물성 분석 및 전기화학적 특성 평가를 진 행하였다.
1. 서 론
- 전기 전도도가 높고 비표면적이 넓은 다공성 N i foa m (thickness 1.6 mm, porosity ≥ 95%)을 활용하였으며, 수열 합성을 통해 NiCo2O4 물질을 합성하기 위한 전구체로는 Ni(NO3)2·6H2O(Nickel nitrate hexahydrate, Sigma Aldrich), Co(NO3)2·6H2O(Cobalt nitrate hexahydrate, JUNSEI Chemical), urea(CO(NH2)2, Sigma Aldrich)를 사용하였다.
- 먼저, Ni foam 표면의 산화막을 제거하기 위해 3M의 HCl 용액에 15 분간 전처리 공정을 진행한 후, 아세톤, 에 탄올, 증류수 순서로 각각 10 분씩 초음파 처리를 진행하여 불순물 제거 및 염산으로 인해 낮아진 pH를 높여주었다.
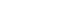
- 증류수 30 ml에 Ni(NO3)2·6H2O, Co(NO3)2·6H2O, urea를 각각 0.2 M, 0.4 M, 1.0 M로 적정 몰비의 양으로 용해한 후, 혼합 용액을 전처리한 Ni foam과 함께 autoclave 반응 기에 넣어 120°C에서 6 시간 동안 수열 합성 공정을 진행 하였다. 수열 합성된 전극을 증류수와 에탄올을 사용해 세 척하여 잔여 불순물을 제거한 후, 진공 오븐에서 건조시킨 다음, NiCo2O4 결정성 향상을 위해 열처리 공정을 진행하 였다. 이때, 열처리 조건은 200, 300, 400°C에서 2 시간 동 안 5°C/min의 승온속도로 대기 분위기에서 진행하였고, 각 전극은 열처리 조건에 따라 NCO/NF-200, NCO/NF- 300, NCO/NF-400로 표기하였다. Fig. 1에 공정 과정을 모 식도로 나타냈다.
- 제조된 전극의 상 분석은 X선 회절 분석기(X-ray Diffractometer, JP/SmartLab, Rigaku)를 이용하여 진행하였으며, 전극 표면의 화학적 분석은 X선 광전자 분광기(X-ray photoelectron spectroscopy, K-Alpha+, ThermoFisher Scientific) 를 통해 진행하였다. 주사전자현미경(Scanning Electron Microscope, Crossbeam 540, ZEISS)과 투과전자현미경 (Transmission Electron Microscope, JEM-ARM200F, JEOL) 을 이용해 제조한 전극의 미세조직 및 결정구조를 분석하 였다.
- 전기화학 특성평가는 WonATech 사의 ZIVE SP 1 장비 를 이용해 3전극 전기화학 셀로 진행하였다. 비교군으로 5 mg의 RuO2 분말과 IrO2 분말을 각각 500 μL의 증류수 와 495 μL의 에탄올 혼합 용액에 분산시킨 다음, 50 μL의 Nafion(10 wt%) 용액을 첨가하여 N i foa m에 400 μL을 떨 어뜨려 건조시킨 후 동일한 방법으로 측정하였다. 기준전 극과 상대전극은 각각 Hg/HgO 전극과 Pt 전극을 사용하 였다. 전해질로는 SAMCHUN chemical 사의 1M KOH 용액을 사용하였으며, 특성평가를 진행하기 전에 N2 purge 를 통해 전해질에 존재하는 용존 산소를 제거하였다. 측정 된 전압은 Reversible hydrogen electrode(RHE)로 변환하 여 iR 보정 없이 사용하였고, 변환식은 다음과 같다.
- 산소 발생 반응을 평가하기 위해 1.0 ~ 1.8 V(V vs RHE) 의 범위에서 5 mV s-1의 scan rate로 Linear sweep voltammetry( LSV) 측정을 진행하였으며, 이를 바탕으로 Ta fel slope을 계산하였으며 계산식은 다음과 같다.
- 위 식에서 Ƞ은 과전압, a는 상수, b는 Tafel slope, j는 전 류 밀도를 나타낸다.
- Electrochemical impedance spectroscopy(EIS) 분석은 100 kHz ~ 10 mHz의 주파수 범위에서 1.53 V(V vs RHE) 의 전압을 인가하여 진행하였으며, 전극의 안정성을 평가 하기 위해 50 mA/cm2에 해당하는 전류를 18 시간 동안 인가하여 Chronoamperometry(CA) 분석을 진행하였다.
2. 실험방법
Schematic illustration of fabrication process of from hydrothermal synthesis NiCo2O4/Ni foam electrode.
- 제조한 NCO/NF-300전극의 공정에 따른 디지털 이미지 를 Fig. 2에 나타내었다. Fig. 2a는 전처리된 Ni foam, F ig. 2b는 수열 합성 공정 이후의 전극, Fig. 2c는 수열 합성 및 후열처리 공정을 거친 전극이다. 공정이 진행됨에 따라 진 한 검은 빛깔을 나타내는 전극의 모습을 확인할 수 있다.
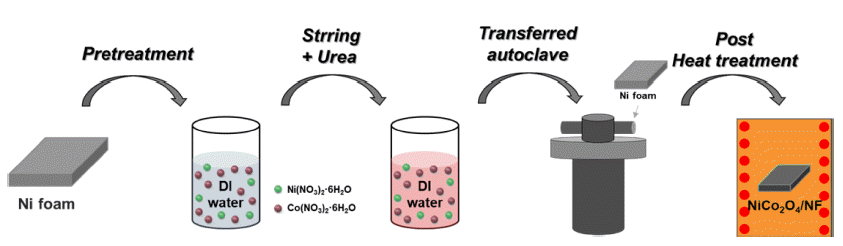
- 제조된 전극의 상 분석과 전극 표면의 화학적 분석 결 과를 Fig. 3에 나타내었다. Fig. 3a는 후열처리 온도에 따 라 제조된 전극의 XRD 패턴 결과를 나타낸 것으로, 제조 된 모든 전극에서 31.1°, 36.7°, 59.1°, 65.0°의 2θ 값에서 회 절 피크가 나타났으며, 이는 각각 NiCo2O4의 (220), (311), (511), (440) 면에 해당되는 것을 통해 NiCo2O4(PDF#20- 0781) 상이 형성되었음을 확인하였다[20, 21]. 후열처리의 온도가 증가할수록 NiCo2O4에 해당하는 피크의 강도가 증 가하는 것으로 보아 열처리 온도가 높아질수록 NiCo2O4상 의 결정성이 향상되는 것으로 판단할 수 있다. Fig. 3b-e는 전극 표면의 화학적 결합 분석을 위해 진행한 XPS 결과 를 나타낸 것으로, Fig. 3c에 나타낸 Ni 2p 스펙트라에서 는 Ni 2p3/2와 Ni 2p1/2에 대한 피크(854.73 eV, 872.63 eV) 와 satellite 피크(861.03 eV, 879.63 eV)가 관찰되었다. Fig. 3d의 Co 2p 스펙트라에서도 유사하게 Co 2p3/2와 Co 2p1/2 에 대한 피크(779.53 eV, 794.78 eV)와 satellite 피크(788.23 eV, 803.78 eV)가 관찰되었으며, 이는 Ni2+, Ni3+ 이온과 Co2+, Co3+ 이온들이 합성된 NiCo2O4 물질의 스피넬 구조 에서 octahedral과 tetrahedral site를 점유하고 있음을 나타 낸다[22, 23]. 이어서 Fig. 3e에 나타난 O 1s 스펙트라에서 는 529.28 eV에서 금속과 산소 원자의 화학적 결합인 M-O (M = Ni, Co) 결합을 나타내는 피크가 관찰되었고, 530.88 eV에서는 hydroxide 결합을 나타내는 피크가 관찰되었으 며, 532.73 eV에서는 전극 표면에 흡착된 물 분자를 나타 내는 피크가 관찰되었다[24-26].
- Fig. 4는 b a re NF 및 제조된 NCO/NF 전극의 후열처리 온도에 따른 SEM 저배율과 고배율 이미지를 나타낸 것이 다. Fig. 4c-d, 4e-f, 4g-h는 각각 NCO/NF-200, NCO/NF- 300, NCO/NF-400전극의 미세구조이다. 수열합성 전 b a re NF은 전체적으로 smooth한 표면을 보이고 있으나, 수열 합성과 후열처리 된 NCO/NF 전극의 경우 약 10 um 길이 를 갖는 needle 형태의 NiCo2O4가 꽃과 같은 형태를 보이 고 있는 것을 확인할 수 있다. 또한, 후열처리 공정의 온 도가 증가할수록 needle 이 성장하며 needle간 간극이 커 지는 것을 관찰할 수 있다.
- Fig. 5는 N i foa m 표면에 합성된 n eedle a rra y의 결정구 조 및 미세조직을 분석하기 위한 TEM이미지로, 약 900 nm 직경을 가진 needle 형태의 NiCo2O4임을 확인할 수 있 었다. Fig. 5c의 HR-TEM 이미지를 통해 NiCo2O4의 (311) 결정면에 해당하는 면간 거리인 0.245 nm가 관찰되었으며 [27, 28], Fig. 5d에 나타난 SAED 패턴을 통해 (111), (311), (422) 결정면들을 나타내는 패턴들을 확인함으로써 NiCo2O4 가 Ni foam 기판 위에 다결정 형태로 합성되었음을 알 수 있다[29, 30]. Fig. 5e는 해당 nano needle의 EDS mapping 결과로, Ni, Co 및 O에 해당하는 각 원소들이 균일하게 분포되어 있는 것을 확인할 수 있다.
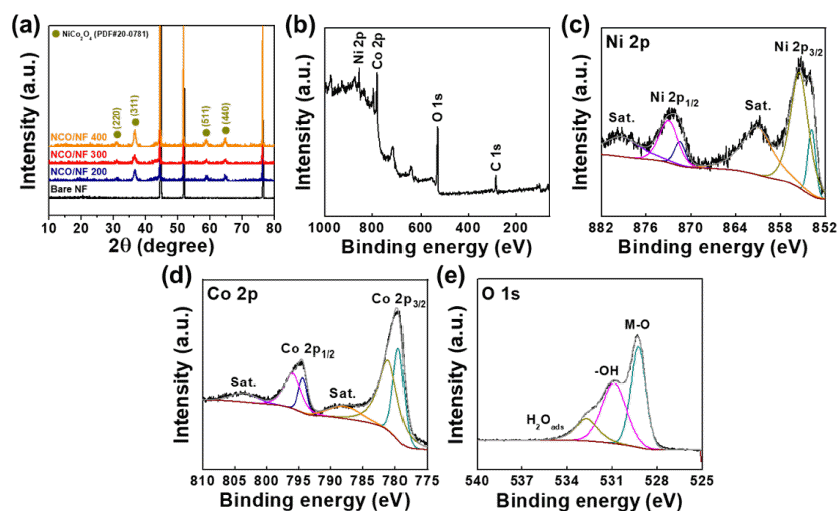
- 제조된 전극 및 비교군인 RuO2/NF와 IrO2/NF 전극을 3 전극 셀로 조립하고 1M의 KOH를 전해질로 사용하여 상 온에서 전기화학 특성평가를 진행하고 이에 대한 결과를 Fig. 6에 나타내었다. Fig. 6a는 전극의 산소 발생 능력을 평가하기 위해 양의 전압을 인가함에 따라 측정되는 전류 밀도를 나타낸 LSV곡선 그래프이다. 50 mA/cm2의 전류 밀도를 기준으로 하여 전극들의 과전압을 비교해보았을 때, NCO/NF-300 전극은 416mV으로 NCO/NF-200(425 mV) 전극과 NCO/NF-400(435 mV) 전극에 비해 낮은 과전압을 나타내었으며, 비교군인 RuO2/NF(457 mV), IrO2/NF(441 mV) 전극보다 우수한 특성을 보이는 것을 확인할 수 있 다. Fig. 6b의 LSV 측정 결과를 바탕으로 도식한 전극들 의 Tafel plot 결과에서도 NCO/NF-300 전극이 가장 낮은 Tafel slope 값으로, 가장 우수한 산소 발생 반응 특성을 보인다는 것을 확인할 수 있다. 이는 Fig. 6c의 EIS 분석 을 통해 얻어진 전극들의 Nyquist plot 그래프에서 알 수 있듯이 전극 계면에서 전자 및 전하가 이동할 때 발생하 는 전하 전달 저항(Charge transfer resistance, Rct) 값이 NCO/NF-300이 가장 낮은 값(12.59 Ω)을 보이기 때문이다 (NCO/NF-200: 13.49 Ω, NCO/NF-400: 13.35 Ω)[31]. 해당 전기화학적 성능평가 결과를 통해 NCO/NF-300전극이 가 장 우수한 산소 발생 특성을 나타낸다는 것을 알 수 있다. 비정질 물질은 결정질 물질에 비해 무작위로 배향된 결합 을 포함하여 더 많은 결함을 가질 수 있고, 이는 전기촉매 로써 중간체의 흡탈착을 더욱 최적화시킬 수 있다고 알려 져 있다[32]. 때문에 더 높은 결정성을 갖는 NCO/NF-400 전극보다 비정질과 결정질상이 혼합된 NCO/NF-300전극 이 보다 우수한 성능을 나타낸다고 생각할 수 있다. Fig. 6d는 NCO/NF-300전극의 장기 안정성 테스트 결과를 나 타내는 그래프로, 50 mA/cm2의 전류 밀도에 해당하는 전 류를 18 시간 동안 인가한 결과, 18 시간 동안 전압의 변 화가 거의 없이 일정하게 유지되며 우수한 안정성을 보이 는 것을 확인하였다.
3. 결과 및 고찰
Optical images of electrodes. (a) Bare NF electrode, (b) electrode after hydrothermal synthesis process and (c) electrode after hydrothermal synthesis and post heat treatment process (NCO/NF-300).

XRD patterns of electrodes and XPS spectra of NCO/NF-300 for structural and chemical analysis. (a) XRD patterns and (b-e) XPS spectra of NCO/NF-300; (b) survey, (c) Ni 2p, (d) Co 2p, and (e) O 1s.
(a-b) SEM images of prepared electrodes at various magnifications. (a-b) Bare NF, (c-d) NCO/NF-200, (e-f) NCO/NF- 300, (g-h) NCO/NF-400.

(a-b) TEM images of NCO/NF-300 at different magnifications. (c) HR-TEM image of NCO/NF-300. (d) SAED pattern of NCO/NF-300. (e) EDS mapping images.

Electrochemical analysis of OER in 1.0M KOH electrolyte. (a) Polarization curves, (b) Tafel plots of NCO/NF-200, NCO/NF-300, NCO/NF-400, Bare NF, RuO2/NF, IrO2/NF. (c) Nyquist plots of NCO/NF-200, NCO/NF-300, NCO/NF-400, Bare NF. (d) Chronoamperometry measurement of OER by NCO/NF 300 for 18 h.
- 본 연구에서는 수열 합성법을 통해 Ni foam 위에 needle 형태의 NiCo2O4 array를 합성하고 후열처리 조건에 따른 NiCo2O4/NF 전극의 전기화학적 특성평가를 통해 산소 발 생 능력을 평가하였다. 최적 조건으로 제조된 NCO/NF- 300 전극의 경우 50mA/cm2의 전류 밀도에서 416mV의 과전압과 낮은 Ta fel 기울기 값 49.06 mV dec-1을 나타내 어 기존 귀금속계 촉매와 비교했을 때 우수한 특성을 보 이고 있으며, 장기 안정성 또한 우수함을 확인하였다. 이 는 다공성 Ni foam을 활용한 넓은 비표면적과 후열처리를 통한 결정성 형성으로 인한 낮은 charge transfer resistance 때문으로 판단된다. 이를 통해 제조된 전극은 알칼라인 수 전해 산소 발생 반응을 위한 저비용 고효율 전극으로 사 용이 될 수 있을 것으로 기대된다.
4. 결 론
-
Acknowledgements
- 이 논문은 충북대학교 국립대학육성사업(2021)지원을 받아 작성되었음.
감사의 글
- 1. H. Ishaq and I. Dincer: Renewable Sustainable Energy Rev., 135 (2021) 110192..Article
- 2. H. Lund: Energy, 32 (2007) 912..Article
- 3. O. Ellabban, H. Abu-Rub and F. Blaabjerg: Renewable Sustainable Energy Rev., 39 (2014) 748..Article
- 4. V. Sebestyén: Renewable Sustainable Energy Rev., 151 (2021) 111626..Article
- 5. I. Dincer and C. Acar: Int. J. Hydrogen Energy, 42 (2017) 14843..Article
- 6. P. K. Rohith, J. Priolkar and G. R. Kunkolienkar In Hydrogen: An innovative and alternative energy for the future, 2016 World Conference on Futuristic Trends in Research and Innovation for Social Welfare (Startup Conclave), 29 (2016) 1..Article
- 7. C. Acar and I. Dincer: Int. J. Hydrogen Energy, (2022)..
- 8. O. Schmidt, A. Gambhir, I. Staffell, A. Hawkes, J. Nelson and S. Few: Int. J. Hydrogen Energy, 42 (2017) 30470..Article
- 9. Z.-Y. Yu, Y. Duan, X.-Y. Feng, X. Yu, M.-R. Gao and S.- H. Yu: Adv. Mater., 33 (2021) 2007100..ArticlePubMed
- 10. C. Hu, L. Zhang and J. Gong: Energy Environ. Sci., 12 (2019) 2620..Article
- 11. M.-I. Jamesh and M. Harb: J. Energy Chem., 56 (2021) 299..Article
- 12. Q. Xu, J. Zhang, H. Zhang, L. Zhang, L. Chen, Y. Hu, H. Jiang and C. Li: Energy Environ. Sci., 14 (2021) 5228..Article
- 13. D. A. Corrigan and R. M. Bendert: J. Electrochem. Soc., 136 (1989) 723..Article
- 14. V. Vij, S. Sultan, A. M. Harzandi, A. Meena, J. N. Tiwari, W.-G. Lee, T. Yoon and K. S. Kim: ACS Catalysis, 7 (2017) 7196..Article
- 15. S. Trasatti: Electrochimi. Acta, 29 (1984) 1503..Article
- 16. J. Luo, J.-H. Im, M. T. Mayer, M. Schreier, M. K. Nazeeruddin, N.-G. Park, S. D. Tilley, H. J. Fan and M. Grätzel: Science, 345 (2014) 1593..ArticlePubMed
- 17. J. Kubisztal and A. Budniok: Int. J. Hydrogen Energy, 33 (2008) 4488..Article
- 18. H. Dai, A. Javey, E. Pop, D. Mann, W. Kim and Y. Lu: Nano, 01 (2006) 1..Article
- 19. Z. W. Seh, J. Kibsgaard, C. F. Dickens, I. Chorkendorff, J. K. Nørskov and T. F. Jaramillo: Science, 355 (2017) eaad4998..
- 20. S. Khalid, C. Cao, L. Wang and Y. Zhu: Sci. Rep., 6 (2016) 22699..ArticlePubMedPMC
- 21. Y. Gong, Z. Yang, Y. Lin, J. Wang, H. Pan and Z. Xu: J. Mater. Chem. A, 6 (2018) 16950..Article
- 22. H. Park, B. H. Park, J. Choi, S. Kim, T. Kim, Y.-S. Youn, N. Son, J. H. Kim and M. Kang: Nanomaterials, 10 (2020) 1727..ArticlePubMedPMC
- 23. M. Qin, D. Lan, G. Wu, X. Qiao and H. Wu: Appl. Surf. Sci., 504 (2020) 144480..Article
- 24. A. Y. Faid and H. Ismail: ChemistrySelect, 4 (2019) 7896. .Article
- 25. J.-L. Ortiz-Quiñonez, U. Pal and M. S. Villanueva: ACS Omega, 3 (2018) 14986..ArticlePubMedPMC
- 26. L. Zhang, Y. Li, J. Peng and K. Peng: Electrochim. Acta, 318 (2019) 762..Article
- 27. J. Liu, J. Zhang, D. Wang, D. Li, J. Ke, S. Wang, S. Liu, H. Xiao and R. Wang: ACS Sustainable Chemistry & Engineering, 7 (2019) 12428..
- 28. Z. Peng, D. Jia, A. M. Al-Enizi, A. A. Elzatahry and G. Zheng: Adv. Energy Mater., 5 (2015) 1402031..Article
- 29. T. Zhang, K. Yang, C. Wang, S. Li, Q. Zhang, X. Chang, J. Li, S. Li, S. Jia, J. Wang and L. Fu: Adv. Energy Mater., 8 (2018) 1801690..Article
- 30. Q. Ouyang, Z. Lei, Q. Li, M. Li and C. Yang: J. Mater. Chem. A, 9 (2021) 14466..Article
- 31. F.-T. Tsai, Y.-T. Deng, C.-W. Pao, J.-L. Chen, J.-F. Lee, K.-T. Lai and W.-F. Liaw: J. Mater. Chem. A,, 8 (2020) 9939..Article
- 32. Y. Zhai, X. Ren, J. Yan and S. Liu: Small Structures, 2 (2021) 2000096..Article
Figure & Data
References
Citations

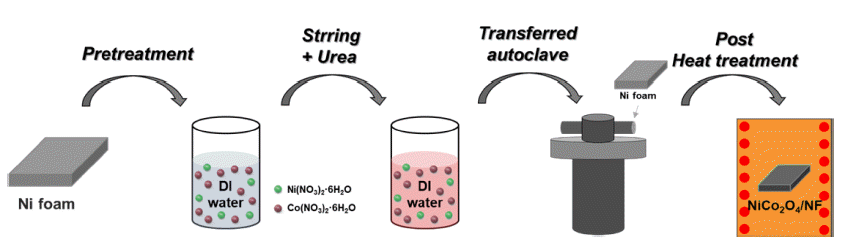

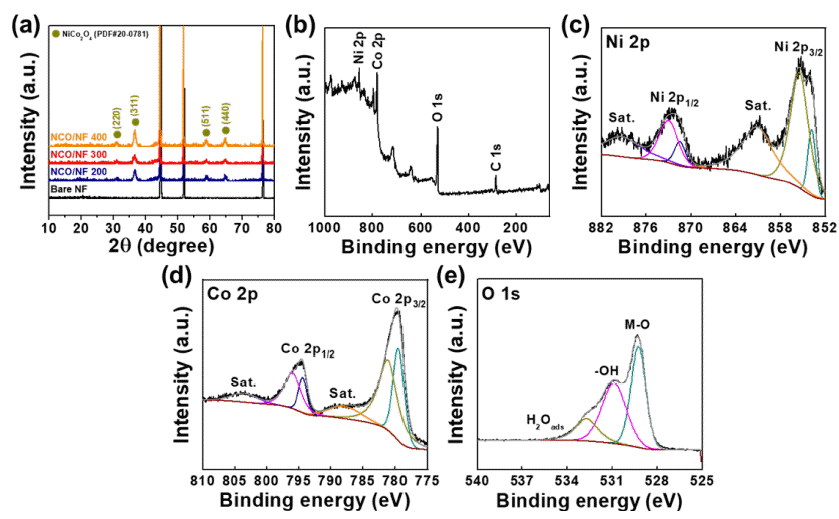


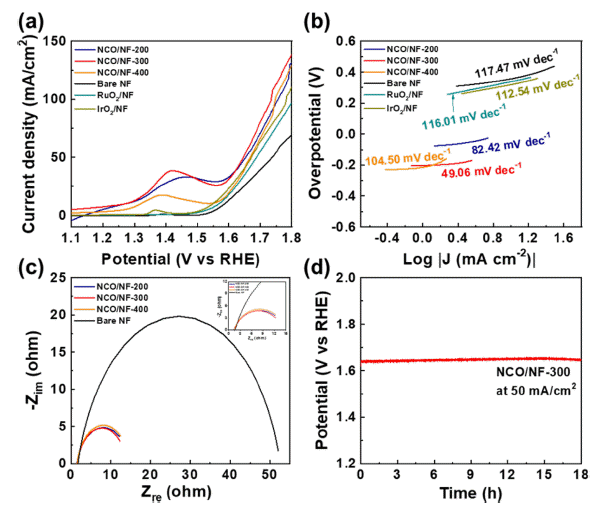
Fig. 1
Fig. 2
Fig. 3
Fig. 4
Fig. 5
Fig. 6
TOP
 KPMI
KPMI

 ePub Link
ePub Link Cite this Article
Cite this Article